Il grande complesso di molecole di editing genetico è difficile da trasferire nelle cellule da un'applicazione esterna. Le nanoparticelle lipidiche biodegradabili forniscono la codifica dell'mRNA per le molecole di modifica genica nella cellula Credito:dall'animazione di Visual Science e Skoltech, visual-science.com/crispr
Una collaborazione di ricerca tra la Tufts University e l'Accademia cinese delle scienze ha portato allo sviluppo di un meccanismo di somministrazione significativamente migliorato per il metodo di editing genetico CRISPR/Cas9 nel fegato, secondo uno studio pubblicato di recente sulla rivista Materiale avanzato . La consegna utilizza nanoparticelle lipidiche sintetiche biodegradabili che trasportano gli strumenti di modifica molecolare nella cellula per alterare con precisione il codice genetico delle cellule con un'efficienza fino al 90%. Le nanoparticelle rappresentano uno degli strumenti di consegna CRISPR/Cas9 più efficienti segnalati finora, secondo i ricercatori, e potrebbe aiutare a superare gli ostacoli tecnici per consentire l'editing genetico in un'ampia gamma di applicazioni terapeutiche cliniche.
Il sistema di editing genetico CRISPR/Cas9 è diventato un potente strumento di ricerca che scopre la funzione di centinaia di geni ed è attualmente esplorato come strumento terapeutico per il trattamento di varie malattie. Però, rimangono alcuni ostacoli tecnici prima che possa essere pratico per le applicazioni cliniche. CRISPR/Cas9 è un grande complesso molecolare, contenente sia una nucleasi (Cas9) che può tagliare entrambi i filamenti di una sequenza genomica mirata, e un RNA ingegnerizzato "a guida singola" (sgRNA) che scansiona il genoma per aiutare la nucleasi a trovare quella sequenza specifica da modificare. Poiché è un grande complesso molecolare, è difficile rilasciare CRISPR/Cas9 direttamente nel nucleo della cellula, dove può svolgere il suo lavoro. Altri hanno impacchettato le molecole di modifica in virus, polimeri, e diversi tipi di nanoparticelle per farle entrare nel nucleo, ma la bassa efficienza del trasferimento ne ha limitato l'uso e la potenza per le applicazioni cliniche.
Le nanoparticelle lipidiche descritte nello studio incapsulano l'RNA messaggero (mRNA) che codifica per Cas9. Una volta che il contenuto delle nanoparticelle, compreso lo sgRNA, viene rilasciato nella cellula. Il macchinario per la produzione di proteine della cellula prende il sopravvento e crea Cas9 dallo stampo dell'mRNA, completando il kit di editing genetico. Una caratteristica unica delle nanoparticelle è costituita da lipidi sintetici che comprendono legami disolfuro nella catena grassa. Quando le particelle entrano nella cellula, l'ambiente all'interno della cellula rompe il legame disolfuro per disassemblare le nanoparticelle e il contenuto viene rilasciato rapidamente ed efficientemente nella cellula.
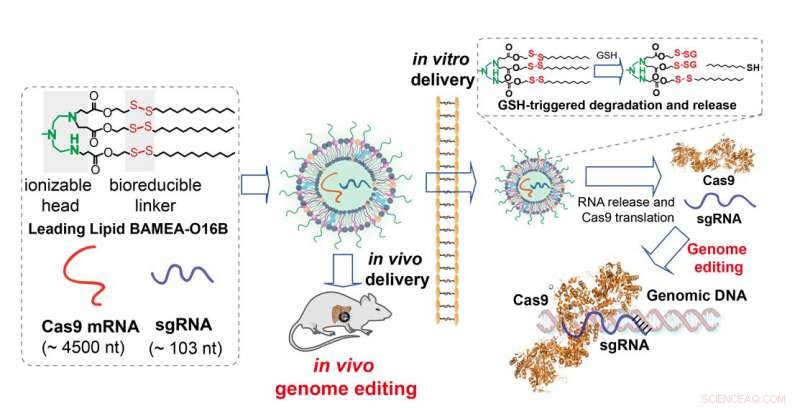
I lipidi formulati con un linker bioriducibile formano la parete di nanoparticelle che incapsulano l'mRNA di Cas9 più sgRNA. Entrando nella cella, in vitro o in vivo, i linker sono rotti e le particelle si disintegrano per la consegna dei contenuti e la traduzione dell'mRNA in enzima attivo per l'editing del genoma CRISPR/Cas9 Credito:Qiaobing Xu, Tufts University
"Stiamo appena iniziando a vedere studi clinici sull'uomo per le terapie CRISPR, " disse Qiaobing Xu, co-autore dello studio e professore associato di ingegneria biomedica alla Tufts University. "Ci sono molte malattie che sono state a lungo intrattabili per le quali le terapie CRISPR potrebbero offrire nuove speranze, ad esempio l'anemia falciforme, Distrofia muscolare di Duchenne, Malattia di Huntington, e anche molti tumori. La nostra speranza è che questo progresso ci faccia fare un altro passo avanti per rendere CRISPR un approccio efficace e pratico al trattamento".
I ricercatori hanno applicato il nuovo metodo ai topi, cercando di ridurre la presenza di un gene che codifica per PCSK9, la cui perdita è associata a una riduzione del colesterolo LDL, e ridotto rischio di malattie cardiovascolari. "Le nanoparticelle lipidiche sono uno dei vettori CRISPR/Cas9 più efficienti che abbiamo visto, " ha detto Ming Wang, anche co-autore dello studio e professore all'Accademia cinese delle scienze, Laboratorio nazionale di Pechino per le scienze molecolari. "Possiamo effettivamente abbattere l'espressione di PCSK9 nei topi con l'80% di efficienza nel fegato, suggerendo una vera promessa per applicazioni terapeutiche."