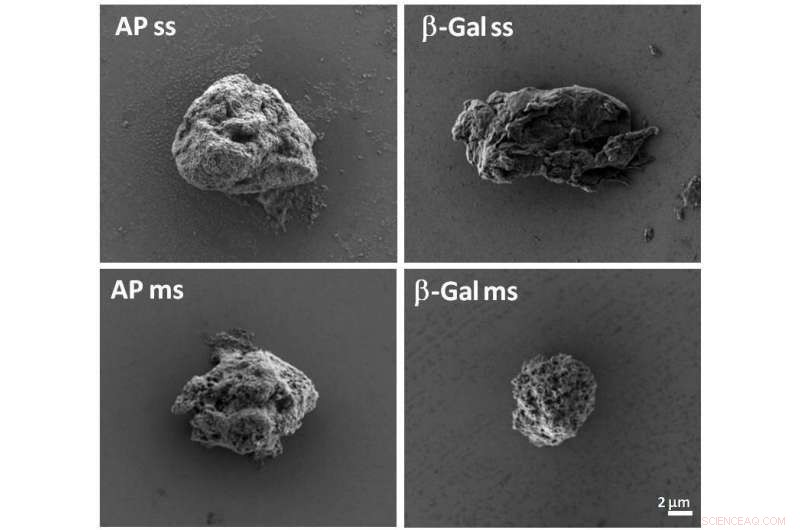
Corpi di inclusione artificiale. Credito:CIBER-BBN , UAB, IR Sant Pau
La medicina di precisione sta diventando sempre più importante, creare terapie personalizzate più efficienti per ogni paziente e sviluppi farmacologici innovativi. In campo oncologico, Per esempio, i ricercatori stanno sviluppando diversi approcci volti a sistemi di rilascio diretto e controllato di farmaci, diminuendo così la tossicità per l'organismo.
In questo senso, ricercatori della Bioingegneria del CIBER, Settore Biomateriali e Nanomedicina (CIBER-BBN), l'Istituto di Biotecnologia e Biomedicina dell'Universitat Autònoma de Barcelona (IBB-UAB) e l'Hospital Sant Pau Research Institute hanno sviluppato un nuovo tipo di biomateriale proteico in grado di un rilascio prolungato di proteine terapeutiche somministrate per via sottocutanea in animali da laboratorio.
"Queste strutture, misura pochi micrometri di diametro, contengono proteine funzionali che vengono rilasciate in modo simile a come gli ormoni umani vengono rilasciati dal sistema endocrino, " afferma Antonio Villaverde, ricercatore presso l'UAB e il CIBER-BBN e uno dei coordinatori dello studio.
Lo studio è il risultato di una collaborazione scientifica stabile tra il gruppo di Antonio Villaverde e il gruppo guidato da Ramon Mangues presso l'Hospital Sant Pau Research Institute. Ha incluso anche il coinvolgimento dell'Istituto per la Ricerca Biologica e Tecnologica dell'Università Nazionale di Cordoba-CONICET in Argentina.
Dottor Mangues, anche ricercatore presso il CIBER-BBN e coautore del paper, spiega che "il nuovo biomateriale imita un prodotto batterico che si trova comunemente nei processi biotecnologici noti come 'corpi di inclusione, ' che sono di interesse farmacologico, e che in questa versione artificiale offrono un'ampia gamma di possibilità terapeutiche per il campo oncologico e per qualsiasi altro settore clinico in cui sia necessario un rilascio prolungato."
I ricercatori hanno utilizzato come modelli enzimi comuni alla biotecnologia e una tossina batterica nanostrutturata diretta alle cellule metastatiche del cancro del colon-retto umano, che sono stati testati su modelli animali. "In questo modo, siamo riusciti a generare altrettanti catalizzatori immobili un nuovo farmaco antitumorale ad azione prolungata, " spiegano i principali autori dello studio.
Enorme potenziale clinico
I granuli proteici artificiali sviluppati qui, che in precedenza erano state proposte come "nanopills" (pillole terapeutiche su scala nanoscopica), imitano l'azione dei corpi di inclusione batterica e hanno un enorme potenziale clinico per i vaccini e i sistemi di somministrazione di farmaci a rilascio controllato.
"Abbiamo visto che i corpi di inclusione naturali, somministrati come farmaci, può produrre risposte indesiderate del sistema immunitario a causa dell'inevitabile contaminazione dei materiali batterici, " affermano i ricercatori. Tuttavia, in questo nuovo studio, lo sviluppo di corpi di inclusione artificiali con una capacità di secrezione "previene molti dei problemi normativi associati al potenziale sviluppo di nanopillole batteriche, ' e offre una piattaforma trasversale attraverso la quale ottenere componenti funzionali per usi cosmetici e clinici, "aggiungono.
Questo studio suggerisce che i corpi di inclusione artificiale possono diventare una nuova categoria di biomateriali sfruttabili da utilizzare in applicazioni biotecnologiche, per la struttura con cui sono fabbricati e per la previsione di future applicazioni cliniche.