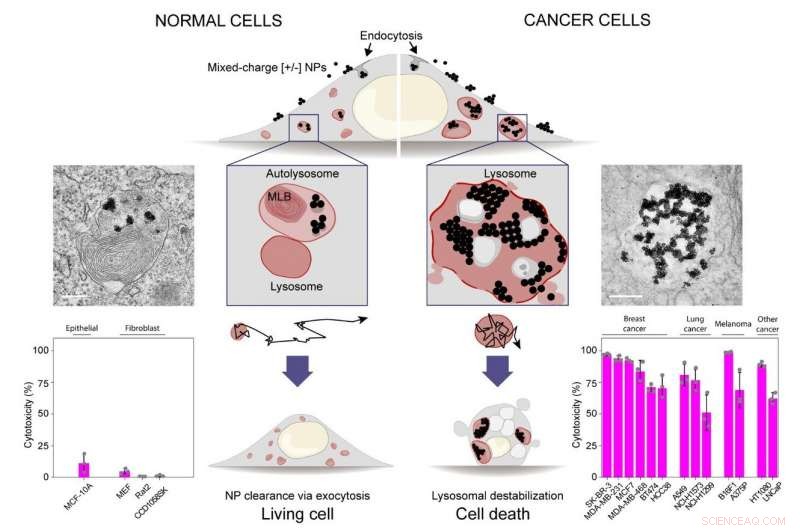
Nanoparticelle a carica mista per la destabilizzazione dei lisosomi cancerosi e l'uccisione selettiva delle cellule cancerose. Gli istogrammi nella riga in basso mostrano che le nanoparticelle a carica mista uccidono selettivamente tredici linee cellulari cancerose (istogramma a destra), pur non danneggiando quattro normali tipi/linee di cellule epiteliali o fibroblasti (istogramma a sinistra). Credito:IBS
Un team di ricercatori del Center for Soft and Living Matter, all'interno dell'Istituto di Scienze di Base (IBS, Corea del Sud) e affiliato con l'Ulsan National Institute of Science and Technology (UNIST) ha scoperto un nuovo approccio per mirare selettivamente e uccidere diversi tipi di cellule tumorali.
I lisosomi sono piccole sacche piene di un gran numero di enzimi e acidi che lavorano per abbattere e riciclare componenti cellulari danneggiati e indesiderati. In altre parole, sono contemporaneamente sia il contenitore dei rifiuti di una cellula che il centro di riciclaggio. Tipicamente, i lisosomi eliminano i sottoprodotti di questo processo di degradazione rilasciandoli all'esterno della cellula. Rilasciare la spazzatura all'esterno ha solo senso. Per esempio, immagina di raccogliere tutta la spazzatura di casa tua in un bidone e poi svuotare lo stesso cestino proprio sul pavimento in cucina, rendendo le tue condizioni di vita miserabili. Allo stesso modo, perforare i lisosomi e rilasciare il loro contenuto tossico all'interno della cellula danneggia irreparabilmente i componenti cellulari che, in casi estremi, può innescare la morte cellulare.
Poiché i lisosomi cancerosi sono più facili da danneggiare rispetto ai lisosomi delle cellule sane, gli scienziati hanno cercato di utilizzare questa strategia come un'alternativa promettente per colpire i tumori resistenti ai trattamenti convenzionali. Però, solo una manciata di potenziali terapie può colpire i lisosomi, e la maggior parte di loro manca di selettività contro il cancro.
Pubblicato in Nanotecnologia della natura , questo studio mostra che le nanoparticelle ricoperte da una miscela di molecole caricate positivamente [+] e negativamente [-] possono uccidere selettivamente le cellule tumorali prendendo di mira i loro lisosomi. La morte delle cellule cancerose deriva da una notevole successione di fenomeni di trasporto e di aggregazione, iniziando con la formazione di piccoli cluster di nanoparticelle sulle superfici cellulari e culminando con l'assemblaggio di cristalli di nanoparticelle di dimensioni micron all'interno dei lisosomi del cancro. I cristalli di nanoparticelle inducono gonfiore lisosomiale, perdita graduale dell'integrità delle membrane lisosomiali, e infine morte cellulare.
"In questo lavoro, abbiamo sfruttato il sistema di gestione dei rifiuti deregolamentato delle cellule tumorali per agire come una "catena di assemblaggio su scala nanometrica" per la costruzione di cristalli di nanoparticelle di alta qualità che distruggono i "reattori" lisosomiali che hanno permesso loro di crescere in primo luogo, " dice Bartosz A. Grzybowski, co-autore principale dello studio.
L'aggregazione di nanoparticelle a carica mista è favorita dall'ambiente acido tipico delle cellule cancerose. "Cellule non cancerose, però, internalizzano anche nanoparticelle a carica mista, ma l'aggregazione delle nanoparticelle è limitata. Le nanoparticelle transitano rapidamente attraverso le vie di riciclaggio e vengono eliminate da queste cellule, " spiega Kristiana Kandere-Grzybowska, co-autore principale dello studio.
"Le nostre conclusioni si basano su un confronto di tredici diversi sarcomi, melanoma, linee cellulari di carcinoma mammario e polmonare con quattro tipi di cellule non cancerose, " aggiunge il primo autore dello studio, Magdalena Borkowska. "Le nanoparticelle erano efficaci contro tutte e tredici le linee di cancro, pur non danneggiando le cellule non cancerose".
L'aggregazione delle nanoparticelle mentre transitano attraverso il sistema endolisosomiale delle cellule cancerose è un processo complesso. Il team ha scoperto che le nanoparticelle con una composizione superficiale di circa l'80% [+] e il 20% [-] di ligandi mostrano una selettività del cancro ottimale. Il fatto che i ligandi carichi negativamente siano anche sensibili al pH sembra essere la chiave per la selettività del cancro. Nel pH acido, trovato intorno alle cellule cancerose e all'interno dei lisosomi, questi ligandi sono protonati e inclini a interagire con ligandi simili sulle nanoparticelle vicine, favorendone così l'aggregazione. L'equilibrio tra le interazioni attrattive, i legami tra i ligandi [-] e le interazioni forti tra i nuclei delle nanoparticelle, e le repulsioni elettrostatiche tra i ligandi [+] sulle particelle vicine determinano l'entità dell'aggregazione delle nanoparticelle. Globale, le interazioni tra le particelle, le proteine del siero e l'ambiente interno delle cellule lavorano di concerto per danneggiare i lisosomi del cancro.
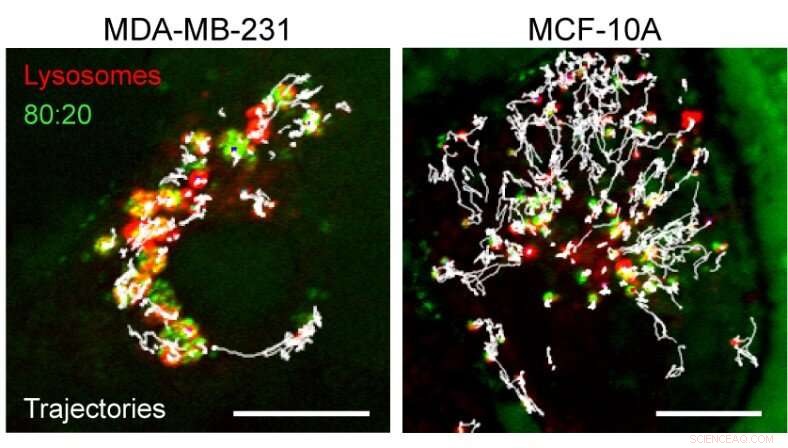
L'effetto dell'aggregazione delle nanoparticelle all'interno dei lisosomi. L'immagine mostra le traiettorie (bianco) dei lisosomi (rosso) nel cancro (a sinistra) rispetto alle cellule normali (a destra). Gli aggregati di nanoparticelle (verdi) nelle cellule tumorali hanno compromesso la capacità dei lisosomi di esaminare l'interno della cellula. Barra della scala, 10?m. Credito:IBS
"I cluster di nanoparticelle possono alterare la composizione lipidica della membrana del lisosoma, pregiudicarne l'integrità e renderlo meno robusto meccanicamente. inaspettatamente, il nostro team ha anche scoperto che alcune proteine, come le molecole di segnalazione della crescita cellulare mTORC1, vengono spostati (e quindi inibiti) dalla superficie dei lisosomi cancerosi contenenti nanoparticelle. Questo è importante perché la crescita e la divisione delle cellule tumorali richiedono mTORC1, e le nanoparticelle lo stanno spegnendo solo nelle cellule tumorali, " spiega Kandere-Grzybowska.
Mentre le singole nanoparticelle hanno approssimativamente le stesse dimensioni di una molecola proteica media, e quindi troppo piccolo per essere visto con la maggior parte degli approcci di microscopia a cellule vive dinamiche, si possono osservare i cristalli composti da più nanoparticelle. Il team ha utilizzato una combinazione di approcci complementari, compresa la microscopia in campo oscuro, microscopia confocale a riflessione, e TEM, nonché approcci biochimici e computazionali per valutare il pieno impatto delle nanoparticelle a carica mista sugli organelli lisosomiali.
Questo studio apre nuove direzioni di ricerca. La strategia della carica mista potrebbe essere applicata ad altri tipi di nanoparticelle, come particelle a base di polimeri, dendrimeri o nanoparticelle di ossido di ferro. Un altro passo importante sarà testare l'efficacia delle nanoparticelle a carica mista contro i tumori in modelli animali.