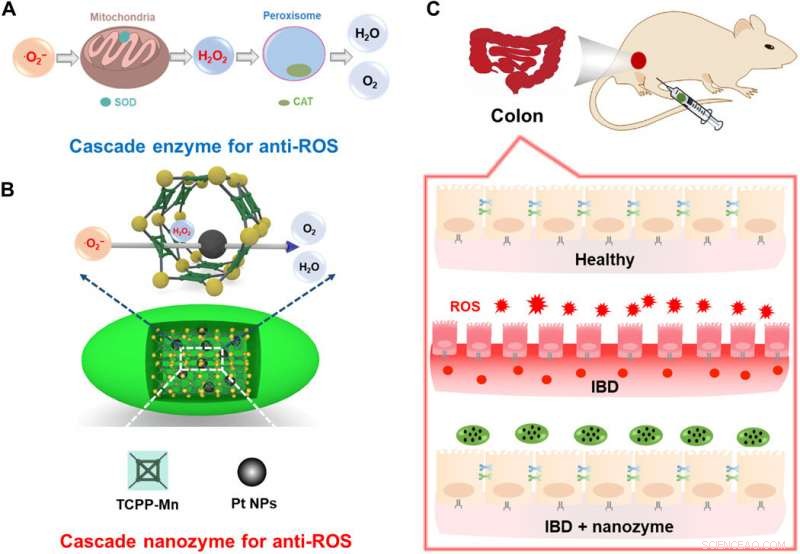
Illustrazione schematica del progetto di un nanozima integrato con attività anti-ROS a cascata per la terapia dell'IBD. (A) Enzimi a cascata cellulare per anti-ROS. L'efficacia terapeutica di un tale sistema è limitata a causa delle diverse posizioni subcellulari degli enzimi SOD e CAT e della limitata stabilità extracellulare. (B) Costruzione di un nanozima a cascata per la terapia anti-ROS incorporando Pt NP all'interno di PCN222-Mn MOF. La vicinanza su nanoscala dei siti catalitici attivi favorisce le reazioni a cascata. (C) L'IBD dei topi può essere efficacemente alleviato attraverso il trattamento con il nanozima a cascata integrato. Credito:progressi scientifici, doi:10.1126/sciadv.abb2695
In un recente rapporto, Yufeng Liu e un team di ricercatori interdisciplinari in Cina hanno sviluppato una cascata di nanozimi integrata per eliminare le specie reattive dell'ossigeno in eccesso (ROS; radicali liberi dell'ossigeno). Il nanozima imitava la superossido dismutasi (un gruppo di enzimi) e incorporava una struttura metallo-organica (MOF) a base di manganese (Mn) per trasformare i radicali dell'ossigeno in perossido di idrogeno (H 2 oh 2 ). Utilizzando esperimenti in laboratorio e in vivo, il team ha mostrato il potenziale di eliminazione dei ROS dei nanozimi a cascata integrati. Come prova del concetto, hanno alleviato due forme di disturbo infiammatorio intestinale (IBD):la colite ulcerosa e il morbo di Crohn utilizzando nanozimi a cascata come trattamenti efficaci. Lo studio ha fornito un nuovo metodo per costruire sistemi a cascata simili a enzimi e illustrare la promessa della loro terapia efficiente per il trattamento dell'IBD in vivo. L'opera è ora pubblicata su Progressi scientifici .
Durante le reazioni catalitiche a cascata che si verificano negli organismi viventi, più enzimi sono combinati all'interno di compartimenti subcellulari per un'accurata trasduzione del segnale e un metabolismo efficace. Tali reazioni a cascata confinate sono vantaggiose rispetto alle reazioni a più stadi convenzionali a causa delle barriere di diffusione ridotte e delle concentrazioni locali migliorate di intermedi per una migliore economia atomica e reazioni in totale. Gli scienziati hanno compiuto sforzi sostanziali per imitare tali sistemi a cascata su impalcature, ma il loro alto costo e la loro bassa stabilità hanno limitate ampie applicazioni pratiche. Di conseguenza, i ricercatori hanno esplorato imitazioni enzimatiche per comprendere e costruire reazioni a cascata in laboratorio. In questo lavoro, Liu e al. ha dettagliato un sistema di reazione a cascata a singolo componente basato su nanozimi con elevata attività e ha dimostrato il loro ruolo durante la terapia in vivo della malattia infiammatoria intestinale (IBD) associata a specie reattive dell'ossigeno (ROS).
Design, sintesi e caratterizzazione dello scaffold enzimatico
Il team ha progettato e sintetizzato un nanozima a cascata mimetico integrato di superossido dismutasi (SOD) e catalasi (CAT) e lo ha designato come Pt@PCN222-Mn. Per costruire l'impalcatura, hanno introdotto una porzione simile alla SOD di porfirina di manganese (Mn) (III) e una nanoparticella di platino simile a CAT all'interno di una struttura metallica organica (MOF) a base di zirconio (Zr) su scala nanometrica denominata PCN222. Il costrutto integrato (Pt@PCN222-Mn) ha mostrato una maggiore attività di scavenging dei ROS per proteggere i topi dall'IBD correlato ai ROS, una malattia cronica ancora incurabile, e quindi ampliare il potenziale dei nanozimi a cascata per applicazioni biomediche in vivo.
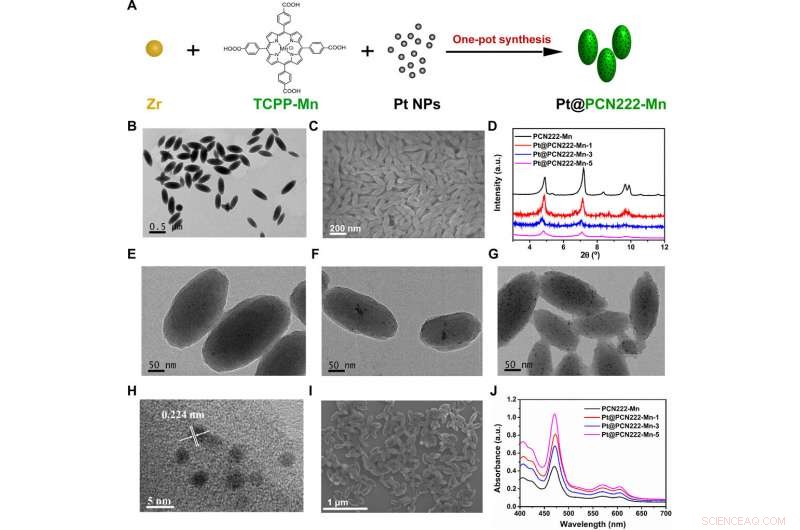
Sintesi e caratterizzazione strutturale di Pt@PCN222-Mn e materiali correlati. (A) Procedura di sintesi di Pt@PCN222-Mn. (B) Microscopio elettronico a trasmissione (TEM) e (C) Immagini al microscopio elettronico a scansione (SEM) di PCN222-Mn. (D) Modelli di diffrazione dei raggi X su polvere (PXRD) di PCN222-Mn, Pt@PCN222-Mn-1, Pt@PCN222-Mn-3, e Pt@PCN222-Mn-5. Immagini TEM di (E) Pt@PCN222-Mn-1, (F) Pt@PCN222-Mn-3, e (G) Pt@PCN222-Mn-5. (H) Immagini TEM ad alta risoluzione e (I) SEM di Pt@PCN222-Mn-5. (J) Spettri di assorbimento di PCN222-Mn, Pt@PCN222-Mn-1, Pt@PCN222-Mn-3, e Pt@PCN222-Mn-5. a.u., unità arbitrarie. Credito:progressi scientifici, doi:10.1126/sciadv.abb2695
Durante gli esperimenti, Liu et al. ha confermato la riuscita sintesi dei costrutti preliminari a base di manganese mediante risonanza magnetica nucleare, Spettroscopia infrarossa in trasformata di Fourier e misure spettroscopiche nell'ultravioletto visibile. Il team ha sintetizzato il componente contenente un MOF su nanoscala e ha confermato la sua formazione con la microscopia elettronica a trasmissione (TEM) e la microscopia elettronica a scansione (SEM). Gli scienziati hanno quindi sviluppato tre nanozimi a cascata e li hanno denominati Pt@PCN222-Mn-1, Pt@PCN222-Mn-3 e Pt@PCN222-Mn-5, rispettivamente. Di questi, Pt@PCN222-Mn-5 aveva un'area superficiale maggiore rispetto ad altri nanoenzimi anti-ROS studiati finora.
Indagare l'attività catalitica dei nanozimi a cascata
Scavenging per i radicali dell'ossigeno ( • oh 2 − ) è la fase iniziale della reazione a cascata anti-ROS, quindi il team ha studiato l'attività catalitica dei costrutti sintetici per monitorare la loro capacità di eliminare allo stesso modo i radicali dell'ossigeno. Il lavoro ha evidenziato il ruolo chiave del manganese nella porfirina per imitare le attività simili alla superossido dismutasi (SOD) dei diversi costrutti enzimatici, dove i costrutti Pt@PCN222-Mn-5 hanno mostrato la più alta attività simile a SOD tra i mimici enzimatici. Il team ha confermato i risultati utilizzando la spettroscopia di risonanza paramagnetica elettronica (EPR).
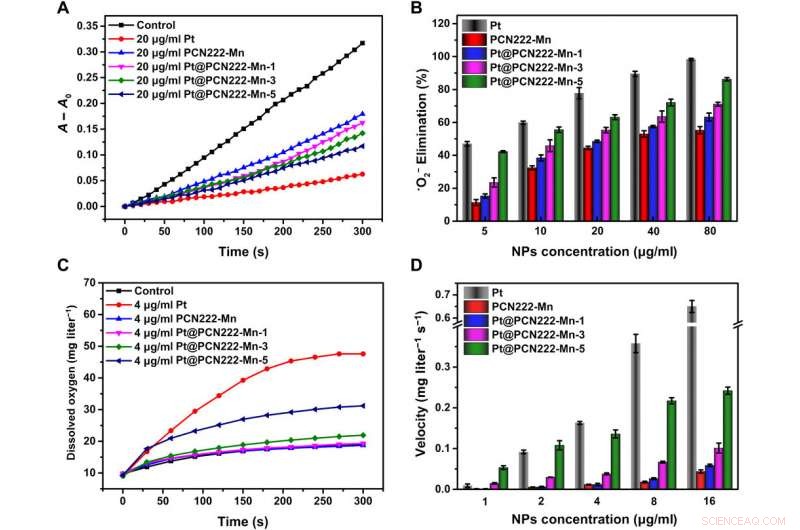
Attività di ROS-scavenging di Pt@PCN222-Mn e materiali correlati. (A) Curve cinetiche tipiche di A - A0 (550 nm) per monitorare la riduzione di NBT con X e XO in assenza e presenza di Pt, PCN222-Mn, Pt@PCN222-Mn-1, Pt@PCN222-Mn-3, e Pt@PCN222-Mn-5. (B) Dipendenza tra l'efficienza di eliminazione di •O2− e le concentrazioni di nanozimi. (C) Curve cinetiche tipiche della generazione di ossigeno dalla decomposizione di H2O2 (50 mM) in presenza di Pt, PCN222-Mn, Pt@PCN222-Mn-1, Pt@PCN222-Mn-3, e Pt@PCN222-Mn-5. (D) Dipendenza tra le velocità di produzione di ossigeno nei primi 60 s e le concentrazioni di nanozimi. I dati sono mostrati come medie ± SD (n =3). Credito:progressi scientifici, doi:10.1126/sciadv.abb2695
Come secondo passo cruciale nella cascata di ROS-scavenging negli ambienti biologici, l'enzima CAT (catalasi) ha catalizzato la decomposizione del perossido di idrogeno (H 2 oh 2 ) in acqua e ossigeno. Liu et al. ha quindi monitorato le attività simili a CAT dei nanozimi monitorando l'ossigeno generato dal perossido di idrogeno in decomposizione. Come prima, Pt@PCN222-Mn-5 ha mostrato la più alta attività CAT-like tra i imitatori di enzimi basati su MOF. In base ai risultati, Liu et al. ha confermato che l'attività simile alla SOD deriva dalla frazione legata al manganese del costrutto enzimatico, mentre le nanoparticelle integrali di platino erano principalmente responsabili dell'attività simile a CAT.
Focus enzima Pt@PCN222-Mn-5 e terapia antinfiammatoria in vivo
Per comprendere appieno l'attività del nanozima a cascata Pt@PCN222-Mn-5, il team ha studiato la sua attività enzimatica sinergica simile a SOD e CAT e ha osservato effetti sinergici pronunciati per quest'ultimo. Il team ha scelto il nanozima per ulteriori indagini e ne ha testato la funzionalità con una linea cellulare durante gli studi di citotossicità. A una concentrazione inferiore a 80 µg/mL, il nanozima non ha mostrato alcuna citotossicità e ha dimostrato un eccellente potenziale di scansione delle specie reattive dell'ossigeno.
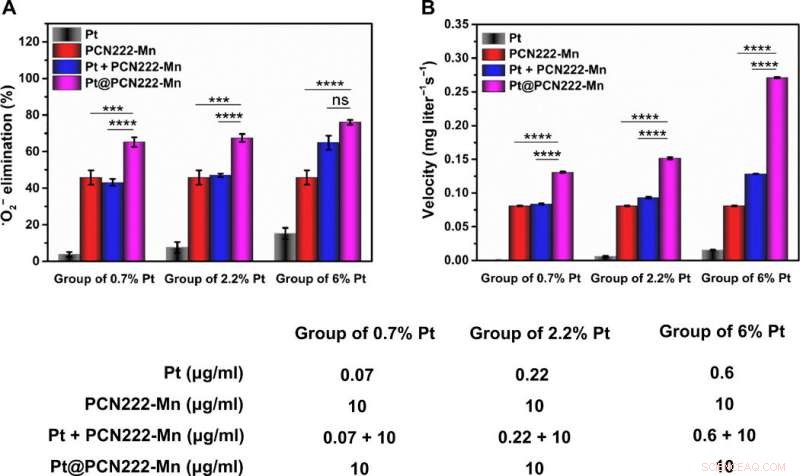
Attività sinergica di ROS-scavenging di Pt@PCN222-Mn-5. (A) Efficienza di eliminazione di •O2− con diverse concentrazioni di Pt, PCN222-Mn, Pt + PCN222-Mn, e Pt@PCN222-Mn. (B) Velocità di produzione di ossigeno nei primi 60 s, con diverse concentrazioni di Pt, PCN222-Mn, Pt + PCN222-Mn, e Pt@PCN222-Mn. I dati sono mostrati come medie ± SD (n =3). ***P <0,005 e ****P <0,001; ns, insignificante; prova. Credito:progressi scientifici, doi:10.1126/sciadv.abb2695
Sulla base dei risultati sperimentali, Liu et al. hanno condotto terapie in vivo per il trattamento della colite ulcerosa (CU) e del morbo di Crohn (MC) in modelli murini della malattia. Poiché la UC è una forma di disturbo infiammatorio intestinale che è tipicamente accompagnato da specie reattive dell'ossigeno in eccesso, gli scienziati hanno testato gli effetti terapeutici di Pt@PCN222-Mn-5 insieme ai farmaci esistenti per il trattamento dell'IBD. Il team ha somministrato il trattamento tramite iniezione intraperitoneale a ciascun topo e ha osservato effetti terapeutici efficaci di Pt@PCN222-Mn-5 per alleviare lo stato di malattia della UC nei topi. Il team ha ottimizzato le dosi del nanozima a cascata utilizzando diversi gruppi di trattamento e ha riscontrato che l'enzima principale di interesse è il più favorevole. Quando hanno esplorato allo stesso modo il CD, un altro tipo di IBD utilizzando un modello murino indotto da malattia, la strategia di trattamento ha indicato una maggiore efficacia per i nanozimi a cascata rispetto ai tradizionali farmaci a piccole molecole utilizzati nel trattamento dell'IBD.
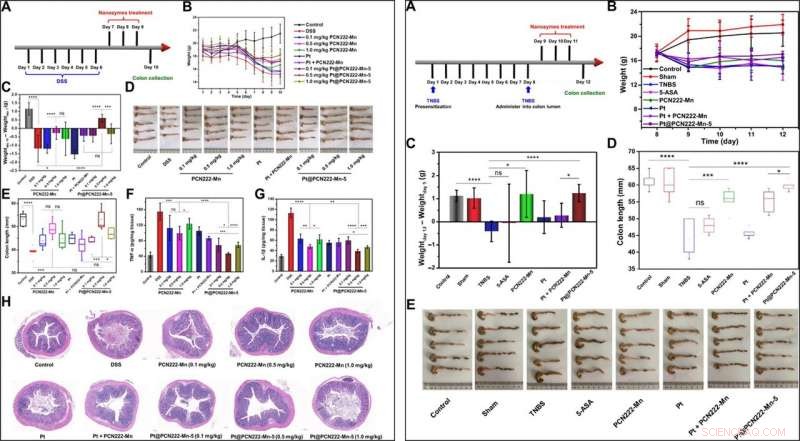
A SINISTRA:terapia UC con Pt@PCN222-Mn-5. (A) Procedura generale dell'esperimento sugli animali (colite indotta da DSS). (B) Sviluppo giornaliero del peso corporeo per 10 giorni. (C) Cambiamenti nel peso corporeo dei topi prima (giorno 7) e dopo i trattamenti indicati (giorno 10). (D) Immagini dei due punti e (E) le corrispondenti lunghezze dei due punti nei gruppi indicati. (F) Livelli di IL-1β e (G) TNF-α negli omogenati del colon dei gruppi indicati. (H) Sezioni del colon colorate con H&E di topi dei gruppi indicati il giorno 10. I dati sono mostrati come medie ± SD (n =5). *P <0,05, **P <0,01 ***P <0,005, e ****P <0,001; ns, insignificante; prova. Credito fotografico (D):Yufeng Liu, Facoltà di Ingegneria e Scienze Applicate, Università di Nanchino. A DESTRA:terapia CD con Pt@PCN222-Mn-5. (A) Procedura generale dell'esperimento sugli animali [2, 4, Colite indotta da acido 6-trinitrobenzensolfonico (TNBS). (B) Sviluppo giornaliero del peso corporeo dopo la somministrazione della soluzione di TNBS nel lume del colon. (C) Cambiamenti nel peso corporeo dei topi prima (giorno 9) e dopo i trattamenti indicati (giorno 12). (D) lunghezze dei due punti e (E) le immagini corrispondenti dei due punti dei gruppi indicati. I dati sono mostrati come medie ± SD (n =5). *P <0,05, ***P <0,005, e ****P <0,001; ns, insignificante; prova. Credito fotografico (E):Yuan Cheng, Facoltà di Ingegneria e Scienze Applicate, Università di Nanchino. Credito:progressi scientifici, doi:10.1126/sciadv.abb2695
In questo modo, Yufeng Liu e colleghi hanno sviluppato un nanozima integrato per catalizzare reazioni a cascata ed eliminare le specie reattive dell'ossigeno (ROS). Il nanozima integrato aveva due siti attivi spazialmente separati per imitare la superossido dismutasi (SOD) e la catalasi (CAT). Utilizzando esperimenti in laboratorio hanno mostrato l'eccezionale attività di ROS-scavenging del nanozima a cascata, la loro eccellente biocompatibilità e buona disperdibilità in acqua. Il team ha stabilito un modello animale infiammatorio per testare la capacità anti-ROS del nanozima a cascata in un organismo biologico e ha determinato il loro potenziale terapeutico superiore sia nei confronti dei modelli di colite ulcerosa (UC) che di malattia di Crohn (CD) di disturbo infiammatorio intestinale (IBD). Il team ha ottimizzato la concentrazione del nanozima per ottenere un efficace sollievo dall'IBD nei modelli animali. Il lavoro ha mostrato eccellenti attività di eliminazione dei ROS per il trattamento infiammatorio e fornisce un metodo promettente per costruire nanozimi con più siti attivi per ulteriori applicazioni in biomedicina.
© 2020 Scienza X Rete