
Un'immagine al microscopio a scansione in falsi colori di un array di transistor da 10 FET. Rosso:elastomero siliconico; Verde:PI; Azzurro:SU8; Giallo oro; Grigio:silicone. Credito:Gu et al.
Le cellule animali possono utilizzare elementi o ioni per generare impulsi elettrici. Questi impulsi vengono quindi convogliati da una cellula all'altra, viaggiando attraverso le reti cellulari.
La capacità di registrare con precisione i segnali elettrici scambiati dalle cellule potrebbe aiutare la ricerca e migliorare le pratiche in numerosi campi legati alla salute, tra cui cardiologia e neurologia. La maggior parte delle tecnologie esistenti, tuttavia, sono limitate sia nella precisione del rilevamento che nella scalabilità.
I ricercatori dell'Università della California di San Diego hanno recentemente sviluppato un dispositivo di rilevamento altamente sensibile che potrebbe essere utilizzato per registrare i segnali elettrici delle cellule con maggiore precisione. Questo dispositivo, presentato in un articolo pubblicato su Nature Nanotechnology , è composto da più sensori, che possono misurare collettivamente la propagazione di segnali elettrici scambiati da celle diverse o all'interno di singole celle.
Il recente studio è stato condotto dal Dr. Yue Gu mentre lavorava nel laboratorio del Prof. Sheng Xu presso la UC San Diego. Il dottor Gu, ora è un associato post-dottorato alla Yale University.
"La creazione della nostra struttura 3D, nota anche come architettura 'pop-up', si basa su un metodo unico, la tecnica di instabilità compressiva che ho sviluppato durante i miei studi post-dottorato nel 2015", il Prof. Xu, uno degli autori di il recente documento, ha detto a Phys.org. "La tecnica di instabilità compressiva sfrutta le tecniche di microfabbricazione in camera bianca convenzionali e versatili per generare sofisticate strutture 3D."
Le strutture 3D "pop-up" utilizzate dal Prof. Xu e dai suoi colleghi possono essere costruite utilizzando un'ampia gamma di materiali compatibili con le tecniche di microfabbricazione. I materiali di cui sono fatti possono a loro volta determinare la loro funzione, che potrebbe essere l'attenuazione delle onde elettromagnetiche, le vibrazioni meccaniche, la pressione e il rilevamento della deformazione o il rilevamento del segnale elettrico.

Fotografia di un array di transistor da 128 FET. Credito:Gu et al.
Nel loro studio, i ricercatori hanno deciso di costruire queste strutture 3D in modo che potessero essere utilizzate per registrare con precisione i segnali elettrici generati e scambiati dalle cellule. Il loro obiettivo principale era sfruttare efficacemente la versatilità della tecnica di instabilità compressiva per costruire un dispositivo in grado di raccogliere registrazioni intra e intercellulari accurate.
"L'inclusione di materiali semiconduttori e transistor di ingegneria in questa architettura pop-up estende l'applicazione della tecnica", ha spiegato il prof. Xu. "La nostra determinazione ad applicare questa struttura alle cellule, in particolare alle cellule muscolari cardiache, è stata innescata dalle discussioni che il dottor Gu e io abbiamo avuto con cardiologi e neurologi nel 2015, che si lamentavano delle difficoltà di registrazione dei segnali intracellulari utilizzando gli strumenti esistenti, come come patch-clamp, che è il gold standard per la registrazione dei segnali elettrici cellulari."
Dopo aver appreso delle sfide che i ricercatori medici stavano affrontando quando cercavano di raccogliere registrazioni precise di segnali elettrici cellulari, il dottor Xu e il dottor Gu hanno iniziato a sperimentare approcci ingegneristici unici che potrebbero semplificare il loro lavoro. In definitiva, ciò ha portato allo sviluppo del nuovo array di sensori introdotto nel loro recente articolo.
"Un altro obiettivo del nostro studio era l'implementazione di sensori intracellulari nei tessuti cardiaci ingegnerizzati in 3D", ha affermato il prof. Xu. "È risaputo che le proprietà elettrofisiologiche delle cellule variano quando si trovano in animali vivi, isolati dagli animali vivi e coltivate in piatti. La registrazione dei segnali in vivo è sempre il passaggio più significativo e tuttavia impegnativo."
Il Prof. Xu ei suoi colleghi sono stati i primi a raccogliere registrazioni intracellulari precise di cellule all'interno del tessuto cardiaco ingegnerizzato. Il loro studio potrebbe quindi essere un primo passo verso la raccolta di registrazioni cellulari in vivo affidabili.
"Il potenziale della membrana cellulare che polarizza il terminale di gate dei singoli transistor si traduce in una variazione della corrente dal drain al terminale di source dei transistor", ha spiegato il prof. Xu. "Pertanto, le fluttuazioni di corrente riflettono i potenziali di membrana momentanei. I transistor multipli nell'array che abbiamo sviluppato possono registrare simultaneamente segnali da diverse posizioni di una cella o da celle diverse."
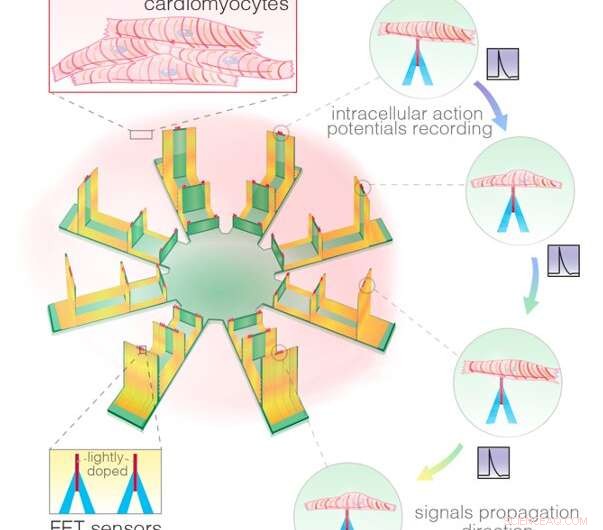
Un'immagine schematica mostra il rilevamento intracellulare da parte di un array di transistor da 128 FET e la registrazione delle propagazioni del segnale tra le cellule. Credito:Gu et al.
Per monitorare i comportamenti di propagazione del segnale all'interno e tra le cellule, il dispositivo dei ricercatori sequenzia i segnali raccolti dai suoi numerosi transistor. In contrasto con altri metodi proposti in precedenza per la raccolta di registrazioni cellulari, il nuovo dispositivo è in grado di monitorare più celle contemporaneamente. Inoltre, i suoi transistor possono mantenere intatti i potenziali di membrana cellulare a piena ampiezza, senza subire attenuazioni o impedenze associate al processo attraverso il quale accede alle cellule.
"Le superfici dei transistor funzionalizzate da materiali a doppio strato di fosfolipidi possono anche camuffare i transistor inorganici come cellule, il che facilita notevolmente il loro inserimento nel corpo cellulare", ha spiegato il prof. Xu. "In tali condizioni, l'interiorizzazione è descritta come un processo di fusione spontanea, che non lascia minimamente invasività alla cellula."
Il dispositivo di rilevamento sviluppato dal Prof. Xu e dai suoi colleghi può anche monitorare la velocità di conduzione del segnale elettrico all'interno di un cardiomiocita. Questa misurazione può essere di vitale importanza per il lavoro dei cardiologi, poiché confrontarla con la velocità di conduzione tra cellule vicine può aiutare a rilevare e comprendere alcune malattie cardiache, inclusa la fibrosi cardiaca.
"Come parte del nostro studio, abbiamo distribuito l'array di transistor nel tessuto cardiaco 3D e registrato per la prima volta i segnali elettrici intracellulari di singole cellule", ha affermato Xu. "Nel processo, abbiamo anche registrato la conduzione dei segnali elettrici e calcolato la loro velocità."
Finora, i ricercatori hanno testato il loro dispositivo di rilevamento basato su transistor principalmente sul tessuto cardiaco, ottenendo risultati molto promettenti. Le loro scoperte iniziali suggeriscono che potrebbe eventualmente essere utilizzato per raccogliere registrazioni precise di segnali elettrici prodotti e scambiati dalle cellule, sia in laboratorio che in vivo, sul cervello o sul cuore di animali vivi o pazienti umani.
"Ora stiamo perseguendo diversi nuovi obiettivi", ha aggiunto Xu. "Il primo consiste nell'utilizzare i nostri transistor per eseguire test in vivo su cuori o cervelli intatti. Il secondo è registrare le attività intracellulari dei neuroni in diverse posizioni neuronali. Infine, poiché alcune cellule endocrine sono anche elettrogeniche, il che significa che le loro attività elettriche sono legati ad altri eventi fisiologici, sono anche di grande interesse". + Esplora ulteriormente
© 2022 Rete Science X