In generale, maggiore è il grado di ripristino delle informazioni di un vaccino rispetto a un virus, maggiore è la sua potenziale efficacia. Il virus stesso è il vaccino più autentico, come il virus varicella-zoster, che fornisce un’immunità permanente dopo una singola infezione. Tuttavia, i virus evolvono anche meccanismi per eludere la sorveglianza immunitaria nel corso della loro lunga storia evolutiva, ad esempio eludendo la ricerca del sistema immunitario cambiando frequentemente travestimenti attraverso un'elevata mutabilità.
In alternativa, possono ridurre la propria visibilità e nascondersi in modo invasivo attraverso meccanismi speciali, e i coronavirus sono abili nell'utilizzare entrambe queste tattiche.
Essendo un virus a RNA, i coronavirus hanno il vantaggio naturale di essere altamente mutabili. Nel frattempo, chiamati "corona" a causa delle sporgenze a forma di corona sulla loro superficie, i coronavirus mostrano le informazioni antigeniche più cruciali sulla proteina del dominio legante il recettore (RBD) situata nella parte superiore di queste sporgenze a forma di corona.
L'informazione antigenica è sparsa tra i picchi solitari sulla superficie virale, somiglianti ad una corona. Questa struttura spazialmente discreta è difficile da riconoscere in modo efficace per il sistema immunitario.
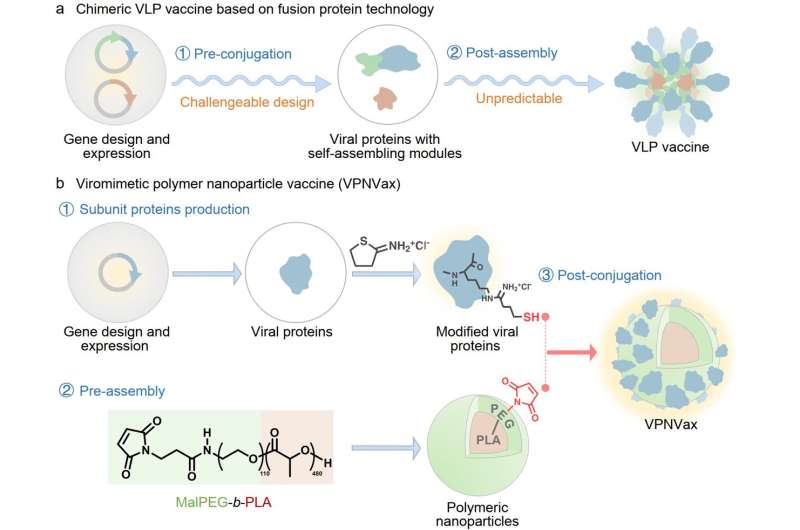
Affrontando le caratteristiche strutturali dei coronavirus, un team guidato dai professori Xuesi Chen e Wantong Song dell’Istituto di chimica applicata di Changchun ha segnalato un vaccino con nanoparticelle polimeriche viromimetiche (VPNVax). Il vaccino è stato preparato riorganizzando le proteine RBD del coronavirus e modificandole sulla superficie di nanoparticelle polimeriche preassemblate di polietilenglicole e acido polilattico.
Questa strategia di preparazione modulare offre numerosi vantaggi:(1) consente un controllo flessibile della densità dell'antigene (valenza) sulla superficie del vaccino a nanoparticelle; (2) consente la sostituzione delle proteine antigeniche per rispondere rapidamente alle epidemie di diverse varianti virali; (3) facilita la trasformazione diretta da proteine di subunità a vaccini a nanoparticelle, ottimizzando il processo di preparazione rapida su larga scala.
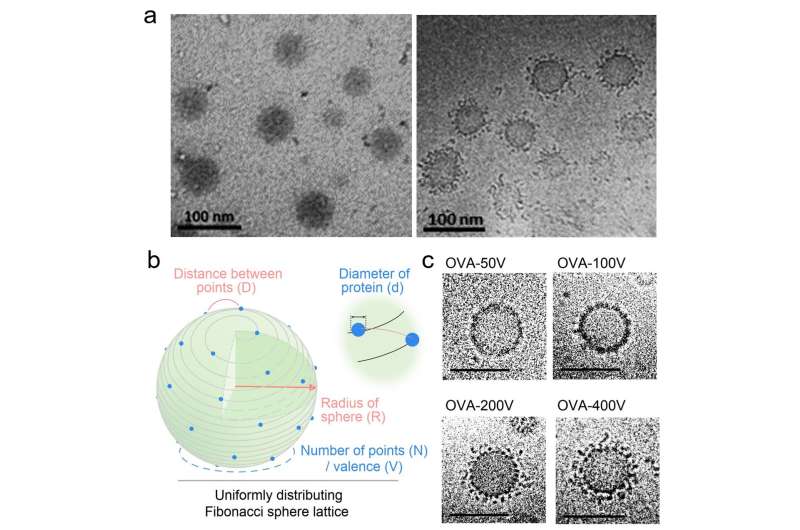
La morfologia di VPNVax al microscopio crioelettronico è estremamente simile alla struttura del virus, con proteine antigeniche densamente distribuite sulla superficie sferica del trasportatore di nanoparticelle. Attraverso calcoli teorici utilizzando il modello del reticolo sferico di Fibonacci e la regolazione delle condizioni di reazione chimica, il team di ricerca ha preparato con successo VPNVax con diverse valenze superficiali.
I risultati hanno mostrato che la valenza dell'antigene di superficie ha effettivamente avuto un impatto significativo sull'effetto immunostimolante del vaccino a nanoparticelle. Una maggiore densità di antigene sulla superficie di VPNVax migliora la sua capacità di attivazione diretta sulle cellule B, convalidando indirettamente il meccanismo del coronavirus di eludere la sorveglianza immunitaria riducendo la densità di antigene di superficie attraverso protrusioni simili a corona.
Ciò ha inoltre sottolineato la necessità di ottimizzare e controllare la valenza superficiale dei vaccini a nanoparticelle. Tuttavia, una valenza eccessivamente elevata ha anche ridotto la stabilità strutturale di VPNVax, rendendo necessaria una valenza moderata per raggiungere un equilibrio tra effetti stimolatori e stabilità.
Il gruppo di ricerca ha inoltre scoperto che per le proteine antigeniche di diverse dimensioni, l'effetto immunostimolante ottimale del VPNVax preparato si verificava quando la copertura proteica superficiale era compresa tra il 20% e il 25%. Inoltre, il VPNVax con parametri strutturali ottimali, se combinato con adiuvanti commerciali in alluminio, ha ottenuto un effetto di stimolazione immunitaria più forte e il suo siero immunitario ha dimostrato di avere effetti di neutralizzazione del virus.
Ancora più importante, questa piattaforma vaccinale basata su polimeri può sviluppare e sfruttare ulteriormente la funzione adiuvante del trasportatore polimerico. Trasportando agonisti immunitari o regolando la chiralità del polimero, VPNVax potrebbe attivare contemporaneamente le risposte immunitarie cellulari.
In sintesi, la ricerca condotta sulla piattaforma VPNVax riguardante la relazione struttura-effetto dei vaccini con nanoparticelle e la strategia di preparazione che combina la tecnologia di sintesi dei materiali offre nuove intuizioni per la progettazione della prossima generazione di vaccini con particelle simili a virus.
Il lavoro è pubblicato sulla rivista National Science Review .
Ulteriori informazioni: Zichao Huang et al, Vaccini modulari con nanoparticelle polimeriche viromimetiche (VPNVax) per suscitare risposte immunitarie umorali durature ed efficaci, National Science Review (2023). DOI:10.1093/nsr/nwad310
Fornito da Science China Press