Un team guidato dal Prof. Wang Yucai e dal Prof. Associato Jiang Wei dell'Università di Scienza e Tecnologia della Cina (USTC) dell'Accademia Cinese delle Scienze (CAS) ha rivelato il meccanismo delle membrane basali vascolari (BM) del tumore che bloccano le nanoparticelle ( NP) per la prima volta e ha sviluppato una strategia immunoguidata per aumentare la penetrazione delle NP attraverso la barriera del midollo osseo. Il loro lavoro è stato pubblicato su Nature Nanotechnology .
Precedenti ricerche sul trasporto nanoterapeutico dal sistema vascolare al tumore dipendevano principalmente dall'effetto Enhanced Permeability and Retention (EPR), che ritiene che le NP possano attraversare la barriera endoteliale vascolare del tumore, l'ultima difesa della penetrazione delle NP, sfruttando l'elevata permeabilità delle vasi tumorali. Tuttavia, studi clinici hanno scoperto che le NP trasportano solo circa lo 0,7% dei farmaci all'interno del tumore, suggerendo altri meccanismi per ostacolare la penetrazione delle NP.
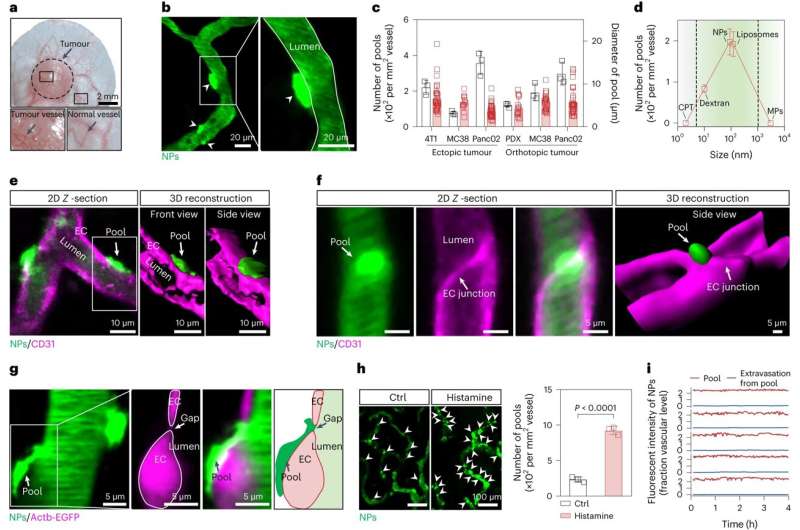
Per far luce su questo meccanismo sottovalutato, il team ha utilizzato la microscopia intravitale non invasiva multifase e ha rivelato che il midollo osseo che circonda le cellule endoteliali e le cellule murali dei vasi tumorali impedisce gravemente lo stravaso di NP, formando pool di NP perivascolari nel vuoto subendoteliale.
Dopo aver analizzato accuratamente il posizionamento spaziale, la microstruttura e le cause dei pool di NP, il team ha inoltre scoperto che la degradazione enzimatica del BM potrebbe ridurre significativamente il pool di NP, aumentando l'efficienza di trasporto della nanomedicina. Sulla base di questa scoperta, il team ha sviluppato una strategia immunoguidata utilizzando gli enzimi proteolitici localizzati rilasciati dai leucociti infiammatori per creare una finestra temporanea sul midollo osseo, consentendo un rilascio esplosivo di NP in profondità nel tumore, migliorando significativamente l’arricchimento dei nanomedicinali e l’effetto terapeutico.
Lo studio non solo propone una nuova strategia di trasporto della nanomedicina distinta dall'EPR, ma fornisce anche un nuovo supporto teorico per l'applicazione delle nanoterapie nel cancro, facendo avanzare la comprensione del meccanismo di trasporto transvascolare delle NP.
Ulteriori informazioni: Qin Wang et al, Superare la barriera della membrana basale per migliorare la somministrazione nanoterapeutica ai tumori, Nature Nanotechnology (2023). DOI:10.1038/s41565-023-01498-w
Informazioni sul giornale: Nanotecnologia naturale
Fornito dall'Università della Scienza e della Tecnologia della Cina