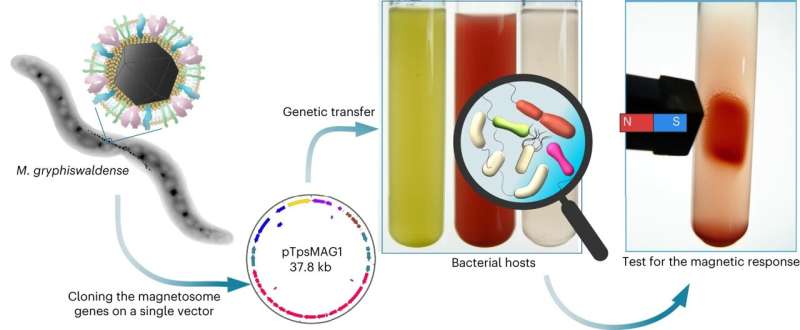
I batteri magnetici possiedono capacità straordinarie grazie alle nanoparticelle magnetiche, i magnetosomi, che sono concatenate all'interno delle loro cellule. Un gruppo di ricerca dell'Università di Bayreuth ha ora trasferito tutti i circa 30 geni responsabili della produzione di queste particelle a batteri non magnetici in un'ampia serie di esperimenti.
Ciò ha prodotto una serie di nuovi ceppi batterici che ora sono in grado di produrre magnetosomi. I risultati della ricerca presentati in Nature Nanotechnology sono rivoluzionari per la generazione di cellule viventi magnetizzate, che hanno un grande potenziale per lo sviluppo di metodi diagnostici e terapeutici innovativi in biomedicina.
Sulla base di studi approfonditi, i ricercatori hanno inizialmente identificato 25 specie di proteobatteri non magnetici – di gran lunga il dominio batterico più esteso – che sono particolarmente adatti per il trasferimento genico e per lo studio della formazione dei magnetosomi. Sia le proprietà biochimiche che la disponibilità di sequenze genetiche specifiche sono stati fattori decisivi.
La magnetizzazione ha avuto successo in sette specie:questi batteri producono continuamente magnetosomi in cui i cristalli di magnetite contenenti ferro sono concatenati insieme in un modo simile a quello del batterio donatore Magnetospirillum gryphiswaldense.
"In termini di future applicazioni in biomedicina, è particolarmente promettente il fatto che due specie di batteri che abbiamo ingegnerizzato geneticamente con successo siano già ampiamente utilizzate nella biotecnologia."
"Secondo lo stato attuale della ricerca, sono ben compatibili con le cellule umane. Ciò apre nuove prospettive per una varietà di applicazioni biomediche, ad esempio per il trasporto di principi attivi farmaceutici controllato da microrobot, per le tecniche di imaging magnetico o anche per ottimizzazioni della terapia antitumorale con ipertermia", afferma la prima autrice del nuovo studio, la dott.ssa Marina Dziuba, ricercatrice associata presso il gruppo di ricerca Microbiologia di Bayreuth.
I ricercatori di Bayreuth hanno studiato più in dettaglio i magnetosomi prodotti dai nuovi ceppi batterici transgenici e hanno così identificato una serie di fattori che potrebbero essere causalmente coinvolti nella formazione dei magnetosomi.
Anche il confronto tra il genoma di questi ceppi e il genoma di quei batteri geneticamente modificati che non sono riusciti a produrre magnetosomi ha portato a preziose informazioni. Esistono molte prove che suggeriscono che la formazione di magnetosomi di ceppi batterici transgenici è strettamente correlata alla loro capacità di fotosintetizzare o di impegnarsi nei cosiddetti processi di respirazione anaerobica indipendenti dall'ossigeno.
Nel complesso, il nuovo studio mostra che non è un singolo o alcuni geni particolari a mancare ai batteri transgenici quando non sono in grado di formare magnetosomi. Piuttosto, il fattore decisivo per sintetizzare i magnetosomi dopo aver ricevuto i cluster di geni estranei è una combinazione di alcune proprietà metaboliche e la capacità di utilizzare in modo efficiente le informazioni genetiche dei geni estranei per produrre proteine cellulari.
"Il nostro studio mostra che sono necessarie ulteriori ricerche per comprendere in dettaglio la biosintesi dei magnetosomi, identificare le barriere al loro trasferimento e sviluppare strategie per superarle. Allo stesso tempo, tuttavia, i nostri risultati gettano nuova luce sui processi metabolici che supportano la formazione dei magnetosomi Forniscono quindi un quadro per le indagini future sul modo di progettare nuovi ceppi di batteri magnetici biocompatibili su misura per innovazioni biomediche e biotecnologiche," spiega il Prof. Dr. Dirk Schüler, Cattedra di Microbiologia presso l'Università di Bayreuth.
In ricerche precedenti, il team di Bayreuth era già riuscito a introdurre i geni responsabili della formazione dei magnetosomi del batterio Magnetospirillum gryphiswaldense, un organismo modello per la ricerca, nel genoma dei batteri non magnetici. Tuttavia, solo in pochi casi, questo trasferimento genico ha prodotto batteri geneticamente modificati che, a loro volta, hanno iniziato a formare magnetosomi.
Non era del tutto chiaro quali fattori potessero influenzare la produzione di magnetosomi da parte dei batteri transgenici. In questo contesto, lo studio ora pubblicato, a cui ha partecipato anche un partner di ricerca dell'Università della Pannonia a Veszprém/Ungheria, fornisce un nuovo importante slancio per la magnetizzazione mirata delle cellule viventi.
Ulteriori informazioni: Dziuba, M.V., Müller, FD., Pósfai, M. et al. Esplorazione della gamma ospite per il trasferimento genetico della biosintesi degli organelli magnetici. Nanotecnologia naturale (2023). DOI:10.1038/s41565-023-01500-5 www.nature.com/articles/s41565-023-01500-5
Informazioni sul giornale: Nanotecnologia naturale
Fornito dall'Università di Bayreuth