I ricercatori della Yale University, New Haven, hanno ottimizzato un veicolo di mRNA a base di polimeri per la somministrazione mirata ai polmoni e hanno dimostrato il potenziale della piattaforma per la vaccinazione delle mucose contro gli agenti patogeni respiratori.
In un articolo, "Le nanoparticelle polimeriche forniscono mRNA al polmone per la vaccinazione delle mucose", pubblicato su Science Translational Medicine , il team presenta la creazione di RNA messaggero (mRNA) inalabile per uso terapeutico.
La ricerca clinica è alla ricerca di un modo efficiente e mirato per fornire mRNA ai polmoni per varie applicazioni terapeutiche, comprese le terapie sostitutive delle proteine, l’editing genetico e la vaccinazione. Le sfide principali sono state mantenere la stabilità dell'mRNA ed evitare l'interferenza immunitaria.
Il team di Yale ha creato formulazioni polimeriche PACE (Polymerized Albumin Conjugates for mRNA Encapsulation) per fornire mRNA locale ai polmoni. I ricercatori hanno ottimizzato i poliplex PACE per migliorare la protezione dell'mRNA, l'efficienza della trasfezione e la presentazione dell'antigene per strategie terapeutiche e di vaccinazione efficaci specifiche per i polmoni.
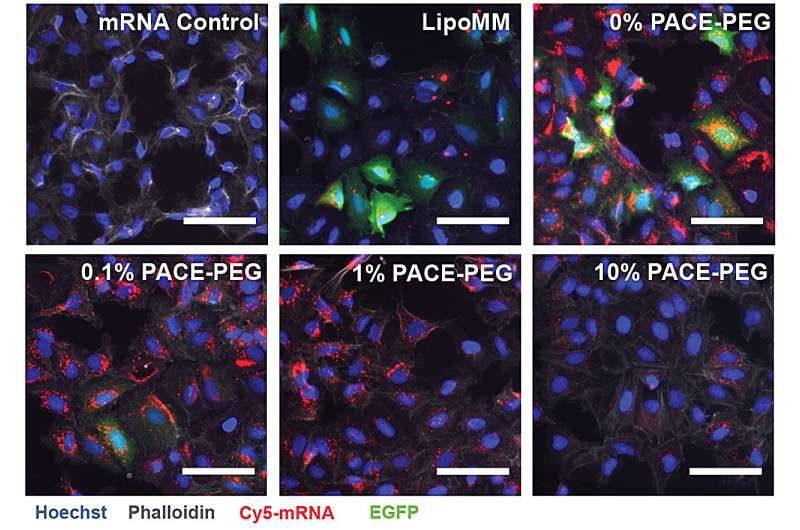
Per stabilizzare PACE, un rapporto ottimizzato di molecole di polietilenglicole (PEG) è stato integrato nella struttura polimerica durante il processo di copolimerizzazione enzimatica, che ha stabilizzato i poliplex e modificato le caratteristiche chiave. Il PEG è stato in grado di influenzare le dimensioni, la carica superficiale e altre proprietà dei poliplex, rendendoli più adatti al caricamento ed efficaci nel rilascio dell'mRNA alle cellule polmonari.
La formulazione stabilizzata ha avuto scarsi risultati in un esperimento di coltura cellulare in vitro. I ricercatori notano che i metodi tradizionali di coltura cellulare non sono buoni predittori dei sistemi di consegna, né positivamente né negativamente. L'ambiente all'interno del corpo, in particolare i polmoni, interagisce in modo molto diverso rispetto a un insieme di cellule. Ad esempio, mancano le superfici della mucosa e quelle superfici sono esattamente ciò di cui il sistema PACE-PEG è progettato per trarre vantaggio. Il vero test avverrebbe in vivo con un modello murino.
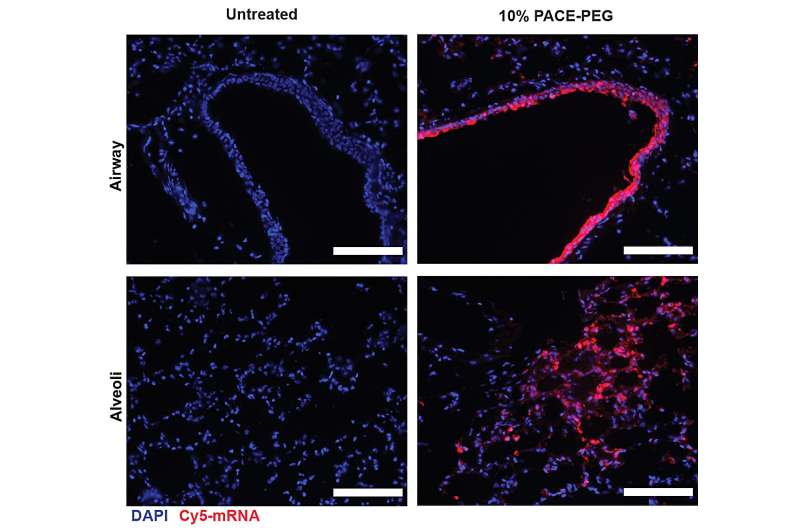
I ricercatori hanno incapsulato l’mRNA che codifica la proteina spike di SARS-CoV-2 nel PACE e hanno inoculato topi suscettibili all’infezione da SARS-CoV-2. I topi hanno ricevuto una dose di 10 μg di PACE-mRNA somministrata per via intranasale nei giorni 0 e 28. Lo sviluppo dell'immunità adattativa nei linfonodi mediastinici è stato testato e confermato 14 giorni dopo il boost.
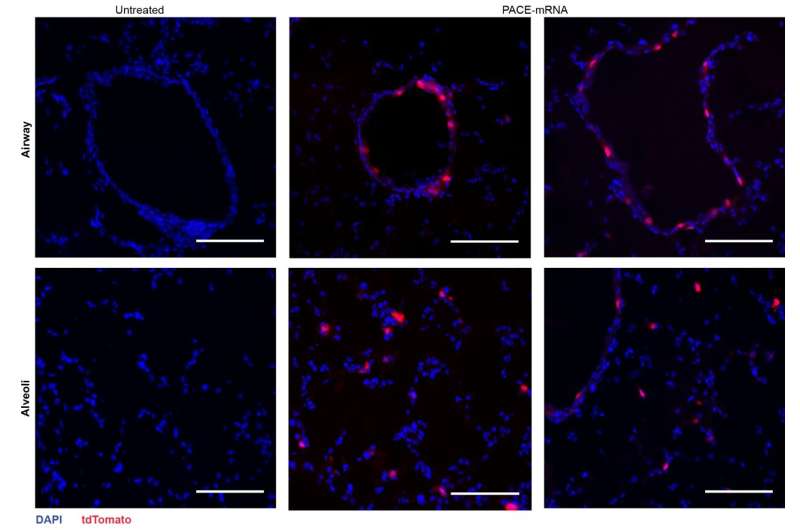
Dopo aver valutato la risposta immunitaria locale, i ricercatori hanno esaminato i tessuti polmonari, il siero del sangue e il liquido di lavaggio broncoalveolare per le risposte locali e sistemiche delle cellule T e degli anticorpi antigene-specifici. La trasfezione si è verificata principalmente nelle cellule epiteliali polmonari e nelle cellule presentanti l'antigene, due tipi di cellule che sono bersagli rilevanti per le malattie polmonari
La vaccinazione ha aumentato con successo il picco CD8 + specifico della proteina Cellule T nel tessuto polmonare e CD8 + circolanti Cellule T nel flusso sanguigno. CD8 + Le cellule T esprimevano marcatori indicativi della memoria residente nei tessuti. Sia gli anticorpi IgG circolanti che quelli della mucosa sono stati trovati a concentrazioni significativamente più elevate nei topi vaccinati.
Ai topi è stata quindi introdotta una dose letale di SARS-CoV-2. La vaccinazione PACE-mRNA ha ridotto significativamente la carica virale nei polmoni e ha migliorato il peso e la sopravvivenza dei topi vaccinati. Questa protezione è stata attribuita alla risposta immunitaria proteina-specifica indotta dalla vaccinazione.
Il gruppo di controllo non ha mostrato evidenza di una risposta immunitaria specifica per la proteina del picco e non ha mostrato una carica virale ridotta o un miglioramento della sopravvivenza dopo la sfida virale.
Lo studio presenta i poliplex PACE-mRNA come un metodo promettente per il rilascio efficiente e mirato di mRNA ai polmoni con potenziali benefici sia per l'espressione proteica terapeutica che per la vaccinazione della mucosa contro i patogeni respiratori.
Lo studio illustra anche l’importanza dei modelli animali rispetto alla sola coltura cellulare nel determinare gli effetti nel mondo reale. I risultati positivi indicano che sono necessarie ulteriori ricerche, con ulteriori test pianificati su modelli animali più grandi.
Ulteriori informazioni: Alexandra Suberi et al, Le nanoparticelle polimeriche forniscono mRNA al polmone per la vaccinazione delle mucose, Science Translational Medicine (2023). DOI:10.1126/scitranslmed.abq0603
Informazioni sul giornale: Scienza Medicina Traslazionale
© 2023 Rete Scienza X