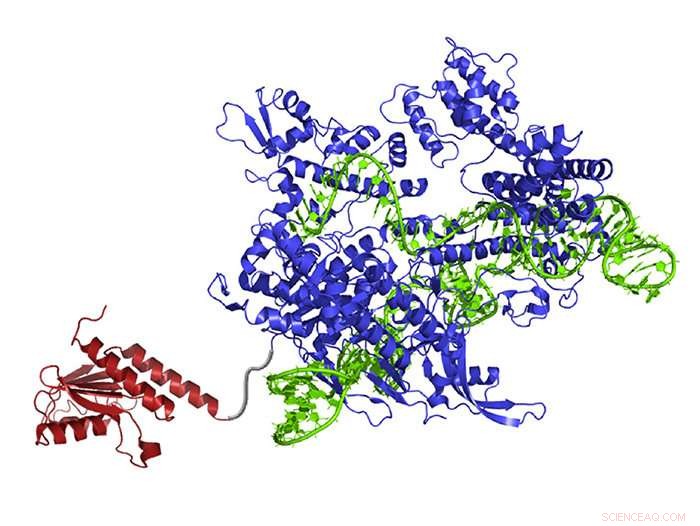
Un editor di base del DNA appena creato contiene un enzima che riorganizza gli atomi (rosso) che può trasformare l'adenina in inosina (letta e copiata come guanina), guida RNA (verde) che dirige la molecola nel punto giusto, e nickase Cas9 (blu), che taglia il filamento opposto di DNA e induce la cellula a scambiare la base complementare. Credito:Gaudelli et al./ Natura 2017
Scienziati dell'Università di Harvard e del Broad Institute del MIT e di Harvard hanno sviluppato una nuova classe di strumenti per l'editing del genoma. Questo nuovo "editor di base" può riparare direttamente il tipo di cambiamenti di una singola lettera nel genoma umano che rappresentano circa la metà delle mutazioni puntiformi associate alla malattia umana. Queste mutazioni sono associate a disturbi che vanno dalla cecità genetica all'anemia falciforme, ai disordini metabolici e alla fibrosi cistica.
Il gruppo di ricerca, guidato da David Liu, professore di chimica e biologia chimica all'Università di Harvard, membro principale dell'istituto presso il Broad Institute, e un investigatore dell'Howard Hughes Medical Institute (HHMI), sviluppato una macchina molecolare in grado di convertire la coppia di basi del DNA A*T in G*C, senza tagliare la doppia elica, con alta efficienza e praticamente nessun prodotto indesiderato. Lo sviluppo è un'importante aggiunta alla crescente suite di strumenti di modifica del genoma.
Il nuovo sistema è descritto in un articolo pubblicato oggi in Natura . Oltre a Liu, lo studio è stato condotto da Nicole Gaudelli, un borsista post-dottorato nel laboratorio di Liu; Alexis Komor, un ex borsista post-dottorato nel laboratorio di Liu che ora è assistente professore alla UCSD; studente laureato Holly Rees; ex studenti laureati Michael Packer e Ahmed Badran, e l'ex borsista post-dottorato David Bryson.
Il nuovo sistema, soprannominato Adenine Base Editor, o ABE, può essere programmato per colpire una specifica coppia di basi in un genoma utilizzando un RNA guida e una forma modificata di CRISPR-Cas9. Funziona riorganizzando gli atomi in un'adenina bersaglio (A) - una delle quattro basi che compongono il DNA - per assomigliare invece alla guanina (G), e poi indurre le cellule a fissare l'altro filamento di DNA per completare la conversione della coppia di basi, rendere permanente il cambiamento. Di conseguenza, quella che era una coppia di basi A*T diventa una coppia di basi G*C.
Non solo il sistema è molto efficiente rispetto ad altre tecniche di modifica del genoma per correggere le mutazioni puntiformi, ma non ci sono praticamente sottoprodotti rilevabili come inserimenti casuali, cancellazioni, traslocazioni, o altre conversioni da base a base.
Fare questo cambiamento specifico è importante perché circa la metà dei 32, 000 mutazioni puntiformi associate alla malattia già identificate dai ricercatori sono un cambiamento da G* C ad A* T.
"Abbiamo sviluppato un nuovo editor di base, una macchina molecolare, che in modo programmabile, irreversibile, efficiente, e modo pulito può correggere queste mutazioni nel genoma delle cellule viventi, " disse Liu, che è anche Richard Merkin Professor e Direttore del Merkin Institute of Transformative Technologies in Healthcare al Broad. "Quando mirato a determinati siti nel DNA genomico umano, questa conversione inverte la mutazione associata a una particolare malattia".
ABE si unisce ad altri sistemi di editing di base sperimentati nel laboratorio di Liu, come BE3 e la sua variante migliorata, BE4. Utilizzando questi editor di base, i ricercatori possono ora correggere tutte le cosiddette mutazioni di "transizione" da C a T, da T a C, da A a G, o da G ad A, che insieme rappresentano quasi i due terzi di tutte le mutazioni puntiformi che causano malattie, compresi molti che causano malattie gravi per le quali non esiste un trattamento attuale. Sono necessarie ulteriori ricerche, Liu osserva, per consentire all'ABE di colpire il più possibile il genoma, come Liu e i suoi studenti hanno precedentemente ottenuto attraverso varianti ingegneristiche di BE3.
Lo sviluppo del nuovo editor di base è iniziato quando il team ha iniziato uno sforzo di un anno per sviluppare un nuovo enzima in grado di convertire l'adenina in inosina (I), un nucleotide che si comporta in modo simile a G durante la sintesi del DNA o dell'RNA. Il progetto, guidato da Gaudelli, alla fine ha portato ad alte prestazioni, ABE di settima generazione.
"La sfida principale per me durante lo sviluppo dell'ABE è stata superare l'ostacolo psicologico legato al fatto che l'ABE potesse o meno passare dal concetto alla realtà, poiché la componente chiave dell'editor non esisteva naturalmente e doveva essere evoluta nel nostro laboratorio, ", ha detto Gaudelli. "Era importante mantenere la fede che non solo potevamo sognare una macchina così molecolare, ma anche costruirlo».
Per dimostrare il potenziale di ABE, Liu e colleghi hanno utilizzato per la prima volta l'ABE per correggere direttamente una mutazione che causa l'emocromatosi ereditaria (HHC) nelle cellule umane.
Hanno anche usato l'ABE per installare una mutazione nelle cellule umane che sopprime una malattia, ricreando la cosiddetta "mutazione britannica" riscontrata in individui sani che normalmente svilupperebbero malattie del sangue come l'anemia falciforme ma invece hanno una mutazione che fa sì che i geni dell'emoglobina fetale rimangano attivi dopo la nascita, proteggendoli dalle malattie del sangue.
Sebbene lo sviluppo di ABE sia un entusiasmante passo avanti nell'editing di base, rimane ancora del lavoro prima che l'editing di base possa essere utilizzato per curare i pazienti con malattie genetiche, compresi i test di sicurezza, efficacia, ed effetti collaterali.
"Creare una macchina in grado di apportare il cambiamento genetico necessario per curare una malattia è un importante passo avanti, ma è solo una parte di ciò che è necessario per curare un paziente, " ha detto Liu. "Dobbiamo ancora consegnare quella macchina, dobbiamo testarne la sicurezza, dobbiamo valutare i suoi effetti benefici negli animali e nei pazienti e valutarli rispetto a qualsiasi effetto collaterale:dobbiamo fare molte più cose".
"Ma avere la macchina è un buon inizio."