
Un tipo modificato della proteina Eos può essere reso fluorescente quando illuminato con luce laser blu e rossa. Sfondo:due proteine del citoscheletro in blu e rosso. La proteina visibile in rosso è stata etichettata con il nuovo tipo Eos modificato. (Montaggio:Mohr MA et al. Angewandte Chemie 2017. Copyright Wiley-VCH. Riprodotto con permesso)
Gli scienziati hanno identificato il meccanismo che consente alle proteine fluorescenti di cambiare colore in due fasi. Stanno quindi gettando le basi per nuove applicazioni in microscopia e analisi funzionali nella ricerca biologica.
Tutto è iniziato con un'osservazione che gli scienziati dell'ETH hanno fatto circa due anni fa con una speciale proteina fluorescente isolata dai coralli, Dendra 2, che diventa verde fluorescente. La luce può essere usata per cambiare la sua struttura molecolare in modo che cambi il suo colore in rosso. I ricercatori hanno scoperto un nuovo modo per indurre questo cambio di colore:in primo luogo, viene brevemente eccitato con un impulso di luce laser blu e quindi illuminato immediatamente con luce nel vicino infrarosso. Le applicazioni per questo interruttore di colore a due fasi includono la microscopia a fluorescenza.
Un team internazionale di ricercatori guidati da Periklis Pantazis, del Dipartimento di Scienze e Ingegneria dei Biosistemi (D-BSSE) dell'ETH di Zurigo a Basilea, ha ora spiegato questo meccanismo di cambio colore a due fasi. Gli scienziati si riferiscono a questo come "conversione innescata". La nuova conoscenza consente ai ricercatori di modificare altre proteine sensibili alla luce in modo che possano essere eccitate anche loro in due fasi.
I ricercatori del Politecnico di Zurigo, l'Istituto di tecnologia di Karlsruhe, e il Janelia Research Campus ad Ashburn, Virginia, ha esaminato da vicino le proteine attivate con luce blu ed è riuscito a dimostrare che queste proteine entrano in uno stato eccitato della durata di diversi millisecondi. "È relativamente lungo, " spiega Pantazis. "Gli altri fenomeni di fluorescenza sono molto più brevi".
Gli scienziati hanno anche dimostrato che questo stato è un caso di un fenomeno noto dalla chimica quantistica, uno "stato di tripletta". Dopo circa cinque millisecondi, la proteina fluorescente Dendra 2 ritorna al suo stato fondamentale. La conversione innescata avviene solo se la seconda fase, l'illuminazione con luce nel vicino infrarosso, si verifica all'interno della finestra temporale del tripletto.
Sequenze di amminoacidi modificate
La durata dello stato di tripletta dipende molto dalla stabilità della proteina fluorescente. Questo, a sua volta, dipende dall'esatta sequenza dei mattoni delle proteine (aminoacidi), ecco perché gli scienziati hanno modificato la sequenza di amminoacidi Dendra 2 in diversi punti. Quindi, hanno fatto lo stesso con un'altra proteina fluorescente, Eos. Fino ad ora, questa proteina non può essere eccitata in due fasi. È documentato nella letteratura scientifica che queste posizioni sono essenziali per lo stato di tripletta.
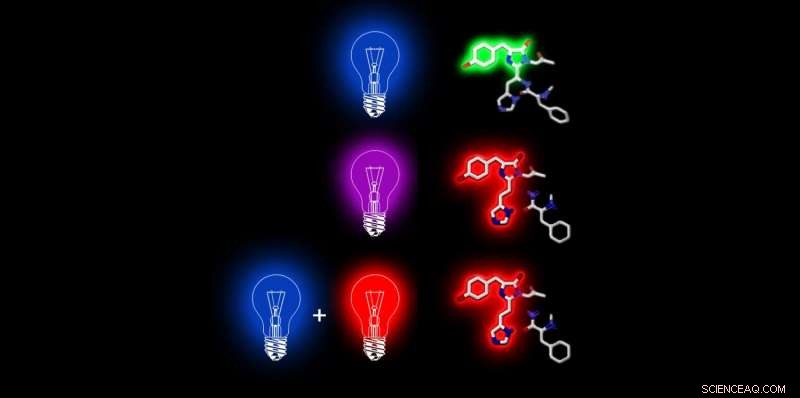
Quando Dendra 2 (a destra con il suo composto chimico fluorescente) è illuminato con luce laser blu, è verde fluorescente. Con luce viola, cambia la sua struttura chimica in modo che possa solo emettere fluorescenza rossa. Questo cambiamento della struttura chimica si verifica anche quando viene illuminato brevemente con il blu e subito dopo con la luce rossa (o con la luce laser blu e rossa contemporaneamente). Credito:ETH Zurigo
Gli scienziati hanno misurato la durata dello stato di tripletta con tutte le nuove proteine. Questo stato è stato esteso in modo significativo in molte delle proteine testate. Gli scienziati sono stati anche in grado di modificare la proteina Eos in modo che anch'essa potesse essere attivata in due fasi. Sono riusciti a farlo con altre sei proteine che non erano mai state attivate in due fasi prima. "Le proteine modificate non sono state solo rese commutabili in due fasi per la prima volta; sono anche più stabili e quindi emettono fluorescenza più intensamente, "dice Manuel Mohr, uno studente di dottorato nel gruppo di Pantazis e autore principale dello studio.
Gli scienziati hanno fatto la scoperta originale con un laser che non è convenzionalmente disponibile, che utilizza la luce nel vicino infrarosso. Oggi, però, gli scienziati hanno dimostrato che l'effetto può essere ottenuto anche utilizzando gli stessi laser rossi convenzionali che si trovano in ogni microscopio a fluorescenza. In altre parole, la conversione innescata è possibile con qualsiasi microscopio a fluorescenza.
La conversione innescata può essere utilizzata in microscopia per contrassegnare un punto strettamente definito in un campione di tessuto. Gli scienziati lo fanno puntando un raggio laser blu e rosso nel tessuto in modo che i raggi si incrocino in un unico punto. Primed conversion occurs only at this intersection. "Because neither blue nor red laser light have a toxic effect, the method is ideal for living organisms, " says Pantazis. Applications with other microscopy techniques may also be possible, including super-resolution microscopy, which has been around for several years now.
Brain mapping and gene sequencing
"We now know how to modify photoconvertible proteins to make them switch in two phases, " says Pantazis. The ETH scientists are working together with protein experts to modify other fluorescent proteins used in microscopy in the same way.
The researchers recently modified proteins so that they can be split off from a gene-activating messenger in a way that allows them to be light-activated with two colours. Per esempio, they could illuminate tissue with a blue and red beam intersecting at a single point, making it possible to activate specific genes in a single cell of the tissue. Proteins that detect calcium can be modified in this way, as well, and could potentially be used for 3-D brain mapping.
Biologists can ultimately use the new technique for other functional analyses in 3-D. ETH Zurich has already issued several licences for the patent, including to a start-up that plans to develop a DNA sequencing technique using a 3-D matrix.