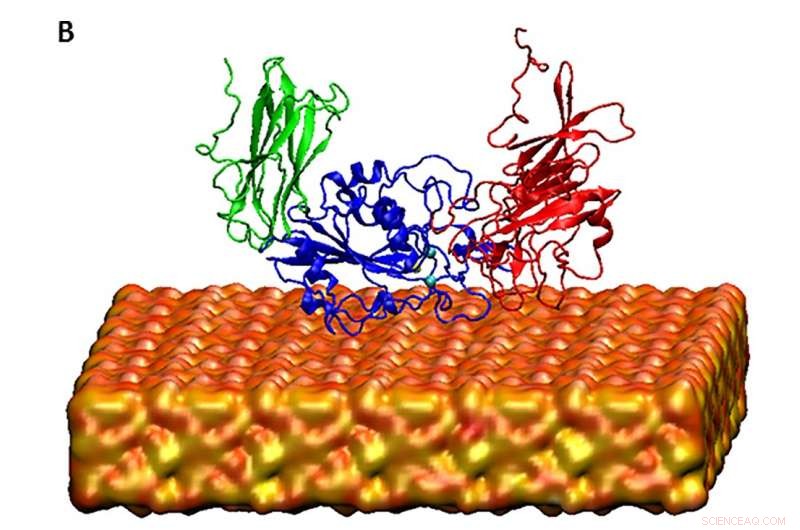
I supercomputer XSEDE Stampede presso TACC e Comet presso SDSC hanno aiutato gli autori dello studio a simulare il dominio del pezzo principale dell'integrina del recettore proteico della membrana cellulare in soluzione, basato su modelli di dinamica molecolare. Credito:Davoud Ebrahimi
Alcuni segreti per riparare i nostri scheletri potrebbero essere trovati nelle ragnatele setose dei ragni, secondo recenti esperimenti guidati da supercomputer. Gli scienziati coinvolti affermano che i loro risultati aiuteranno a comprendere i dettagli dell'osteorigenerazione, o come si rigenerano le ossa.
Uno studio ha scoperto che i geni potrebbero essere attivati nelle cellule staminali umane che avviano la biomineralizzazione, una tappa fondamentale nella formazione dell'osso. Gli scienziati hanno ottenuto questi risultati con la seta ingegnerizzata derivata dalla linea di trascinamento delle ragnatele dei tessitori di sfere dorate, che hanno combinato con la silice. Lo studio è apparso a settembre 2017 sulla rivista Materiali funzionali avanzati ed è stato il risultato dello sforzo congiunto di tre istituzioni:Tufts University, Massachusetts Institute of Technology e Nottingham Trent University.
Gli autori dello studio hanno utilizzato i supercomputer Stampede1 presso il Texas Advanced Computing Center (TACC) dell'Università del Texas ad Austin e Comet presso il San Diego Supercomputer Center (SDSC) dell'Università della California San Diego attraverso uno stanziamento di XSEDE, l'ambiente di scoperta della scienza e dell'ingegneria eXtreme, finanziato dalla National Science Foundation. I supercomputer hanno aiutato gli scienziati a modellare il modo in cui il recettore proteico della membrana cellulare chiamato integrina si ripiega e attiva i percorsi intracellulari che portano alla formazione dell'osso. La ricerca aiuterà i maggiori sforzi per curare le malattie della crescita ossea come l'osteoporosi o la malattia della valvola aortica calcifica.
"Questo lavoro dimostra un legame diretto tra biomateriali a base di seta-silice e percorsi intracellulari che portano all'osteogenesi, ", ha affermato la coautrice dello studio Zaira Martín-Moldes, borsista post-dottorato presso il Kaplan Lab della Tufts University. Ricerca lo sviluppo di nuovi biomateriali a base di seta. "Il materiale ibrido ha promosso la differenziazione delle cellule staminali mesenchimali umane, le cellule progenitrici del midollo osseo, agli osteoblasti come indicatore di osteogenesi, o formazione di tessuto simile all'osso, ", ha detto Martín-Moldes.
"La seta ha dimostrato di essere un'impalcatura adatta per la rigenerazione dei tessuti, grazie alle sue eccezionali proprietà meccaniche, " Ha spiegato Martín-Moldes. È biodegradabile. È biocompatibile. Ed è sintonizzabile tramite modifiche di bioingegneria. Il team sperimentale della Tufts University ha modificato la sequenza genetica della seta dai ragni tessitori di sfere d'oro (Nephila clavipes) e ha fuso il peptide promotore della silice R5 derivato da un gene della diatomea Cylindrotheca fusiformis silaffin.
Lo studio sulla formazione ossea mirava alla biomineralizzazione, un processo critico nella biologia dei materiali. "Ci piacerebbe generare un modello che ci aiuti a prevedere e modulare queste risposte sia in termini di prevenzione della mineralizzazione che di promozione, ", ha detto Martín-Moldes.
"Simulazioni di supercalcolo ad alte prestazioni sono utilizzate insieme ad approcci sperimentali per sviluppare un modello per l'attivazione dell'integrina, che è il primo passo nel processo di formazione dell'osso, ", ha affermato il coautore dello studio Davoud Ebrahimi, un associato post-dottorato presso il Laboratorio di Meccanica Atomistica e Molecolare del Massachusetts Institute of Technology.
L'integrina si inserisce nella membrana cellulare e media i segnali tra l'interno e l'esterno delle cellule. Nel suo stato dormiente, l'unità principale che sporge dalla membrana è piegata come una traversina che annuisce. Questo stato inattivo impedisce l'adesione cellulare. Nel suo stato attivato, l'unità principale si raddrizza ed è disponibile per il legame chimico nella regione del ligando esposta.
"Il campionamento di diversi stati della conformazione delle integrine a contatto con superfici silicizzate o non silicizzate potrebbe prevedere l'attivazione del percorso, " Ha spiegato Ebrahimi. Il campionamento del ripiegamento delle proteine rimane un problema classico dal punto di vista computazionale, nonostante i recenti e grandi sforzi nello sviluppo di nuovi algoritmi.
La chimera derivata da seta e silice che hanno studiato pesava circa 40 kilodalton. "In questa ricerca, cosa abbiamo fatto per ridurre i costi di calcolo, abbiamo solo modellato la parte principale della proteina, che è entrare in contatto con la superficie che stiamo modellando, " disse Ebrahimi. "Ma ancora una volta, è un grande sistema da simulare e non può essere eseguito su un sistema ordinario o su computer ordinari."
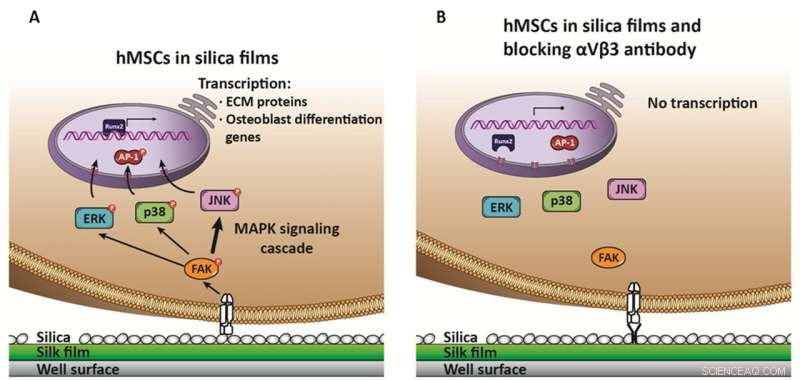
Meccanismo proposto per l'induzione dell'osteogenesi delle hMSC su superfici di silice. Il legame dell'integrina αVβ3 alla superficie della silice ne favorisce l'attivazione, che innesca una cascata di attivazione che coinvolge i tre percorsi MAPK, ERK, p38, ma principalmente JNK (riflesso come freccia più ampia), che promuove l'attivazione e la traslocazione di AP-1 nel nucleo per attivare il fattore di trascrizione Runx2. Runx2 è l'ultimo responsabile dell'induzione delle proteine della matrice extracellulare ossea e di altri geni di differenziazione degli osteoblasti. B) In presenza di un anticorpo neutralizzante contro αVβ3, non c'è attivazione e induzione di cascate MAPK, quindi nessuna induzione di geni della matrice extracellulare ossea e quindi, nessuna differenziazione. Credito:Davoud Ebrahimi
Il team computazionale del MIT ha utilizzato il pacchetto di dinamica molecolare chiamato Gromacs, un software per la simulazione chimica disponibile su entrambi i sistemi di supercalcolo Stampede1 e Comet. "Potremmo eseguire queste grandi simulazioni avendo accesso ai cluster computazionali XSEDE, " Egli ha detto.
"Ho un'esperienza positiva di lunga data nell'utilizzo delle risorse XSEDE, " ha detto Ebrahimi. "Li uso ormai da quasi 10 anni per i miei progetti durante le mie esperienze di laurea e post-dottorato. E lo staff di XSEDE è davvero utile in caso di problemi. Se hai bisogno di un software che dovrebbe essere installato e non è disponibile, ti aiutano e ti guidano attraverso il processo di ricerca. Ricordo di aver scambiato molte e-mail la prima volta che stavo cercando di utilizzare i cluster, e non ero così familiare. Ho ricevuto molto aiuto dalle risorse XSEDE e dalle persone di XSEDE. Apprezzo molto il tempo e lo sforzo che mettono per risolvere i problemi computazionali che di solito incontriamo durante la nostra simulazione, "Ebrahimi rifletté.
Il calcolo combinato con la sperimentazione ha aiutato a far avanzare il lavoro nello sviluppo di un modello di osteorigenerazione. "Proponiamo un meccanismo nel nostro lavoro, " ha spiegato Martín-Moldes, "che inizia con la superficie della seta di silice che attiva uno specifico recettore proteico della membrana cellulare, in questo caso integrina αVβ3." Ha detto che questa attivazione innesca una cascata nella cellula attraverso tre percorsi della proteina kinasi attivata da mitogeni (MAPK), il principale è la cascata della chinasi N-terminale c-Jun (JNK).
Ha aggiunto che anche altri fattori sono coinvolti in questo processo come Runx2, il principale fattore di trascrizione correlato all'osteogenesi. Secondo lo studio, il sistema di controllo non ha mostrato alcuna risposta, e nemmeno il blocco dell'integrina usando un anticorpo, confermando il suo coinvolgimento in questo processo. "Un altro risultato importante è stata la correlazione tra la quantità di silice depositata nel film e il livello di induzione dei geni che abbiamo analizzato, " Martín-Moldes ha detto. "Questi fattori forniscono anche una caratteristica importante da controllare nella futura progettazione dei materiali per i biomateriali che formano l'osso".
"Stiamo facendo una ricerca di base qui con i nostri sistemi di seta-silice, " Martín-Moldes ha spiegato. "Ma stiamo aiutando a costruire il percorso per generare biomateriali che potrebbero essere utilizzati in futuro. La mineralizzazione è un processo critico. L'obiettivo finale è sviluppare questi modelli che aiutino a progettare i biomateriali per ottimizzare il processo di rigenerazione ossea, quando l'osso è necessario per rigenerarsi o per ridurlo al minimo quando abbiamo bisogno di ridurre la formazione ossea."
Questi risultati aiutano a far progredire la ricerca e sono utili in sforzi più ampi per aiutare a curare e curare le malattie ossee. "Potremmo aiutare a curare le malattie legate alla formazione ossea, come malattia della valvola aortica calcifica o osteoporosi, di cui abbiamo bisogno per conoscere il percorso per controllare la quantità di osso formato, per ridurlo o aumentarlo, disse Ebrahimi.