Il trasferimento di idruro è una reazione importante per la chimica (ad es. celle a combustibile), così come la biologia (ad es. catena respiratoria e fotosintesi). Spesso, una reazione parziale comporta il trasferimento di uno ione idruro (H-). Ma questo trasferimento di idruri comporta un passaggio o più passaggi singoli? Nel diario Angewandte Chemie , gli scienziati hanno ora fornito la prima prova del trasferimento graduale dell'idruro in un sistema biologico.
Un passo importante nella biosintesi della clorofilla è l'idrogenazione dipendente dalla luce della protoclorofilla a clorofilla. Ciò comporta la riduzione di un doppio legame tra gli atomi di carbonio 17 e 18 in questo complesso sistema ad anello in un singolo legame poiché entrambi gli atomi di carbonio si legano a un atomo di idrogeno aggiuntivo. Questo passaggio è catalizzato dall'enzima protoclorofillide ossireduttasi e richiede l'irradiazione con la luce. Parlando tecnicamente, però, questa reazione non aggiunge un atomo di idrogeno a ciascun carbonio. Anziché, c'è la prima aggiunta di uno ione idruro (H–) a C 17 e poi aggiunta di un protone (H+) a C 18 . La prima reazione parziale, il trasferimento dell'idruro, richiede il cofattore nicotinammide adenina dinucleotide fosfato (NADPH). Il NADPH funge da sorgente per due elettroni e un protone (H+), l'equivalente di un anione idruro, H-.
Le reazioni di trasferimento dell'idruro giocano un ruolo chiave in molti sistemi biologici. Però, il loro meccanismo è ancora controverso. Eseguire i tre passaggi elementari:trasferimento di un elettrone, un protone, e un altro elettrone dal NADPH al substrato, si verificano simultaneamente, o per gradi?
A causa della breve durata degli intermedi, la prova diretta di un meccanismo graduale non era in precedenza possibile. Le reazioni dipendenti dalla luce, come l'idrogenazione che si verifica nella biosintesi della clorofilla, che può essere innescata da un breve impulso laser hanno risolto questo problema. Utilizzando la spettroscopia di assorbimento ed emissione risolta nel tempo, i ricercatori che lavorano con Roger J. Kutta e Nigel S. Scrutton presso l'Università di Manchester (Regno Unito) sono stati in grado di caratterizzare il meccanismo di questo trasferimento di idruro.
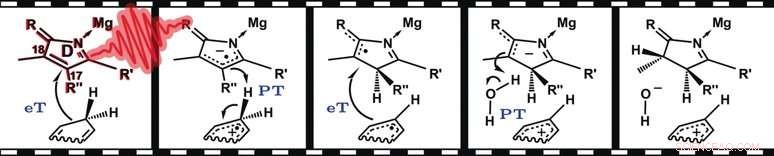
Oltre agli stati eccitati di protoclorofillide, i ricercatori sono stati in grado di risolvere tre intermedi discreti che sono coerenti con un meccanismo parzialmente graduale:un trasferimento iniziale di elettroni da NADPH a protoclorofillide che è stato eccitato (allo stato singoletto) dalla luce è seguito dal trasferimento accoppiato di un protone e un elettrone . Come previsto, il passo finale è il trasferimento del secondo protone.
interessante, i ricercatori hanno trovato diversi intermedi per il tipo selvaggio dell'enzima e una versione mutata (C 226 S):Mentre l'idruro iniziale si lega a C 17 nel tipo selvatico, viene trasferito a C 18 nella versione mutante. Però, il risultato finale è lo stesso stereoisomero della clorofilla.
Le intuizioni ottenute da questi esperimenti forniscono una comprensione più profonda di come l'energia luminosa può essere utilizzata per reazioni chimiche che coinvolgono il trasferimento di idrogeno, in particolare per quanto riguarda la progettazione di catalizzatori fotoattivati.