Credito:Rice University
Gli scienziati della Rice University che affermano che i sensori biologici non sono abbastanza sensibili stanno facendo qualcosa al riguardo.
Il laboratorio del biologo sintetico Jeffrey Tabor ha introdotto una nuova tecnica per aumentare o diminuire la sensibilità dei sistemi a due componenti, una classe di proteine che i batteri usano per percepire un'ampia varietà di stimoli.
La tecnica potrebbe consentire l'ingegnerizzazione di biosensori su misura per batteri intestinali diagnostici, rilevamento di inquinanti ambientali o controllo automatizzato dei livelli di nutrienti nel suolo.
Sensori a due componenti, il focus di un nuovo documento che descrive il lavoro in Nature Communications, sono una vasta famiglia di sensori codificati geneticamente che i batteri utilizzano per rilevare un input specifico e attivare un gene specifico in risposta ai cambiamenti nel loro ambiente.
Sebbene questi sensori siano noti da tre decenni, non erano abbastanza sensibili per Tabor. Lui e l'allievo di Rice e l'autore principale Brian Landry hanno deciso di ridurre la quantità di input necessaria per attivarli.
Combinando modellazione al computer ed esperimenti, hanno ottenuto proprio questo. Nella carta, descrivono la loro scoperta che l'attività della fosfatasi, che è essenziale per la regolazione e la segnalazione nelle cellule, può avere un effetto drammatico sulle soglie di rilevamento dei sistemi a due componenti.
Precedenti ricerche avevano dimostrato che le mutazioni del primo componente, una proteina sensore di segnalazione nota come istidina chinasi, può essere utilizzato per controllare l'entità della fosforilazione del secondo componente, una proteina regolatrice della risposta. Ma nessuno aveva suggerito che le mutazioni della fosfatasi potessero essere usate per alterare la sensibilità di questi percorsi per i loro input, ha detto Tabor.
Un giorno, di fronte a un sensore di nitrati che non si accendeva come previsto nell'intestino di un topo malato, Landry ha ipotizzato che le mutazioni della fosfatasi potrebbero aumentare notevolmente la sensibilità del percorso.
Ha prima convalidato l'ipotesi utilizzando un modello matematico e poi ha condotto esperimenti che hanno mostrato che le mutazioni aumentavano l'efficienza di un sensore di nitrati di un fattore 100. Il laboratorio di Tabor ha continuato a convalidare l'approccio in sistemi a due componenti che rilevano un'ampia varietà di input , anche in specie batteriche molto diverse.
Landry ha lavorato con un altro studente di bioingegneria della Rice, co-autore Lucas Hartsough, per identificare un amminoacido "hot spot" presente nel 64 percento di tutte le istidina chinasi del sensore che possono essere mutate per regolare la sensibilità. Hanno convalidato l'approccio in due percorsi minimamente caratterizzati, che ha suggerito che può essere ampiamente applicato, ha detto Tabor.
Landry ha anche utilizzato la tecnologia per progettare un batterio del suolo, Bacillus subtilis, rilevare e rispondere a un'ampia gamma di concentrazioni di nitrati (fertilizzanti) nel suolo. Tabor e Landry suggeriscono che questo sistema potrebbe essere abbinato a percorsi in fase di sviluppo da un collega del MIT, biologo sintetico Chris Voigt, e il suo laboratorio per progettare i batteri del suolo che mantengono livelli di azoto ottimali nel suolo senza la necessità di fertilizzanti.
I sistemi a due componenti possono essere attivati da molti tipi di input, compresi i gas, molecole di eme nel sangue, zuccheri, polisaccaridi intestinali, ormoni umani o vegetali o anche la luce.
"Ecco perché siamo così entusiasti di questo, "Ha detto Tabor. "Questi sensori funzionano tutti allo stesso modo. Hanno tutti la fosfatasi e la chinasi. Abbiamo identificato più di 25, 000 di loro nei genomi batterici e pensiamo che la nostra strategia funzionerà sulla maggior parte di essi".
Ha detto che la tecnica del suo laboratorio si basa sulla via di segnalazione attraverso la quale le molecole sensoriali naturali dicono alle cellule di fermarsi, avviare o modificare la produzione di proteine. La messa a punto dei sensori naturali per le applicazioni sintetiche è stata finora difficile, Egli ha detto.
"Uno dei grandi limiti è che quando prendi un biosensore dalla natura, potrebbe rilevare la sostanza chimica che ti interessa, ma non alla giusta concentrazione. Questo perché si è evoluto per consentire a un batterio di sopravvivere meglio in un ambiente naturale piuttosto che per soddisfare le esigenze ingegneristiche di un biologo sintetico, " Egli ha detto.
"Chiamiamo questo livello la soglia di rilevamento del sensore, e non ci sono state molte buone tecnologie per mettere a punto quella soglia per soddisfare le nostre esigenze ingegneristiche, " Tabor ha detto. "Questa è stata una delle principali limitazioni nella progettazione dei biosensori. Ma ora, abbiamo trovato un trucco generale che ci permette di calibrare le soglie di rilevamento di questa famiglia di sensori batterici in modo molto razionale, e funziona abbastanza bene."
Nelle sue simulazioni ed esperimenti, il laboratorio ha mutato la proteina istidina chinasi, che rileva un input e rilascia un gruppo fosfato che si lega al regolatore di risposta. Quella, a sua volta, si lega al DNA per attivare l'espressione genica.
"Quando accendi l'espressione genica, questo è il tuo segnale, " ha detto Tabor. "La cosa bella di questi percorsi è che quando l'input è assente, il sensore istidina chinasi agisce invece come fosfatasi e rimuove il gruppo fosfato. Quando ciò accade, il regolatore della risposta cade dal DNA e non attiva più l'espressione genica".
Ha detto che la mutazione della chinasi dell'istidina per favorire l'attivazione o la disattivazione del segnale può essere utilizzata per controllare le azioni dei regolatori di risposta, e quindi la quantità di proteine desiderate prodotte.
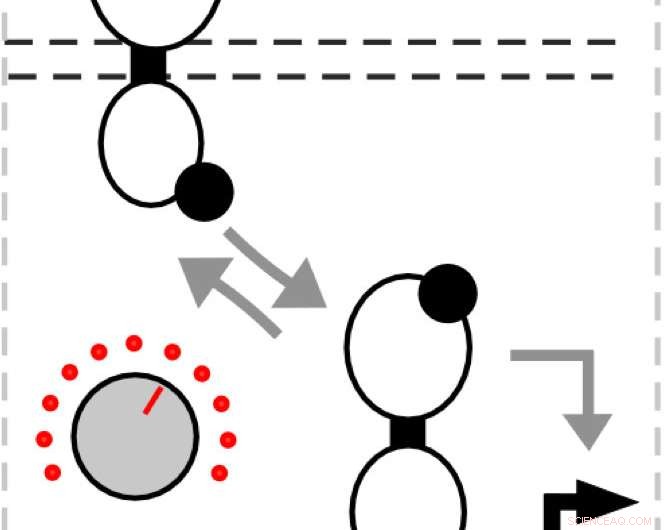
"Abbiamo pensato che fosse come un tiro alla fune tra l'attività della chinasi e l'attività della fosfatasi, " ha detto Tabor. "Quel bilanciamento determina quanto input è necessario per accendere il sensore. Quindi questo è come una manopola in cui possiamo rendere l'attività della fosfatasi più forte o più debole per regolare l'input".
Ha detto che la generalità del processo dovrebbe dare impulso alla biologia sintetica in generale. "Esistono metodi alternativi per fare ciò che abbiamo fatto qui, ma sono molto più laboriosi, " disse Tabor. "È più probabile che falliscano, e prenderebbero un intero dottorato di ricerca. per farli lavorare, mentre possiamo farlo in una settimana e farlo funzionare".