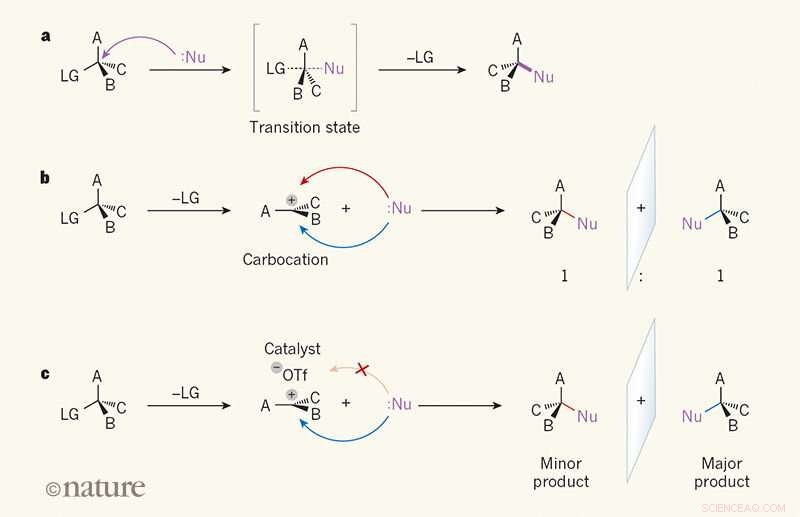
Selettività speculare nelle reazioni di sostituzione. un, In una reazione SN2, un reagente chiamato nucleofilo (Nu; i punti indicano una coppia solitaria di elettroni) attacca un atomo di carbonio in una molecola organica dal lato opposto a un gruppo "in uscita" (LG). UN, B e C possono essere qualsiasi atomo o gruppo. Nello stato di transizione, il legame tra l'atomo di carbonio e l'LG è parzialmente rotto, e un legame tra Nu e l'atomo di carbonio è parzialmente formato (i legami parzialmente rotti e parzialmente formati sono mostrati come linee tratteggiate). Il legame con l'LG poi si rompe, e si forma un unico prodotto. B, Nella reazione SN1, l'LG viene rilasciato per primo, e un planare, intermedio carico chiamato forme di carbocatione. Poiché il Nu può attaccare il carbocatione con la stessa facilità da entrambi i lati, il prodotto si forma come un rapporto 1:1 di isomeri speculari (enantiomeri). C, Wendlandt et al.1 riportano una reazione SN1 in cui un catalizzatore a piccola molecola e uno ione triflato (–OTf) si legano a un lato del carbocatione, dirigere il nucleofilo dall'altra parte. Viene quindi prodotto preferibilmente un enantiomero. Credito: Natura (2018). DOI:10.1038/s41586-018-0042-1
Un team di ricercatori dell'Università di Harvard negli Stati Uniti ha sviluppato un modo per creare una reazione SN1 per creare stereocentri di carbonio quaternario. Nel loro articolo pubblicato sulla rivista Natura , il team descrive il superamento della tendenza delle reazioni SN1 a distruggere la stereochimica per creare il materiale centrato sul carbonio. Tobias Morack e Ryan Gilmour dell'Università di Münster in Germania, offrire un pezzo di News &Views sullo studio nello stesso numero della rivista.
Come notano i ricercatori, fino ad ora, non esiste un buon metodo per creare stereocentri quaternari. Metodi attuali, notano, tendono ad essere basati su substrati pro-chirali, che sono essi stessi una sfida da fare. In questo nuovo sforzo, il team di Harvard ha escogitato un nuovo approccio, uno basato sulla reazione SN1.
Le reazioni SN1 sono un pilastro dei corsi introduttivi di chimica organica, ma notoriamente causano il caos con la stereochimica. Nonostante ciò, i ricercatori credevano di poter utilizzare l'intermedio carbocationico piatto prodotto in tali reazioni come substrato. A quello scopo, hanno ottenuto una reazione SN1 che ha convertito una miscela di acetato di propargil (con quantità uguali di enantiomeri sinistri e destrorsi, un racemo) in una miscela con un centro quaternario. Un donatore di legami idrogeno è stato utilizzato come catalizzatore per rimuovere i materiali acetossi che sono stati sostituiti con una miscela allilica:il risultato è stato un singolo enantiomero.
I prodotti finali erano interessanti, Nota Morack e Gilmour, perché gli stereocentri del carbonio avevano una vasta gamma di orbitali elettronici. Ciò significa che hanno geometrie fisiche diverse e quindi reagiscono in modo diverso. Questo apre le porte al loro utilizzo per produrre un'ampia varietà di molecole che potrebbero essere utilizzate in varie reazioni per sintetizzare nuove sostanze chimiche.
I ricercatori fanno notare che non hanno finito con il lavoro:hanno in programma di provare lo stesso approccio con composti che non sono altrettanto stabili. Così facendo, riconoscono, richiederà l'uso di un catalizzatore ancora più reattivo. Hanno anche in programma di esaminare la conduzione della reazione con diversi nucleofili.
© 2018 Phys.org