Credito:Wiley
Una combinazione di microtubuli naturali e recettori macrociclici sintetici consente il controllo della luce, aggregazione reversibile dei microtubuli in nanostrutture più grandi. Come gli scienziati cinesi hanno riportato sulla rivista Angewandte Chemie , quando in un ambiente cellulare questi microtubuli aggregati possono anche cambiare la morfologia cellulare, provocando la morte cellulare. I ricercatori sperano di saperne di più sulle malattie causate dall'aggregazione impropria delle proteine.
In natura, l'aggregazione di molecole in sovrastrutture gioca un ruolo importante. I microtubuli dinamici sono filamenti proteici che si combinano con altri componenti per formare i citoscheletri delle nostre cellule. Durante il ciclo cellulare, i microtubuli si assemblano e si smontano costantemente. Scienziati della Nankai University e del Collaborative Innovation Center of Chemical Science and Engineering (Tianjin, China) concepì l'idea di combinare i microtubuli in aggregati supramolecolari più grandi usando "recettori" sintetici. In questo modo speravano di produrre biomateriali innovativi e acquisire nuove conoscenze sui processi di aggregazione biologica.
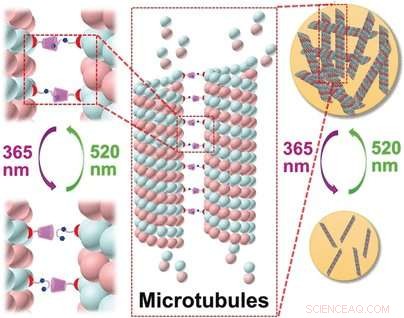
Per attaccare i recettori sintetici ai microtubuli, il team che lavora con Yu Liu ha scelto un farmaco antitumorale chiamato paclitaxel. Questa molecola si lega ai microtubuli e blocca la decostruzione del citoscheletro, fermare la divisione cellulare e causare la morte cellulare. Come recettore, i ricercatori hanno scelto una grande molecola a forma di coppa della famiglia delle ciclodestrine. Queste molecole macrocicliche possono incorporare altre molecole come "ospiti" nelle loro grandi cavità. In questo caso l'ospite è un arilazopirazolo (AAP), una molecola con due anelli aromatici collegati da un doppio legame azoto-azoto. La molecola può assumere una delle due forme:una forma cis piegata e una forma trans diritta. Solo la versione diritta si inserisce nella "tazza" della ciclodestrina. Il trucco intelligente qui è che, utilizzando la luce di due diverse lunghezze d'onda, l'AAP può essere commutato avanti e indietro tra le sue due forme a piacimento.
I ricercatori hanno utilizzato paclitaxel come connettore per collegare "coppe" e i loro "ospiti" ai microtubuli. L'irradiazione con luce visibile e UV commuta i microtubuli tra una forma aggregata e non aggregata, rispettivamente, come dimostrato dall'esame spettroscopico e microscopico. Gli aggregati assumono un'ampia gamma di variazioni morfologiche, che vanno dalle nanofibre ai nanonastri e alle nanoparticelle di diverse dimensioni.
È particolarmente interessante che l'aggregazione dei microtubuli possa essere innescata anche all'interno delle cellule. Questo fa sì che le cellule si rimpiccioliscano e muoiano, che dimostra che l'effetto citotossico del paclitaxel può essere aumentato significativamente.
I ricercatori sperano che il loro approccio aumenterà la nostra comprensione dei processi coinvolti nel nanoassemblaggio proteico fisiologico e patologico, e potrebbe creare nuove prospettive nel trattamento delle malattie causate dall'aggregazione impropria delle proteine.