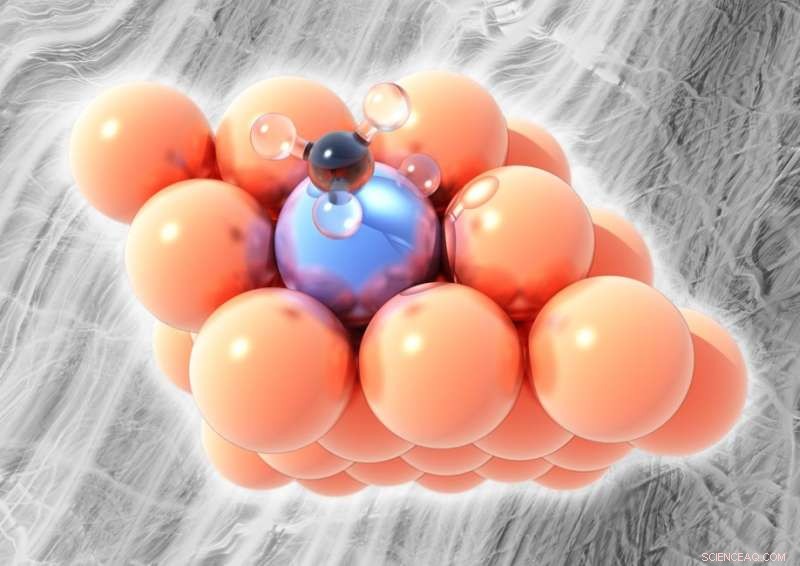
Nella foto, la lega di platino-rame a singolo atomo. Il rame (arancione) non è in grado di rompere i legami tra carbonio (nero) e idrogeno (trasparente) nei derivati del metano se non a temperature più elevate, ma un singolo atomo di platino (blu ghiaccio) nello strato superficiale della lega può rompere atomi di idrogeno a temperature relativamente basse senza formare coke. Credito:Michail Stamatakis, UCL
I progressi tecnologici nella stimolazione dei pozzi di petrolio e gas nell'ultimo decennio consentono ora la produzione di gas naturale dal gas di scisto intrappolato nelle formazioni rocciose sotterranee. Con l'improvviso aumento della disponibilità di gas di scisto, gli scienziati hanno riacquistato interesse per l'attivazione del carbonio-idrogeno (C–H), il processo di rottura dei legami C–H da gas come il metano per formare catene di idrocarburi che possono essere utilizzati come combustibile.
Ma gli scienziati sono molto lontani dal ricavare questi combustibili dal gas di scisto:la maggior parte dei catalizzatori per l'attivazione del C–H rompono troppi atomi di idrogeno, lasciando dietro di sé un solido carbonio indesiderato chiamato coke.
Desiderando una lega metallica che funga da catalizzatore per l'attivazione di C–H pur rimanendo resistente al coke, un team guidato da Charles Sykes della Tufts University ha concepito una lega composta dal platino metallico reattivo e dal rame metallico inerte. In una serie di esperimenti di laboratorio, La squadra di Sykes ha esaminato il rame puro, platino puro, e una lega a singolo atomo di platino-rame (SAA) per determinare le interazioni di ciascun materiale con gli idrocarburi derivati dal metano, molecole che si trovano naturalmente nel gas di scisto. Il team ha scoperto che il SAA platino-rame era resistente alla coke.
A seguito di questa scoperta, il gruppo Multiscale Computational Catalysis &Materials Science guidato da Michail Stamatakis presso l'University College di Londra ha utilizzato le risorse di calcolo ad alte prestazioni (HPC) presso l'Oak Ridge Leadership Computing Facility (OLCF) per smascherare i dettagli degli esperimenti tramite simulazioni. Matteo Darby, un post-dottorato all'epoca e ora destinatario del premio di dottorato del Consiglio di ricerca in ingegneria e scienze fisiche del Regno Unito che lavora nel gruppo Stamatakis, ha eseguito i calcoli per il progetto.
Darby ha scoperto che a basse temperature, il platino rimuove rapidamente gli idrogeni dal metano, portando alla formazione di depositi di carbonio; il rame non è in grado di rompere i legami C–H se non ad alte temperature. La lega platino-rame del team, però, è stato scoperto che rompe efficacemente i legami C–H a temperature intermedie senza formare coke. Come puro rame, la lega era anche in grado di formare catene di metano a due e tre molecole, e poteva raggiungere questo obiettivo a una temperatura di oltre 100 gradi Celsius più fredda di quella richiesta dal rame.
"Questi calcoli sono molto costosi dal punto di vista computazionale. Per alcuni, se li hai eseguiti sul tuo laptop, potrebbero volerci diversi mesi per eseguire un calcolo, "Darby ha detto. "All'OLCF, possono volerci forse un giorno o due perché hai centinaia di core con cui lavorare."
Potenti supercomputer dell'OLCF, una struttura per gli utenti dell'Office of Science del Dipartimento dell'Energia degli Stati Uniti (DOE) situata presso l'Oak Ridge National Laboratory del DOE, risolvere complessi problemi scientifici nel campo dell'energia, materiali, chimica, e molti altri domini scientifici. I risultati delle simulazioni del team spiegano le reazioni del platino e del rame con il metano e offrono un nuovo catalizzatore resistente al coke.
Armato di questa nuova conoscenza, gli sperimentatori di Tufts hanno creato una replica a microlivello delle prestazioni di un vero impianto chimico per ottenere ancora più informazioni sul processo. Il progetto dimostra che la teoria può essere utilizzata per perfezionare gli esperimenti fornendo una comprensione fondamentale, ponendo le basi per un lavoro sperimentale su larga scala.
Un problema di coke
I combustibili comuni che esistono come catene di molecole di idrocarburi includono propano, spesso utilizzato nei forni per il calore, e butano, il liquido che si trova nella maggior parte degli accendini. Usando l'attivazione C–H, gli scienziati possono avviare le reazioni all'interno del più semplice idrocarburo, il metano, e quindi incoraggiare queste molecole a legarsi tra loro per formare combustibili utili. Poiché le formazioni di scisto sono abbondanti e fonti di idrocarburi più lunghi (ad es. petrolio greggio) si stanno esaurendo, gli scienziati stanno cercando modi per convertire cataliticamente il metano in questi combustibili.
I metalli di transizione come platino e nichel sono catalizzatori efficaci, ma causano anche la formazione di grandi quantità di depositi di coke ostruttivi. Questo strato di carbonio ricopre la parte superiore del metallo, rendendo le restanti molecole di metano incapaci di reagire con il resto del materiale metallico.
"La coca è un grosso problema nella chimica industriale, "Darby ha detto. "Una volta depositato, devi togliere il tuo metallo dal reattore, puliscilo, e rimetterlo dentro. Ciò comporta la chiusura del gigantesco impianto chimico o il riscaldamento del metallo a temperature pericolosamente alte".
Controintuitivo per la loro capacità di separare rapidamente gli idrogeni dal metano, platino e nichel sono limitati nella produzione di idrocarburi a catena più lunga a causa del coke. Recentemente gli scienziati hanno cercato leghe costituite da un metallo attivo come il platino o il nichel e un metallo inerte come il rame o l'argento. Ma anche con questo tipo di leghe, la coca ha continuato a rappresentare un problema.
Il team di Sykes ha sviluppato un nuovo SAA, o lega a un solo atomo, con solo 1 atomo di platino ogni 100 atomi di rame, per combattere la coke. Gli atomi di platino sono stati isolati nello strato superficiale del metallo per garantire che non reagissero eccessivamente. Gli esperimenti hanno mostrato che singoli atomi di platino nel rame reagiscono ancora per rompere i legami C–H ma non nella misura in cui si forma il coke.
Darby ha quindi simulato il platino puro, rame puro, e il SAA per determinare a quale delle tre superfici un atomo di carbonio si lega più fortemente. Ha ripetuto questo processo con il carbonio legato a uno, Due, tre, e quattro idrogeni così come atomi di idrogeno da soli. Ha scoperto che queste molecole si legano al rame con una maggiore affinità rispetto al platino, e molta più energia è necessaria affinché il rame rompa i legami C–H. I risultati sono fondamentali per spiegare perché il rame è un catalizzatore inefficace.
"Il platino può rompere i legami C–H milioni di volte più velocemente del rame, e la lega è da qualche parte nel mezzo, "Darby ha detto. "Prima di questo SAA, le persone non potevano collegare tra loro due o tre molecole di metano a basse temperature senza disattivare il metallo. Abbiamo dimostrato di poterne ottenere fino a tre".
La scoperta è importante perché non c'è mai stata una lega che potesse rompere efficacemente i legami C–H e anche rimanere resistente al coke.
"Il nostro SAA dimostra che una soluzione a questo problema potrebbe essere possibile, "Darby ha detto. "Spero che questo aiuterà a stimolare la comunità chimica a provare più combinazioni SAA e vedere se possiamo effettivamente trovare la lega che sarà perfetta per questo."
Particelle delle dimensioni di un atomo
Le simulazioni sono state eseguite su risorse OLCF utilizzando il Vienna ab initio Simulation Package (VASP), un codice progettato per modellare materiali su scala atomica. VASP è il più popolare nel suo genere ed è perfettamente su misura per l'uso su computer paralleli ad alte prestazioni come quelli dell'OLCF.
"Modelliamo le cose a livello atomico, "Darby ha detto. "Abbiamo modellato 100 particelle delle dimensioni di un atomo:il catalizzatore e le molecole di metano. Abbiamo quindi calcolato quanta energia ci vuole per convertire il metano in qualcos'altro".
Confrontando questi calcoli tra loro, Darby è stato in grado di spiegare i risultati sperimentali. Riproducendo tutto nell'esperimento, il team ha potuto vedere fino al livello dell'atomo e simulare il numero di volte in cui i legami specifici si sarebbero spezzati, qualcosa che è impossibile contare in un esperimento.
La speranza del team è che un giorno una lega sia in grado di collegare fino a otto metani (l'ottano composto), che poi può essere utilizzato per alimentare le auto. I risultati del progetto e il lavoro in corso del gruppo Stamatakis consentiranno agli sperimentatori di concentrarsi sui più importanti sistemi di leghe piuttosto che testare sistemi casuali.
"Con l'esperimento, sono principalmente tentativi ed errori, "Darby ha detto. "Le simulazioni ci danno una tabella di marcia."