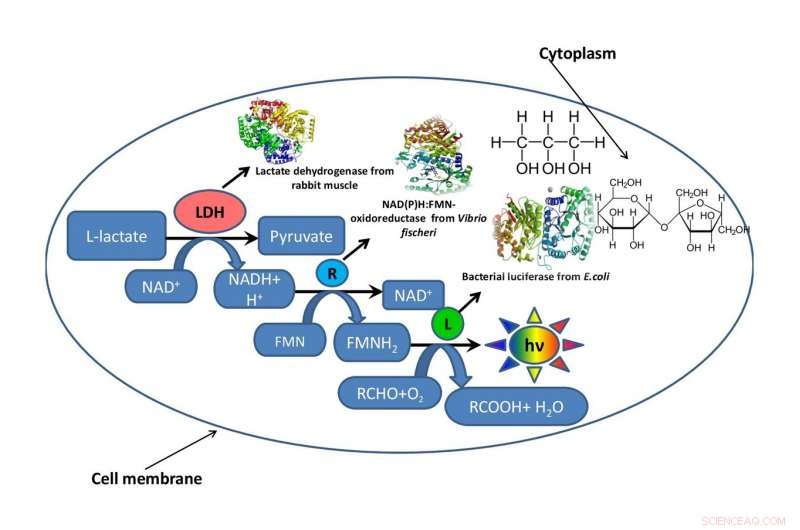
Schema di una cellula batterica con un frammento di catena metabolica funzionante al suo interno circondato da glicerolo o saccarosio che imitano l'ambiente intracellulare. Credito:Oleg Sutormin.
Un team dell'Istituto di biologia e biotecnologia fondamentale della SFU ha utilizzato glicerolo e saccarosio per simulare l'ambiente intracellulare dei batteri luminescenti e ha effettuato una serie di reazioni enzimatiche. Sperano di sviluppare frammenti di catene metaboliche con lunghezze diverse e di studiare reazioni fermentative in condizioni prossime a quelle intracellulari. La ricerca è stata pubblicata su Catalisi Molecolare rivista.
Centinaia di reazioni che coinvolgono gli enzimi si verificano costantemente nelle cellule. Per studiarli più in dettaglio, gli scienziati cercano di creare modelli sperimentali completi dell'ambiente intracellulare. Una caratteristica interessante di tali modelli di ambiente artificiale è la possibilità di regolare i loro parametri per capire come reagirebbe una certa reazione enzimatica e le differenze tra le reazioni enzimatiche in una cellula e quelle in condizioni del tubo.
Per comprendere come la viscosità della miscela di reazione influenzi la velocità dei processi enzimatici, un team dell'Istituto di biologia e biotecnologia fondamentale della SFU ha simulato l'ambiente intracellulare utilizzando due solventi organici:glicerolo e saccarosio. Per testare l'effetto della viscosità della miscela di reazione, gli scienziati hanno utilizzato un frammento di una catena metabolica bioluminescente.
Il lavoro si è articolato in tre fasi. Nella prima fase, i biofisici hanno sviluppato diversi sistemi modello artificiali fatti di glicerolo e saccarosio con diverse concentrazioni di componenti, ma gli stessi livelli di viscosità del mezzo di reazione. Nella seconda fase, hanno determinato come la viscosità della miscela di reazione influenzasse la velocità di una reazione enzimatica nel sistema accoppiato di tre enzimi:LDH, NAD(P)H:FMN-ossidoriduttasi, e luciferasi. Nella terza fase, i ricercatori hanno valutato la stabilità termica del sistema a triplo enzima nell'intervallo di temperature da 15 a 80 gradi.
Come risultato dello studio, gli scienziati hanno concluso che il saccarosio limitava la mobilità degli enzimi in modo più efficiente rispetto al glicerolo. La limitazione della mobilità può portare a cambiamenti nella velocità di reazione o addirittura nel meccanismo. I ricercatori raccomandano ulteriori studi sulla crescente stabilità termica degli enzimi in ambienti con miscele di reazione viscose e l'aumento della temperatura. Propongono anche un approccio per costruire le catene metaboliche cellulari multienzimatiche all'interno della cellula batterica luminosa.
"A causa dell'enorme numero di reazioni enzimatiche all'interno di una cellula reale, affinché il processo del metabolismo si svolga rapidamente e continuamente al suo interno, gli enzimi dovrebbero avere un'elevata cooperatività. Perciò, la maggiore variazione della stabilità termica degli enzimi in presenza di viscogeni, migliore è la cooperazione dei sistemi enzimatici studiati all'interno delle condizioni della cellula reale, e maggiore è la possibilità che un frammento artificiale di una catena metabolica sia naturale per una cellula batterica. È estremamente importante studiare l'influenza dei solventi organici viscosi sulla velocità e sulla stabilità termica delle reazioni enzimatiche. L'unicità del nostro studio è che utilizziamo composti naturali:glicerolo e saccarosio che si trovano effettivamente nella cellula reale, a differenza degli agenti di affollamento utilizzati in studi simili da altri ricercatori, "dice Oleg Sutormin, coautore dello studio, e junior research associate del Laboratorio di Biotecnologie Bioluminescenti della SFU.