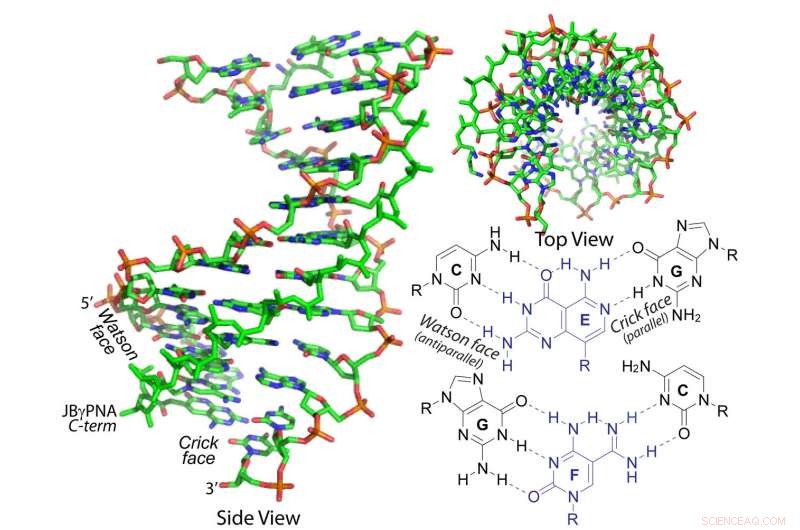
Sviluppato dai ricercatori della Carnegie Mellon University, questo acido nucleico peptide gamma janus (PNA) può invadere la doppia elica del DNA e dell'RNA. Credito:Carnegie Mellon University
I ricercatori della Carnegie Mellon University hanno sviluppato una molecola sintetica in grado di riconoscere e legarsi a DNA o RNA a doppio filamento in normali condizioni fisiologiche. La molecola potrebbe fornire una nuova piattaforma per lo sviluppo di metodi per la diagnosi e il trattamento delle condizioni genetiche. I loro risultati sono pubblicati in Chimica delle comunicazioni .
Il lavoro è stato svolto da un team internazionale di esperti, tra cui Carnegie Mellon Professore di Chimica Danith Ly, un esperto nella progettazione di acidi nucleici peptidici, postdoc in chimica Shivaji Thadke e la studentessa laureata in chimica Dinithi Perera, Professore di Chimica ed esperto di risonanza magnetica nucleare Roberto Gil, e Arnab Mukherjee, un informatico presso l'Indian Institute of Science Education and Research a Pune.
"Dal momento che la struttura a doppia elica del DNA è stata chiarita per la prima volta da Watson e Crick, gli scienziati hanno cercato di progettare molecole in grado di legarsi al DNA e consentire di controllare il flusso di informazioni genetiche, " ha detto Ly. "Questa è la prima molecola bifacciale che può invadere il DNA o l'RNA a doppio filamento in condizioni biologicamente rilevanti".
DNA, che contiene tutte le informazioni genetiche di un organismo, è formato da due filamenti di nucleotidi. I nucleotidi si connettono tra loro mediante legami a idrogeno, formando una catena elicoidale di coppie di basi Watson-Crick. Sebbene queste coppie di basi forniscano un codice relativamente semplice per le nostre informazioni genetiche, entrare nella doppia elica per cambiare il codice è difficile a causa dei forti legami tra le coppie di basi.
Ly e i suoi colleghi dell'Institute for Biomolecular Design and Discovery (IBD) e del Center for Nucleic Acids Science and Technology (CNAST) della Carnegie Mellon University sono leader nella progettazione e nello sviluppo di acidi nucleici gamma peptidici (gamma PNA). Analoghi sintetici del DNA e dell'RNA, i PNA gamma possono essere programmati per legarsi al materiale genetico (DNA o RNA) che causa la malattia, permettendo loro di cercare sequenze dannose e legarsi ad esse per prevenire il malfunzionamento di un gene.
Il gruppo ha creato PNA gamma a doppia faccia chiamati PNA gamma Janus. Prende il nome dal dio romano bifronte, I Janus PNA sono in grado di riconoscere e legarsi con entrambi i filamenti di una molecola di DNA o RNA.
Il concetto di riconoscimento bifacciale, che è la base dei PNA gamma Janus, è stato concepito per la prima volta più di due decenni fa da Jean-Marie Lehn, un premio Nobel noto per il suo lavoro nel campo della chimica supramolecolare, ed esposto da altri ricercatori nel campo.
Il progresso di questa ricerca è stato frenato da due ostacoli. Primo, i ricercatori erano stati in grado di realizzare solo un piccolo numero di basi Janus, e quelle basi variavano considerevolmente in forma e dimensione. Queste limitazioni significavano che le diverse basi di Janus potevano riconoscere solo ripetizioni dello stesso insieme di coppie di basi e non potevano essere usate insieme come mattoni per riconoscere sequenze più complesse nel DNA o nell'RNA.
In secondo luogo, era difficile sintetizzare le basi di Giano per le coppie di basi canoniche. La natura complementare dei due lati delle basi di Giano ha fatto sì che le molecole si ibridassero e si legassero tra loro, impedendo loro di incorporarsi nel DNA e nell'RNA.
Nello studio attuale, Ly e colleghi superano questi ostacoli. Hanno creato una serie completamente nuova di elementi di riconoscimento dell'acido nucleico bifacciale, 16 in totale, che rappresentava ogni possibile combinazione di basi azotate che si poteva trovare nel codice genetico. I PNA gamma Janus possono essere utilizzati per riconoscere qualsiasi combinazione di coppie di basi e combinati e abbinati per rilevare e legarsi a sequenze genetiche complesse.
Thadke ha risolto il problema della sintesi chimica ideando un nuovo metodo sintetico in soluzione e in fase solida per sviluppare i PNA gamma Janus. Ha anche implementato un trucco inerente alla preorganizzazione elicoidale nella spina dorsale del gamma PNA per impedire alle basi di Janus autocomplementari di ibridarsi l'una con l'altra.
Questi nuovi PNA Janus gamma hanno un'energia di legame straordinariamente elevata e sono i primi a essere in grado di invadere una doppia elica canonica di DNA o RNA accoppiato a basi a una forza ionica e a una temperatura fisiologicamente rilevanti.
Lo fanno sfruttando quando le molecole di DNA e RNA a doppio filamento "respirano" e i legami tra le coppie di basi si aprono per frazioni di secondo. Quando questo accade, il Janus PNA si inserisce tra i filamenti separati. Se le coppie di basi non corrispondono, il Janus PNA viene espulso dalla molecola di DNA. Ma se corrispondono, il Janus PNA si lega ad entrambi i filamenti della molecola.
I PNA gamma Janus hanno un'ampia gamma di usi biologici e biomedici. Possono essere progettati per indirizzare il DNA genomico per l'editing genico e la regolazione trascrizionale. Potrebbero anche essere progettati per legarsi in modo specifico e selettivo alla sequenza alle strutture secondarie e terziarie dell'RNA, qualcosa che gli agenti antisenso tradizionali e i ligandi di piccole molecole non sono in grado di fare. Per esempio, i PNA Janus gamma potrebbero essere programmati per legarsi a espansioni ripetute di RNA, che potrebbe portare a nuovi trattamenti per una serie di disturbi neuromuscolari e neurodegenerativi, compresa la distrofia miotonica di tipo 1 e la malattia di Huntington, o agli RNA non codificanti, compreso l'RNA ribosomiale e telomerasico dell'agente patogeno, per combattere le malattie genetiche e infettive.
La tecnologia viene esplorata da startup e aziende farmaceutiche per sviluppi terapeutici.