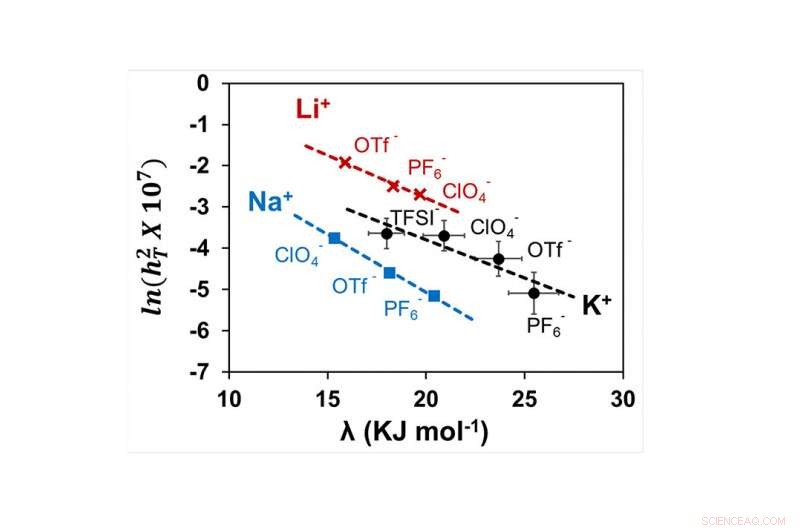
Questo grafico mostra le correlazioni tra tre parametri che portano a un unico descrittore che fornisce una base razionale per progettare composizioni elettrolitiche per batterie metallo alcalino-ossigeno ad alta potenza, comprese le batterie al potassio-aria. Questa ricerca della McKelvey School of Engineering aiuterà gli ingegneri a trovare l'elettrolita giusto per batterie nuove e migliorate, comprese le batterie al potassio-aria. Credito:Ramani lab
Le batterie metallo-aria sono state perseguite come successore delle batterie agli ioni di litio grazie alle loro eccezionali densità di energia gravimetrica. Potrebbero potenzialmente consentire alle auto elettriche di percorrere mille miglia o più con una singola carica.
Un nuovo promettente membro della famiglia delle batterie aria-metallo alcalino è la batteria aria-potassio, che ha più di tre volte la densità di energia gravimetrica teorica delle batterie agli ioni di litio. Una sfida chiave nella progettazione di batterie potassio-aria è la scelta dell'elettrolita giusto, il liquido che facilita il trasferimento di ioni tra il catodo e l'anodo.
Tipicamente, gli elettroliti vengono scelti utilizzando un approccio per tentativi ed errori basato su regole empiriche che mettono in correlazione diverse proprietà degli elettroliti, seguito da test esaustivi (e dispendiosi in termini di tempo) di diversi candidati elettroliti per verificare se si ottiene la prestazione desiderata.
Ricercatori della Washington University di St. Louis, guidato da Vijay Ramani, il Roma B. e Raymond H. Wittcoff Distinguished Professor of Environment &Energy presso la McKelvey School of Engineering, hanno ora mostrato come gli elettroliti per le batterie ad aria con metalli alcalini possono essere scelti utilizzando un singolo, parametro di facile misurazione.
Il loro lavoro è stato pubblicato l'8 luglio nel Atti dell'Accademia Nazionale delle Scienze .
Il team di Ramani ha studiato le interazioni fondamentali tra il sale e il solvente nell'elettrolita e ha mostrato come queste interazioni possono influenzare le prestazioni complessive della batteria. Hanno sviluppato un nuovo parametro, ovvero il Modulo di Thiele "Elettrochimico", una misura della facilità di trasporto di ioni e di reazione su una superficie di un elettrodo.
Questa ricerca documenta la prima volta che la teoria Marcus-Hush del trasferimento di elettroni, vincitrice del premio Nobel, è stata utilizzata per studiare l'impatto della composizione dell'elettrolita sul movimento degli ioni attraverso l'elettrolita, e la loro reazione sulla superficie dell'elettrodo.
È stato dimostrato che questo modulo di Thiele diminuisce esponenzialmente con l'aumento dell'energia di riorganizzazione del solvente, una misura dell'energia necessaria per modificare la sfera di solvatazione di una specie disciolta. Così, l'energia di riorganizzazione del solvente potrebbe essere utilizzata per selezionare razionalmente gli elettroliti per batterie metallo-aria ad alte prestazioni. Niente più tentativi ed errori.
"Abbiamo iniziato cercando di capire meglio l'influenza dell'elettrolita sulla reazione di riduzione dell'ossigeno nei sistemi di batterie metallo-aria, " disse Shrihari Sankarasubramanian, un ricercatore del team di Ramani e autore principale dello studio.
"Abbiamo finito per mostrare come la diffusione degli ioni nell'elettrolita e la reazione di questi ioni sulla superficie dell'elettrodo siano entrambe correlate all'energia necessaria per rompere il guscio di solvatazione attorno agli ioni disciolti".
"Mostrare come un descrittore di un singolo parametro dell'energia di solvatazione sia correlato sia al trasporto ionico che alla cinetica di reazione superficiale è un passo avanti rivoluzionario, "Ha detto Ramani. "Ci permetterà di sviluppare razionalmente nuovi elettroliti ad alte prestazioni per batterie metallo-aria".