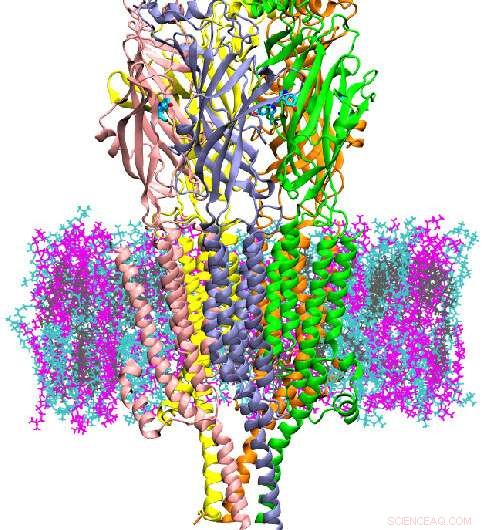
Credito:A. James Clark School of Engineering, Università del Maryland
Scienziati dell'Università del Maryland (UMD) e del National Institute of Standards and Technology (NIST) hanno scoperto un modo per rilevare il meccanismo molecolare mediante il quale 5HT3A, un recettore della serotonina situato nella sinapsi del neurone, è attivato. Avere un modello molecolare di questa attivazione consentirà la sperimentazione di inibitori farmaceutici utilizzando modelli informatici anziché esperimenti tradizionali, potenzialmente riducendo il costo e il tempo di screening di nuovi farmaci.
Lo studio condotto da Jeffery Klauda, un professore di Ingegneria Chimica e Biomolecolare (ChBE) presso l'Università del Maryland (UMD), è stato pubblicato in Atti dell'Accademia Nazionale delle Scienze ( PNAS ) oggi. Nicola Guros, un assistente di ricerca laureato ChBE, è stato il primo autore dello studio ed è stato co-consigliato da Arvind Balijepalli, un ingegnere meccanico al NIST.
5HT3A è un tipo di proteina nota come canale ionico, implicato nella depressione, ansia e mirato a ridurre la nausea indotta dalla chemioterapia. Regola il flusso di ioni nella fessura postsinaptica dei neuroni. Gli autori hanno eseguito simulazioni al computer di 5HT3A per un massimo di 20 microsecondi, molto più a lungo delle precedenti simulazioni eseguite per
"Se pensi alla dinamica molecolare (MD) come a un microscopio molecolare, questo significa che siamo in grado di osservare il meccanismo di attivazione x10 più a lungo del passato, " ha detto Guros. "Nuove capacità computazionali possono fornire il potere di osservare l'attivazione molecolare di proteine complesse in tempi significativamente maggiori. Più lungo è questo lasso di tempo, la migliore convalida che possiamo avere dei risultati sperimentali per dimostrare che i modelli MD sono un metodo robusto per studiare le proteine e testare i prodotti farmaceutici".
L'attivazione e la desensibilizzazione di proteine come 5HT3A si verificano in millisecondi, così mentre più vicino alla vera scala temporale, gli scienziati sono ancora un po' indietro nell'osservare l'intero ciclo di trasporto della proteina. Questo studio, però, è stato in grado di fornire informazioni sugli effetti del legame della serotonina sullo sviluppo di uno stato preattivo di 5HT3A e su come la diversità dei lipidi di membrana influenzi la struttura e la funzione delle proteine.
Rimane molto spazio di simulazione da esplorare con questi modelli, ed è stato reso possibile solo negli ultimi anni con progressi nella potenza di calcolo. Nello specifico, questo studio è stato eseguito utilizzando un'allocazione basata su sovvenzioni sul supercomputer Anton2 gestito dal Pittsburgh Supercomuting Center (PSC) e sponsorizzato dalla ricerca DE Shaw. Le tradizionali risorse di calcolo ad alte prestazioni non sarebbero in grado di raggiungere i tempi di questo studio.
Con l'aumentare della velocità e della potenza di calcolo in futuro, il gruppo spera di studiare gli effetti dei farmaci, come granisetron o ondansetron, nel tentativo di modellare accuratamente i loro effetti sulla proteina e studiare altre terapie mirate.