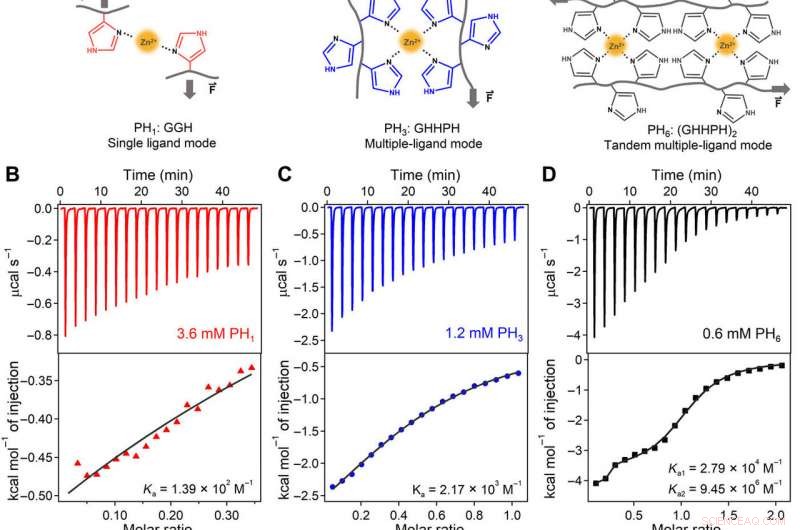
Ingegneria della cooperazione, costanti di legame, e meccanismo molecolare delle interazioni di coordinazione degli ioni metallici a livello molecolare per il carico. (A) I complessi di coordinazione degli ioni metallici formati da singoli ligandi (PH1, a sinistra) sono dinamici e deboli. Quando si forma un sito di chelazione del metallo composto da più ligandi (PH3, mezzo), il legame degli ioni metallici diventa molto più forte e meno dinamico di quello dei singoli ligandi. Per di più, quando si organizzano due siti di chelazione dei metalli in tandem (PH6, Giusto), l'affinità di legame, resistenza meccanica, e il tasso di associazione può essere migliorato grazie alla cooperazione tra i due siti. (da B a D) dati di titolazione ITC di PH1 (sinistra), PH3 (al centro), e PH1 (a destra) peptidi con ZnCl2 in tampone tris 1 M (pH 7,60, contenente 300 mM KCl) a 25°C. (E) Zn2+-costanti di legame (Ka) di PH3 e peptidi PH3 mutati. Gli amminoacidi mutati sono evidenziati in rosso. Le barre di errore rappresentano gli errori di adattamento. (F) Costanti di legame Zn2+ di PH6 e peptidi PH6 mutati. I pannelli sinistro e destro corrispondono a Ka1 e Ka2 per i due siti di legame di PH6. Solo i peptidi PH6 e (GHHGH)2 hanno mostrato due costanti di legame. Il resto dei peptidi ha mostrato caratteristiche di legame a sito singolo. Le barre di errore rappresentano gli errori di adattamento. (G a J) spettri CD di (G) PH1:GGH; (H) PH3:GHHPH; (I) PH6:(GHHPH)2; e (J) (GHHGH)2 peptidi in assenza e presenza di ioni Zn2+. I contenuti relativi delle strutture PPII di PH1 e PH3 sono 9,6 e 34,2% in base all'altezza del picco CD maggiore a 205 nm, assumendo che il complesso PH6-Zn2+ mostri una struttura elicoidale PPII al 100%. (K) Illustrazione schematica del meccanismo di legame Zn2+ cooperativo di PH6. Il cambiamento conformazionale del primo sito di coordinazione porta a cambiamenti strutturali del secondo verso una conformazione più favorevole al legame di Zn2+. N / A, non applicabile. Credito:progressi scientifici, doi:10.1126/sciadv.aaz9531
I tessuti portanti come muscoli e cartilagini mostrano tipicamente un'elevata elasticità, tenacità e velocità di recupero veloci. Però, combinare tali proprietà meccaniche in laboratorio per costruire biomateriali sintetici è fondamentalmente una sfida. In un nuovo studio ora pubblicato su Progressi scientifici , Wenxu Sun e un gruppo di ricerca in fisica, meccanica ingegneristica e dispositivi intelligenti in Cina, sviluppato un forte, idrogel resistente e a rapido recupero. Il team ha progettato il materiale utilizzando reticolanti con interazioni dinamiche cooperative. Hanno progettato un decapeptide ricco di istidina (catena di 10 amminoacidi) contenente due motivi leganti lo zinco (Zn) in tandem (consecutivo) per facilitare la stabilità termodinamica, forza di legame più forte e velocità di legame più rapida del costrutto, rispetto ai singoli motivi proteici leganti o alle proteine ligando isolate. Gli idrogel della rete ibrida ingegnerizzata con il complesso di zinco peptidico hanno mostrato un'elevata stabilità, tenacità e recupero veloce in pochi secondi. Il team di ricerca si aspetta che gli scaffold gestiscano efficacemente le applicazioni di ingegneria dei tessuti portanti e funzionino come elementi costitutivi per la robotica morbida. I nuovi risultati forniscono un percorso generale per mettere a punto le proprietà meccaniche e dinamiche degli idrogel a livello molecolare.
Quando camminiamo, i nostri muscoli, cartilagine e tendini sono soggetti a notevoli carichi meccanici, ma i tessuti biologici possono riprendersi rapidamente per funzionare in modo affidabile per molti cicli meccanici. I bioingegneri hanno esplorato idrogel morbidi con proprietà meccaniche simili ai muscoli come attuatori biomeccanici, cartilagine sintetica, muscolo artificiale, pelle ionica e nella robotica morbida. Hanno dedicato molti sforzi per migliorare la resistenza meccanica e la tenacità degli idrogel introducendo speciali meccanismi di dissipazione dell'energia. Il recupero rapido è anche una caratteristica unica per i tessuti molli portanti, oltre alla resistenza meccanica e alla tenacità, ma gli idrogel sintetici mancano ancora di un meccanismo per un rapido recupero. Ad esempio, idrogel tradizionali a doppia rete (DN) o a rete ibrida (HN) con catene polimeriche corte poiché le reti sacrificali in genere non possono riprendersi presto, spesso impiegando da pochi minuti a giorni.
La forza di un idrogel dipende dalla durata dei suoi reticolanti, dove la lenta cinetica di legame/svincolamento porta a forti idrogel, mentre i tassi di cambio veloci producono quelli morbidi. Per ottenere elevata resistenza e tenacità i reticolanti devono essere lenti, ma per ottenere un rapido recupero, i reticolanti devono essere dinamici con alti tassi di associazione e dissociazione. Per superare questa contraddizione, i materiali portanti presenti in natura hanno utilizzato la cooperatività delle interazioni deboli. In questo lavoro, Sole et al. idrogel di rete ibrida (HN) ingegnerizzati in modo simile con un complesso peptide-metallo appositamente progettato come reticolante fisico. Il team ha formato efficienti siti di legame del metallo in una sequenza peptidica per progettare idrogel con le caratteristiche richieste.
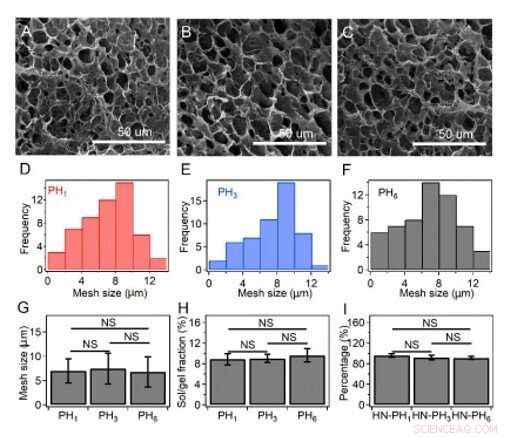
Dimensione della maglia, frazioni sol/gel, e la percentuale effettiva di peptidi incorporati nella rete di idrogel. (A-C) Immagini SEM del gel HN-PH1 (A), il gel HN-PH3 (B) e il gel HN-PH3 (C) prima di aggiungere ioni Zn2+. (D-F) Distribuzioni delle dimensioni delle maglie del gel HNPH1 (D), Gel HN-PH3 (E) e gel HN-PH6 (F) stimati dalle immagini SEM utilizzando il software ImageJ. (G) Dimensione media delle maglie dei gel HN-PHn in assenza di ioni Zn2+. (H) Frazioni sol/gel di diversi gel HN-PHn prima dell'aggiunta di zinco. (I) La percentuale di peptidi incorporati nella rete di idrogel. Le concentrazioni iniziali del peptide erano 0,3 M, 0,10 M, e 0,05 M per PH1, PH3, e PH6, rispettivamente. La percentuale dei peptidi incorporati negli idrogel era simile, come stimato sottraendo la frazione dei peptidi eluiti dalla quantità totale utilizzata. Le barre di errore indicano la media ± S.D. NS:p> 0,05. Credito:progressi scientifici, doi:10.1126/sciadv.aaz9531
Il team ha prima progettato tre brevi peptidi ricchi di istidina (peptidi HR) come ligandi per legarsi con ioni zinco (Zn 2+ ) e costruire idrogeli HN. Hanno indicato le sequenze peptidiche come PH 1 , PH 3 e PH 6 in base al numero di istidine legate. Sole et al. ha sintetizzato i peptidi utilizzando la sintesi peptidica in fase solida e li ha purificati con cromatografia liquida ad alte prestazioni. Hanno osservato la formazione di Zn 2+ complessi di coordinazione dell'istidina mediante spettroscopia ultravioletta (UV) e Raman. La sequenza peptidica specificamente progettata ha permesso a Zn . sinergico e cooperativo 2+ affinità di legame, rispetto ai peptidi con residui casuali di istidina sulle loro sequenze. Gli scienziati hanno studiato il meccanismo molecolare dello ione zinco cooperativo che si lega al PH 6 utilizzando il dicroismo circolare, i risultati suggeriscono cambiamenti conformi del primo sito di coordinazione di PH 6 essere fondamentale per il legame cooperativo e ha mostrato come i cambiamenti strutturali favorissero ulteriori Zn 2+ legame.
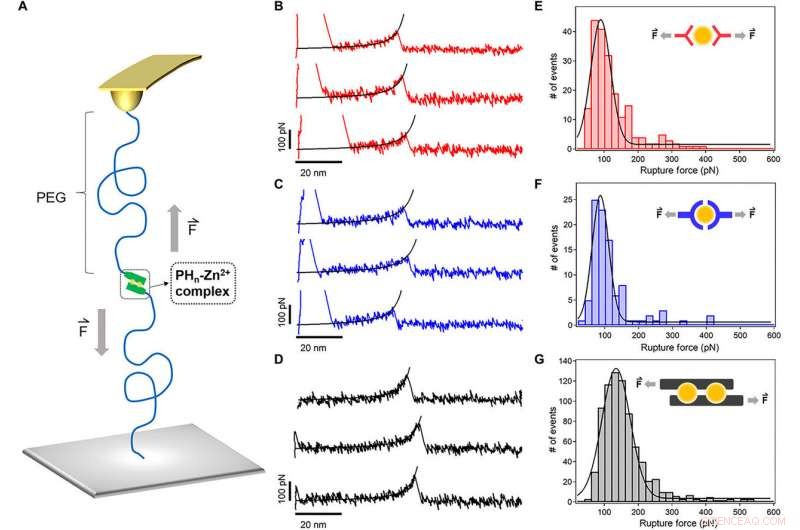
Spettroscopia di forza a singola molecola dei complessi di coordinazione di ioni metallici. (A) Diagramma schematico degli esperimenti di spettroscopia di forza a singola molecola basati su AFM. I ligandi peptidici sono stati collegati alla punta del cantilever e al substrato tramite un linker PEG (MW, 5 kDa). (B a D) Curve tipiche forza-estensione per la rottura di PH1-Zn2+ (rosso), PH3-Zn2+(blu), e complessi PH6-Zn2+ (nero) a una velocità di trazione di 1000 nm s-1. L'adattamento a catena a forma di verme delle curve di estensione della forza (linee nere) ha confermato che il picco a un'estensione di ~ 50 nm corrisponde alla rottura di un singolo legame di chelazione ionica metallica. (da E a G) Gli istogrammi della forza di rottura per PH1-Zn2+ (rosso), PH3-Zn2+(blu), e PH6-Zn2+ (nero), rispettivamente. Il raccordo gaussiano mostra le forze di rottura medie di 90 ± 29, 87 ± 24, e 135 ± 41 pN, rispettivamente. Le modalità di legame dello ione Zn2+ proposte per i tre peptidi sono mostrate nei riquadri. Credito:progressi scientifici, doi:10.1126/sciadv.aaz9531
Sole et al. ha utilizzato tecniche avanzate come la spettroscopia di forza a singola molecola (SMF) basata sulla microscopia a forza atomica (AFM) per misurare la stabilità meccanica dell'HR-peptide-Zn 2+ complessi cioè reticolanti dell'idrogel a livello molecolare. Le forze di rottura medie erano molto più alte per PH 6 rispetto ad altri tipi di idrogel, confermando la tenacità dell'idrogel. I risultati hanno mostrato che la stabilità meccanica dei complessi metallo-ligando potrebbe essere notevolmente migliorata in base ai siti di legame.
The team explored if changes to the intrinsic properties of crosslinkers could alter macroscopic mechanical properties of the hydrogel by preparing a series of hybrid network (HN) hydrogels. They used HR-peptide-Zn 2+ as sacrificial crosslinkers and covalent bonds as permanent crosslinkers in the constructs and named the resulting hydrogels as HN-PH 1 , HN-PH 3 , and HN-PH 6 , based on the peptide sequence used. The network structures were similar in all three hydrogels but the HN-PH 6 gel was more compressible compared to the others, while functioning effectively under stressful mechanical environments. interessante, the scientists could even twist the HN-PH 6 hydrogel into a spiral shape and compress the material with a sharp blade without causing it permanent damage.

Compressing the HN-PH6 hydrogel using a sharp blade does not damage the material. Credit:Science Advances, doi:10.1126/sciadv.aaz9531
The team conducted tensile mechanical tests on the gels and correlated the results on the bulk level with those at the molecular level, to show remarkably higher break strain, Young's modulus and toughness for the HN-PH 6 gels. Sun et al. then examined the recovery property of the material based on loading-unloading cycles and found HN-PH 6 gels to almost totally recover its macroscopic mechanical properties in minutes. Però, if they cut up the HN-PH 6 gels into pieces, the hydrogel could not self-heal since covalent crosslinkers do not reform after fracture. To understand the experimental outcomes, the research team also conducted theoretical analyses and proposed cooperative zinc binding on PH 6 to be an important factor, among other factors to form strong and tough hydrogels with fast recovery rates.
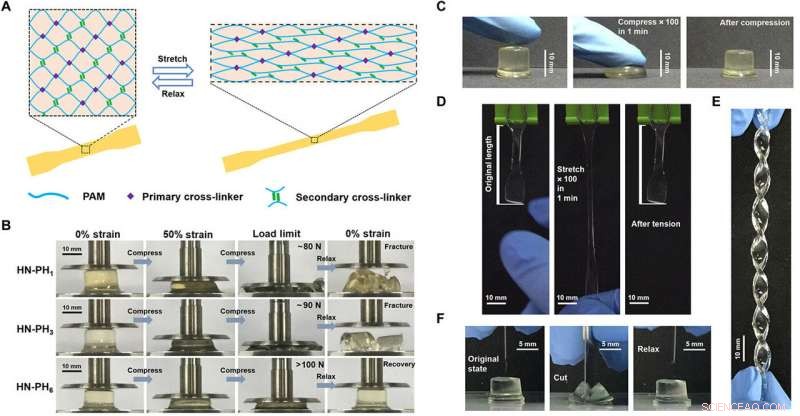
Structure and properties of HN-PHn HN hydrogels cross-linked by the peptide-Zn2+ coordination complexes. (A) Schematic illustration of the network structure of HN-PHn hydrogels. The network comprises covalent bonds as the primary cross-linkers and ligand-metal interactions as the secondary cross-linkers. (B) Optical images of the HN-PH1 (top), HN-PH3 (middle), and HN-PH6 (bottom) hydrogels under a compression-relaxation cycle. The HN-PH1 and HN-PH3 gels were fractured, whereas the HN-PH6 gel was almost fully recovered. (C) Optical images of the HN-PH6 gel under an extreme compressive condition (compressed to>70% strain for 100 times at 1.6 Hz). (D) Optical images of the HN-PH6 gel under an extreme tensile condition (stretched to>150% strain for 100 times at 1.6 Hz). (E) Optical image of the HN-PH6 gel twisted into a spiral shape. (F) Optical images of the HN-PH6 gel compressed with a sharp blade and relaxed. No detectable cut was observed on the gel. PAM, polyacrylamide. Photo credits:Wenxu Sun, Nanjing University. Credit:Science Advances, doi:10.1126/sciadv.aaz9531
In questo modo, Wenxu Sun and colleagues developed a novel hydrogel material, bioinspired by histidine residues found in natural load-bearing materials. Combining such outstanding mechanical properties in the lab has remained a challenge due to the inability to effectively harness the unique metal ion binding properties that are encoded in natural proteins. In this work, Sun et al. used bioinspired Zn 2+ -binding peptide as crosslinkers to form the desired hydrogels at the molecular level, highlighting the importance of cooperative metal coordination during materials synthesis. They intend to examine additional mechanical features, such as adhesion to other tissues, before conducting practical applications in tissue engineering.
© 2020 Scienza X Rete