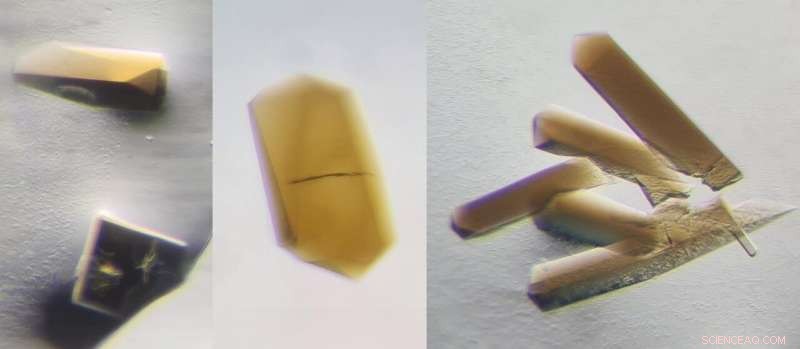
Cristalli di CODH/ACS ottenuti in assenza di ossigeno. Il colore marrone deriva dai metalli naturali ospitati dalle proteine. Credito:Max Planck Institute for Marine Microbiology/T. Wagner
I gas di scarico di molti rami dell'industria contengono principalmente monossido di carbonio e anidride carbonica. Oggi, questi gas vengono semplicemente soffiati nella nostra atmosfera, ma questo potrebbe presto cambiare. L'idea è quella di utilizzare il potere dei batteri per trasformare i gas di scarico tossici in composti preziosi come l'acetato o l'etanolo. Questi possono essere utilizzati successivamente come biocarburanti o composti di base per materiali sintetici. Sono già in fase di valutazione i primi impianti di prova a grandezza naturale, utilizzando questa conversione su scala industriale, e le stelle di questi processi sono batteri che divorano monossido di carbonio, anidride carbonica e diidrogeno, tra i quali Clostridium autoethanogenum è di gran lunga il favorito.
"In questo microbo, sono state caratterizzate le principali linee del metabolismo utilizzate per operare la conversione del gas, "dice Tristan Wagner, leader del gruppo Microbial Metabolism presso il Max Planck Institute for Marine Microbiology. "Ma ci sono ancora molti punti interrogativi a livello molecolare". Quello su cui si concentrano gli scienziati di Brema:come viene elaborato il monossido di carbonio tossico dagli enzimi con un'efficienza così sorprendente?
Grande sorpresa in un cristallo
La conoscenza a livello molecolare della conversione del monossido di carbonio deriva da studi effettuati nella specie Moorella thermoacetica. Questo è un organismo modello marino conveniente e ben studiato, ma mostra una scarsa capacità di disintossicare i gas di scarico, a differenza del Clostridium autoethanogenum. Entrambi i batteri utilizzano lo stesso enzima per convertire il monossido di carbonio:la CO-deidrogenasi/Acetil-CoA sintasi, abbreviato come CODH/ACS. È un enzima molto comune che esisteva già nei tempi primordiali della terra. "Dal momento che entrambe le specie usano lo stesso enzima per convertire il monossido di carbonio, ci aspettavamo di vedere esattamente la stessa struttura con eventuali differenze minori, "dice Wagner.
Per la loro ricerca, Wagner e il suo collega Olivier N. Lemaire stanno studiando il batterio Clostridium autoethanogenum per capire come può prosperare alla termodinamica della Vita, utilizzando un metabolismo simile a quello delle prime forme viventi. Olivier N. Lemaire ha coltivato i batteri e ha purificato il suo CODH/ACS in assenza di ossigeno, che è dannoso per l'enzima. I due scienziati hanno utilizzato il metodo di cristallizzazione per ottenere cristalli dell'enzima CODH/ACS e determinare la struttura 3-D della proteina mediante cristallografia a raggi X. "Quando abbiamo visto i risultati, non potevamo credere ai nostri occhi, " dice Wagner. "L'interfaccia CODH-ACS da Clostridium autoethanogenum differisce drasticamente dal modello di Moorella thermoacetica, anche se era lo stesso enzima e batteri simili."
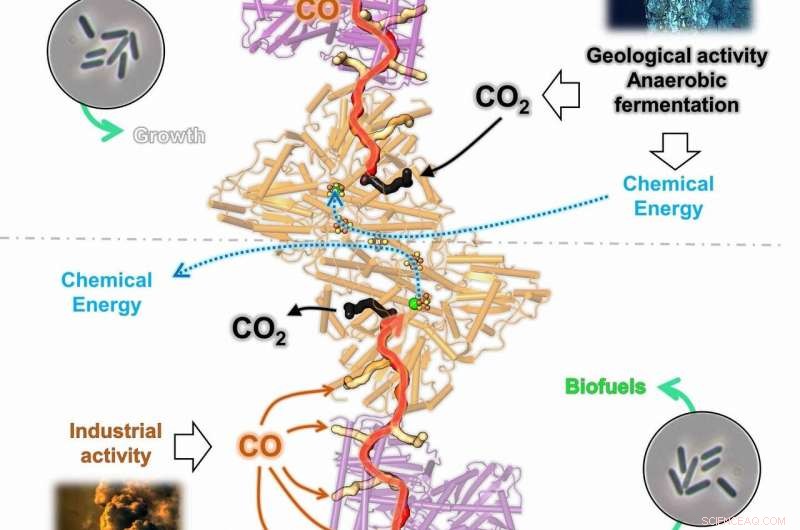
Il grafico mostra la bidirezionalità del complesso CODH/ACS di C. autoethanogenum (CODH in arancione e ACS in viola). In condizioni chemolitoautotrofiche, l'enzima può trasformare l'anidride carbonica (CO2) in monossido di carbonio (CO), sequestrato in un canale del gas (in alto). Il CO sarà trasformato in acetil-CoA, l'elemento costitutivo della cellula utilizzato per ottenere energia cellulare e costruire il materiale cellulare. Durante il processo di conversione del gas, la CO rilasciata dall'attività industriale può essere utilizzata in modo molto efficiente dal CODH/ACS (in basso). Viene catturato dai numerosi canali di gas e genera contemporaneamente Acetil-CoA ed energia chimica, permettendo alla cellula di fare una vita di CO. Credito:O. Lemaire e T. Wagner. L'immagine utilizzata non protetta da copyright è stata ottenuta dalla National Oceanic and Atmospheric Administration (NOAA) e dalla libreria di foto Pexel (Black Smoker; NOAA Office of Ocean Exploration and Research, 2016 Esplorazione delle acque profonde delle Marianne; Fotografia di fabbrica di Chris LeBoutillier
Stessi ingredienti, architettura diversa
Dopo, i due ricercatori hanno effettuato ulteriori esperimenti per dimostrare che la prima struttura non era un artefatto ma la realtà biologica. Gli esperimenti successivi hanno confermato il modello iniziale. Così, la scoperta smentisce chiaramente l'assunto precedente che l'enzima CODH/ACS ha sempre la stessa struttura complessiva. "L'enzima di Moorella thermoacetica ha una forma lineare, " spiega Olivier N. Lemaire, primo autore dello studio, che è stato recentemente pubblicato sulla rivista scientifica BBA Bioenergetica . "Nella Moorella termoacetica, l'enzima produce monossido di carbonio nel CODH e lo utilizza nell'ACS. Fra loro, è intrappolato e incanalato attraverso un canale del gas sigillato. ACS alla fine sintetizzerà acetil-CoA, un elemento costitutivo ulteriormente trasformato in acetato ed etanolo. Il resto della cellula non vede monossido di carbonio".
Ma il Clostridium autoethanogenum assorbe direttamente il monossido di carbonio. "Nel Clostridium autoethanogenum l'enzima CODH/ACS non ha una sola apertura, ma parecchi. In questo modo può raccogliere quanto più monossido di carbonio possibile e convogliarlo in un intero sistema di gallerie, operando in entrambe le direzioni, " dice Lemaire. "Questi risultati mostrano un rimescolamento dei tunnel di gas interni durante l'evoluzione di questi batteri, presumibilmente portando a un complesso bidirezionale che assicura un elevato flusso di conversione del monossido di carbonio verso il risparmio energetico e l'assimilazione del monossido di carbonio, fungendo da principale propulsore cellulare." Alla fine del processo vengono generati anche acetato ed etanolo, che può essere utilizzato per produrre combustibili.
"Ora abbiamo un'immagine di come appare questo enzima molto efficiente e robusto, " dice Tristan Wagner. "Ma la nostra scoperta è solo un passo avanti. Tra l'altro, è ancora una questione aperta come il batterio possa sopravvivere e utilizzare il monossido di carbonio per soddisfare il proprio fabbisogno energetico cellulare. Abbiamo alcune ipotesi, ma siamo ancora all'inizio. Per comprendere l'intero processo chimico di conversione del monossido di carbonio in acetato ed etanolo, ulteriori proteine devono essere studiate."