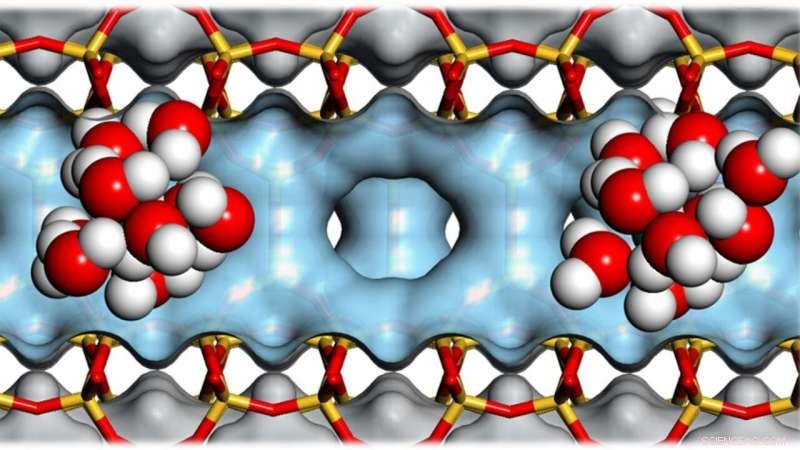
Grappoli di molecole d'acqua all'interno delle cavità delle zeoliti aiutano a catalizzare la conversione della biomassa in biocarburante. Credito:Andreas Jentys / TUM
Le zeoliti sono materiali estremamente porosi:dieci grammi possono avere una superficie interna delle dimensioni di un campo da calcio. Le loro cavità li rendono utili per catalizzare reazioni chimiche e quindi risparmiare energia. Un team di ricerca internazionale ha ora fatto nuove scoperte sul ruolo delle molecole d'acqua in questi processi. Un'applicazione importante è la conversione della biomassa in biocarburante.
Il combustibile ricavato dalla biomassa è considerato climaticamente neutro, sebbene sia ancora necessaria energia per produrlo:le reazioni chimiche desiderate richiedono alti livelli di temperatura e pressione.
"Se in futuro dobbiamo fare a meno delle fonti energetiche fossili e fare un uso efficiente su larga scala della biomassa, dovremo anche trovare il modo di ridurre l'energia necessaria per la lavorazione della biomassa, "dice Johannes Lercher, professore di tecnologia chimica presso l'Università tecnica di Monaco (TUM) e direttore dell'Istituto per la catalisi integrata presso il Pacific Northwest National Laboratory a Richland, Washington (Stati Uniti).
Collaborando con un gruppo di ricerca internazionale, Lercher ha esaminato più da vicino il ruolo delle molecole d'acqua nelle reazioni all'interno dei pori della zeolite, di dimensioni inferiori a un nanometro.
Tutto inizia con gli acidi
Una caratteristica di un acido è che dona facilmente protoni. Così, quando aggiunto all'acqua, l'acido cloridrico si scinde in anioni cloruro carichi negativamente, come quelli che si trovano nei cristalli di sale da cucina, e protoni carichi positivamente che si attaccano alle molecole d'acqua. Ciò si traduce in uno ione idronio caricato positivamente, che sembra passare ulteriormente su questo protone, per esempio a una molecola organica.
Quando la molecola organica è "costretta" ad accettare un protone, cerca di stabilizzarsi. Così, un alcol può dare origine a una molecola con un doppio legame, una tipica fase di reazione nel percorso dalla biomassa al biocarburante. Le pareti di zeolite stabilizzano gli stati di transizione che si verificano durante la conversione e, così, aiutano a ridurre al minimo la quantità di energia richiesta dalla reazione per verificarsi.

Prof. Lercher nel suo laboratorio presso il Dipartimento di Chimica dell'Università Tecnica di Monaco di Baviera. Credito:Andreas Heddergott / TUM
Zeoliti che agiscono come acidi
Le zeoliti contengono atomi di ossigeno nella loro struttura cristallina che già trasportano un protone. Come gli acidi molecolari, formano ioni idronio attraverso le interazioni con l'acqua.
Però, mentre gli ioni idronio si disperdono in acqua, rimangono strettamente associati alla zeolite. Il pretrattamento chimico può variare il numero di questi centri attivi e, così, stabilire una certa densità di ioni idronio nei pori della zeolite.
La zeolite ideale per ogni reazione
Variando sistematicamente la dimensione delle cavità, la densità dei siti attivi e la quantità di acqua, il team di ricerca è stato in grado di chiarire le dimensioni dei pori e le concentrazioni di acqua che hanno catalizzato al meglio reazioni di esempio selezionate.
"Generalmente, è possibile aumentare la velocità di reazione riducendo i pori e aumentando la densità di carica, " Johannes Lercher spiega. "Tuttavia, questo aumento ha i suoi limiti:quando le cose si fanno troppo affollate e le cariche sono troppo vicine l'una all'altra, la velocità di reazione diminuisce di nuovo. In questo modo è possibile trovare le condizioni ottimali per ogni reazione".
"Le zeoliti sono generalmente adatte come nanoreattori per tutte le reazioni chimiche i cui partner di reazione si inseriscono nei pori e in cui un acido viene utilizzato come catalizzatore, " sottolinea Lercher. "Siamo all'inizio di uno sviluppo con il potenziale per aumentare la reattività delle molecole anche a basse temperature e, così, risparmiare considerevoli quantità di energia nella produzione di combustibili o prodotti chimici."