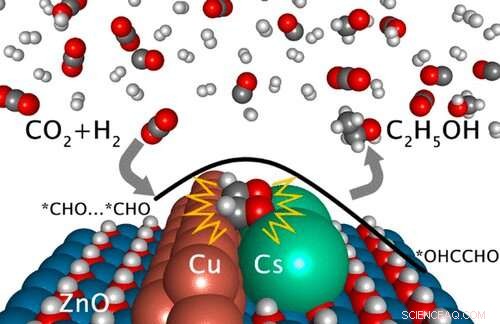
Astratto grafico. Credito:DOI:10.1021/jacs.1c03940
Una collaborazione internazionale di scienziati ha compiuto un passo significativo verso la realizzazione di una tecnologia a zero emissioni di carbonio quasi "verde" che convertirà in modo efficiente l'anidride carbonica, un importante gas serra, e l'idrogeno in etanolo, che è utile come combustibile e ha molte altre applicazioni chimiche. Lo studio riporta una "tabella di marcia" per navigare con successo questa reazione impegnativa e fornisce un quadro dell'intera sequenza di reazione utilizzando la modellazione teorica e la caratterizzazione sperimentale.
Guidato dal Brookhaven National Laboratory del Dipartimento dell'Energia degli Stati Uniti (DOE), il gruppo ha stabilito che portando cesio, rame, e l'ossido di zinco insieme in una configurazione a stretto contatto catalizza una via di reazione che trasforma l'anidride carbonica (CO 2 ) in etanolo (C2H6O). Hanno anche scoperto perché questa interfaccia in tre parti ha successo. Lo studio, che è descritto in un articolo nell'edizione online del 23 luglio del Giornale della Società Chimica Americana ed è presente sulla copertina della pubblicazione, guiderà ulteriori ricerche su come sviluppare un catalizzatore industriale pratico per la conversione selettiva di CO 2 in etanolo. Tali processi porteranno a tecnologie in grado di riciclare la CO 2 emessi dalla combustione e convertirli in prodotti chimici o combustibili utilizzabili.
Nessuno dei tre componenti esaminati nello studio è in grado di catalizzare individualmente la CO 2 -conversione in etanolo, né possono in coppia. Ma quando il trio è riunito in una certa configurazione, la regione in cui si incontrano apre una nuova rotta per la formazione del legame carbonio-carbonio che rende la conversione della CO 2 all'etanolo possibile. La chiave di questo è l'interazione ben sintonizzata tra il cesio, rame, e siti di ossido di zinco.
"C'è stato molto lavoro sulla conversione dell'anidride carbonica in metanolo, tuttavia l'etanolo ha molti vantaggi rispetto al metanolo. Come carburante, l'etanolo è più sicuro e più potente. Ma la sua sintesi è molto impegnativa a causa della complessità della reazione e della difficoltà di controllare la formazione del legame C-C, " ha detto il ricercatore corrispondente dello studio, Ping Liu, chimico di Brookhaven. "Ora sappiamo che tipo di configurazione è necessaria per effettuare la trasformazione, e i ruoli che ogni componente svolge durante la reazione. È una grande svolta".
L'interfaccia si forma depositando piccole quantità di rame e cesio su una superficie di ossido di zinco. Per studiare le regioni in cui i tre materiali si incontrano, il gruppo si è rivolto a una tecnica a raggi X chiamata spettroscopia di fotoemissione a raggi X, che ha mostrato un probabile cambiamento nel meccanismo di reazione per la CO 2 idrogenazione quando è stato aggiunto il cesio. Maggiori dettagli sono stati rivelati utilizzando due approcci teorici ampiamente utilizzati:calcoli della "teoria del funzionale della densità", un metodo di modellazione computazionale per studiare le strutture dei materiali, e "simulazione cinetica Monte Carlo, " simulazione al computer per simulare la cinetica di reazione. Per questo lavoro, il gruppo ha utilizzato le risorse di calcolo del Center for Functional Nanomaterials di Brookhaven e del National Energy Research Scientific Computing Center del Lawrence Berkeley National Laboratory, entrambe le strutture per gli utenti dell'Ufficio delle scienze del DOE.
Una delle cose che hanno imparato dalla modellazione è che il cesio è un componente vitale del sistema attivo. Senza la sua presenza, l'etanolo non può essere prodotto. Inoltre, è importante anche un buon coordinamento con rame e ossido di zinco. Ma c'è molto altro da imparare.
"Ci sono molte sfide da superare prima di arrivare a un processo industriale in grado di trasformare l'anidride carbonica in etanolo utilizzabile, " ha detto il chimico di Brookhaven José Rodriguez, che ha partecipato ai lavori. "Per esempio, ci deve essere un modo chiaro per migliorare la selettività verso la produzione di etanolo. Una questione chiave è capire il legame tra la natura del catalizzatore e il meccanismo di reazione; questo studio è in prima linea in questo sforzo. Puntiamo a una comprensione fondamentale del processo".
Un altro obiettivo di quest'area di ricerca è trovare un catalizzatore ideale per la CO 2 conversione ad alcoli "superiori", che hanno due o più atomi di carbonio (l'etanolo ne ha due) e sono, perciò, più utile e desiderabile per le applicazioni industriali e la produzione di beni di consumo. Il catalizzatore studiato in questo lavoro è vantaggioso perché i catalizzatori a base di rame e ossido di zinco sono già diffusi nell'industria chimica e utilizzati in processi catalitici come la sintesi del metanolo da CO 2 .
I ricercatori hanno pianificato studi di follow-up presso la National Synchrotron Light Source II di Brookhaven, anche un DOE Office of Science User Facility, che offre una suite unica di strumenti e tecniche per la caratterizzazione dei catalizzatori in condizioni di lavoro. Là, studieranno più in dettaglio il sistema Cu-Cs-ZnO e catalizzatori di diversa composizione.