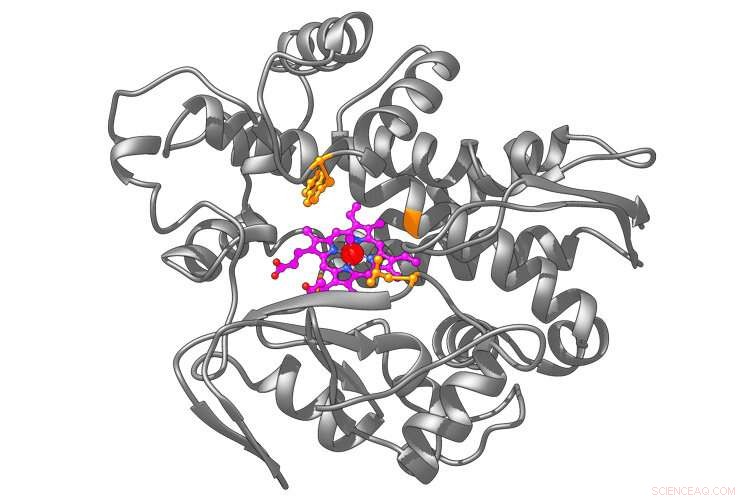
Un metalloenzima artificiale basato sull'enzima naturale chiamato P450 (struttura grigia). I chimici dell'Università di Berkeley hanno creato una molecola di eme (magenta) con un atomo di iridio incorporato (rosso) che, nell'E. coli, è stato incorporato in P450 per eseguire una reazione sconosciuta nel mondo naturale. Credito:immagine dell'UC Berkeley di Brandon Bloomer
Il campo della biologia sintetica ha avuto un grande successo nell'ingegnerizzare lieviti e batteri per produrre sostanze chimiche:biocarburanti, prodotti farmaceutici, fragranze, anche i sapori luppolati della birra, in modo più economico e sostenibile, con solo zucchero come fonte di energia.
Ancora, il campo è stato limitato dal fatto che i microbi, anche con geni generati da piante o altri animali, può fare molecole solo usando le reazioni chimiche della natura. Gran parte della chimica e dell'industria chimica si concentra sulla produzione di sostanze che non si trovano in natura con reazioni inventate in laboratorio.
Una collaborazione tra chimici sintetici e biologi sintetici presso l'Università della California, Berkeley, e Lawrence Berkeley National Laboratory ha ora superato questo ostacolo, ingegneria dei batteri che possono creare una molecola che, fino ad ora, potrebbe essere sintetizzato solo in laboratorio.
Mentre la biosintesi nei batteri E. coli ha prodotto una sostanza di basso valore e in piccole quantità, a questo, il fatto che i ricercatori possano progettare un microbo per produrre qualcosa di sconosciuto in natura apre le porte alla produzione di una gamma più ampia di sostanze chimiche dal lievito e dalla fermentazione batterica, hanno detto i ricercatori.
"È un modo completamente nuovo di fare sintesi chimica. L'idea di creare un organismo che fa un prodotto così innaturale, che combina la sintesi di laboratorio con la biologia sintetica all'interno di un organismo vivente:è solo un modo futuristico per creare molecole organiche da due campi scientifici separati in un modo che nessuno ha mai fatto prima, " ha detto John Hartwig, Professore di chimica alla UC Berkeley e uno dei quattro autori senior dello studio.
I risultati sono stati pubblicati online oggi (14 ottobre) sulla rivista Chimica della natura .
Il risultato potrebbe ampliare notevolmente le applicazioni della biologia sintetica, che è più verde, modo più sostenibile di produrre prodotti chimici per i consumatori e l'industria, ha affermato la coautrice Aindrila Mukhopadhyay, uno scienziato senior del Berkeley Lab e vicepresidente della divisione Biocarburanti e bioprodotti presso il Joint BioEnergy Institute (JBEI) di Emeryville, California.
"C'è così tanto bisogno nelle nostre vite in questo momento di materiali sostenibili, materiali che non influiscano sull'ambiente. Questa tecnologia apre possibilità per combustibili con proprietà desiderabili che possono essere prodotti in modo rinnovabile, così come nuovi antibiotici, nuovi nutraceutici, nuovi composti che sarebbero estremamente difficili da realizzare utilizzando solo la biologia o solo la chimica, " ha detto. "Penso che sia il vero potere di questo:espande la gamma di molecole che possiamo affrontare. Abbiamo davvero bisogno di nuove tecnologie dirompenti, e questo è sicuramente uno di quelli".
Ibridazione di catalizzatori metallici con enzimi naturali
Hartwig, la cattedra Henry Rapoport in chimica organica presso la UC Berkeley e uno scienziato senior della facoltà presso il Berkeley Lab, incorpora catalizzatori metallici in enzimi naturali per produrre i cosiddetti metalloenzimi artificiali, che può sintetizzare sostanze chimiche che sono state difficili da produrre con altri mezzi in laboratorio. Una reazione di questi sistemi su cui lui e il suo laboratorio hanno lavorato negli ultimi sei anni è l'incorporazione di un ciclopropano, un anello di tre atomi di carbonio, in altre molecole. Tali prodotti chimici ciclopropanati stanno diventando sempre più utili nei medicinali, come un farmaco per curare le infezioni da epatite C.
Lui e lo studente laureato alla UC Berkeley Zhennan Liu hanno creato un metalloenzima che è un ibrido di un enzima naturale, P450:ampiamente utilizzato nel corpo, soprattutto nel fegato, per ossidare i composti e il metallo iridio. P450 incorpora naturalmente un cofattore chiamato eme, anche al centro della molecola di emoglobina che trasporta l'ossigeno nel sangue, che contiene naturalmente un atomo di metallo, ferro da stiro.
Sostituendo il ferro con l'iridio, Il laboratorio di Hartwig ha generato un metalloenzima che, in provette, aggiunge con successo ciclopropani, attaccando un terzo carbonio su un doppio legame carbonio-carbonio, ad altre molecole organiche. Il metalloenzima a base di iridio fa questo con stereoselettività, cioè, genera una molecola ciclopropanata, ma non la sua immagine speculare, che si comporterebbe diversamente nel corpo.
Hanno poi collaborato con il borsista postdottorato del Berkeley Lab Jing Huang, un biologo sintetico nei laboratori di Mukhopadhyay e Jay Keasling, Professore di ingegneria chimica e biomolecolare alla UC Berkeley, scienziato senior della facoltà presso Berkeley Lab e CEO di JBEI, per vedere se potevano incorporare l'eme contenente iridio negli enzimi P450 all'interno delle cellule viventi di E. coli e dare ai batteri la capacità di produrre molecole ciclopropanate completamente all'interno della cellula.
Lavorando con lo studente laureato della UC Berkeley Brandon Bloomer, hanno trovato un modo per trasportare la molecola di eme contenente l'iridio in E. coli, dove la maggior parte dell'iridio aggiunto al mezzo in cui crescono i batteri è stato incorporato in un enzima P450.
I biologi sintetici hanno quindi bilanciato il metabolismo dei batteri in modo che potessero produrre il prodotto finale, un limonene ciclopropanato, in una coltura batterica vivente.
"Il prodotto è una molecola relativamente semplice, ma questo lavoro dimostra il potenziale per combinare la biosintesi e la sintesi chimica per creare molecole che gli organismi non hanno mai prodotto prima, e la natura non è mai stata fatta prima, "Ha detto Hartwig.
Mukhopadhyay ha affermato che l'incorporazione di altri metalloenzimi nei batteri potrebbe essere un punto di svolta in termini di produzione microbica per produrre prodotti farmaceutici, così come combustibili sostenibili.
"Oggi, molti farmaci vengono faticosamente estratti da piante difficili da coltivare e che hanno un impatto negativo sull'ambiente. Essere in grado di produrre questi composti in modo affidabile in un laboratorio utilizzando la biotecnologia risolverebbe davvero molti di questi problemi, " lei disse.
Questo vale per produrre "non solo medicinali, ma precursori di polimeri, plastiche rinnovabili, biocarburanti, materiali da costruzione, l'intera gamma di cose che usiamo oggi, dai detersivi ai lubrificanti alle vernici ai pigmenti ai tessuti, " ha aggiunto. "Tutto può essere fatto biologicamente. Ma la sfida sta nello sviluppo di percorsi rinnovabili sostenibili per raggiungerlo. E così qui, abbiamo fatto un passo abbastanza sostanziale verso di esso, dove siamo stati in grado di dimostrare una chimica artificiale all'interno di una cellula, una cellula viva in coltura, che è intrinsecamente quindi scalabile."
Hartwig è d'accordo.
"La visione più ampia è essere in grado di creare organismi che creeranno prodotti innaturali che combinino la chimica della natura con la chimica di laboratorio, "Ha detto Hartwig. "Ma la chimica di laboratorio si verificherebbe ora all'interno della cellula. Se potessimo farlo in modo generale, potremmo progettare organismi per produrre tutti i tipi di farmaci, prodotti agrochimici e persino prodotti chimici di base, come i monomeri per i polimeri, che trarrebbero vantaggio dall'efficienza e dalla selettività della fermentazione e della biocatalisi."