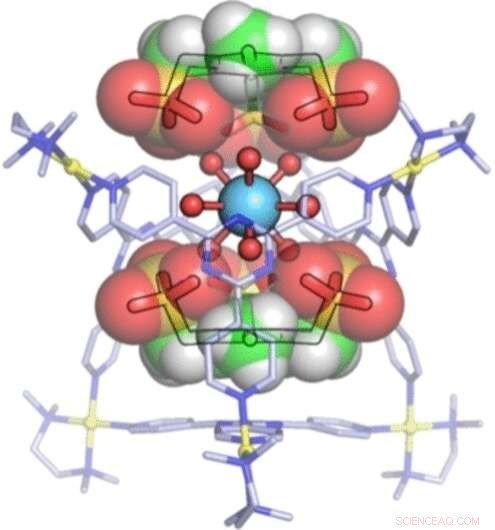
Credito:Wiley
I metalli delle terre rare sono indispensabili per molti prodotti tecnici, da smartphone, laptop, batterie, motori elettrici e turbine eoliche, ai catalizzatori. Nel diario Angewandte Chemie , un team giapponese ha ora introdotto una "gabbia" molecolare con "cappucci" che può essere utilizzata per "confinare" selettivamente alcuni ioni di metalli delle terre rare per l'isolamento o il riciclaggio.
Gli elementi delle terre rare includono 17 metalli:scandio, ittrio, lantanio e lantanidi, i 14 elementi che seguono il lantanio nella tavola periodica, inclusi neodimio ed europio. Il nome è fuorviante perché i metalli delle terre rare non sono in realtà rari. Sono ovunque nell'ambiente ma sono altamente dispersi e legati in minerali ("terre"); i grandi depositi sono rari. Il recupero di questi elementi dai rifiuti elettronici sta diventando sempre più importante. Sono stati scoperti alcuni microrganismi che contengono enzimi con metalli delle terre rare. Questi potrebbero essere utili nell'estrazione e nel recupero e fornire ispirazione per l'uso dei metalli delle terre rare come catalizzatori.
Gli ioni di metalli delle terre rare si trovano anche nei corpi idrici e negli effluenti. Tuttavia, sono difficili da separare individualmente dalle soluzioni acquose. Uno dei motivi è che di solito sono idratati, il che significa che sono legati alle molecole d'acqua. I loro stati di idratazione sono diversi e possono cambiare. Ciò rende più difficile l'identificazione e l'isolamento degli ioni attraverso il legame ai ligandi.
Un team guidato da Makoto Fujita dell'Università di Tokyo e dell'Institute for Molecular Science è ora riuscito a "confinare" le forme idratate di ioni trivalenti di una serie di metalli delle terre rare in "gabbie" chiuse. Ogni molecola di gabbia è costituita da quattro ligandi organici a forma di "piastre" triangolari che sono collegate dalle loro punte a sei ioni di palladio per formare una gabbia ottaedrica con due grandi aperture. Lo ione metallo delle terre rare si inserisce nella gabbia con le sue nove molecole d'acqua legate. La caratteristica fondamentale della gabbia sono i suoi due "tappi" che coprono le aperture. Si tratta di molecole planari con tre bracci di legame caricati negativamente che si legano alle molecole d'acqua dello ione metallico delle terre rare attraverso ponti di idrogeno. Inoltre, sono tenuti stretti dalle interazioni elettrostatiche con gli ioni palladio caricati positivamente nella gabbia.
Non tutti gli ioni di metalli delle terre rare vengono catturati ugualmente bene da questo sistema. Sottili differenze nei loro raggi e nelle modalità di idratazione preferite determinano quanto bene si adattano alle gabbie:il lantanio e i primi lantanidi, come l'europio, sono legati in modo significativamente più forte rispetto ai successivi lantanidi, come l'itterbio. Lo scandio, ad esempio, ha solo sei molecole d'acqua legate ad esso e non riesce a trovare una posizione stabile all'interno della gabbia. È quindi a malapena tenuto in posizione.
Il confinamento di specie metalliche idrofile in una cavità chiusa potrebbe essere un approccio per l'isolamento dei metalli delle terre rare, nonché per lo sviluppo di nuovi catalizzatori analoghi agli enzimi contenenti metalli (metallozimi) nei microrganismi. + Esplora ulteriormente