I ricercatori della Rice University hanno introdotto blocchi di aminoacidi non canonici nelle proteine delle cellule viventi, pioniere di un potente strumento per studiare e manipolare la struttura e la funzione delle proteine. Il risultante organismo innaturale, un ceppo di batteri Escherichia coli, è in grado di monitorare bassi livelli di stress ossidativo. Credito:Xiao Lab/Rice University
Il chimico della Rice University Han Xiao e il suo team hanno ampliato con successo il codice genetico dei batteri Escherichia coli per produrre un blocco di costruzione sintetico, un "aminoacido non canonico". Il risultato è un indicatore vivente dello stress ossidativo.
Il lavoro, dicono, è un passo verso le tecnologie che consentiranno la generazione di nuove proteine e organismi con una varietà di funzioni utili.
Il loro studio appare sulla rivista Cell Press chimica .
Gli amminoacidi sono gli elementi costitutivi del DNA. Generalmente, gli organismi hanno bisogno solo di 20 di loro per programmare l'intero set di proteine necessarie per la vita. Ma Xiao, con l'aiuto di una sovvenzione del National Institutes of Health di 1,8 milioni di dollari, ha deciso di vedere come un 21° amminoacido consentirebbe la progettazione di "organismi innaturali" che servono a scopi specifici.
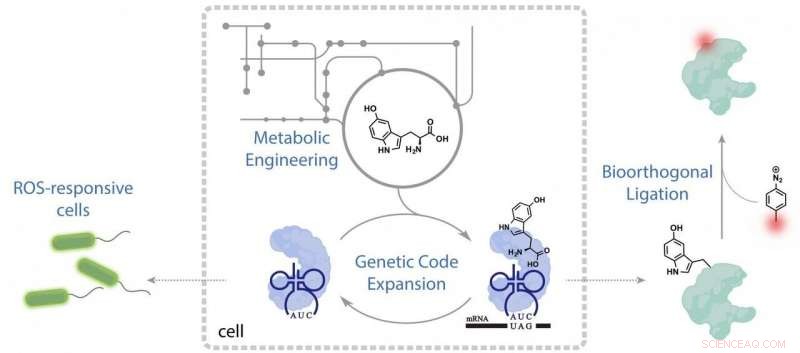
Il nuovo studio fa proprio questo ingegnerizzando i batteri per produrre l'aminoacido extra, chiamato 5-idrossi-triptofano (5HTP), che appare naturalmente nell'uomo come precursore del neurotrasmettitore serotonina, ma non in E. coli. La nuova produzione di 5HTP spinge i batteri a produrre una proteina che emette fluorescenza quando l'organismo è sotto stress metabolico.
"Il processo richiede molte tecniche interdisciplinari, " Xiao ha detto. "In questo studio, abbiamo combinato chimica sintetica, biologia sintetica e ingegneria metabolica per creare un ceppo che sintetizza e codifica un 21° amminoacido non canonico, e poi lo usa per produrre la proteina desiderata."
Xiao ha affermato che la programmazione dei batteri innaturali autonomi era un processo in tre fasi:in primo luogo, i ricercatori guidati dallo studente laureato Yuda Chen hanno creato un macchinario traslazionale bioortogonale per l'aminoacido, 5HTP. Secondo, hanno trovato e preso di mira un codone vuoto, una sequenza di DNA o RNA che non produce una proteina, e lo hanno modificato geneticamente per codificare 5HTP. Terzo, innestando cluster enzimatici di altre specie in E. coli, hanno dato ai batteri la capacità di produrre 5HTP.
"Queste proteine contenenti 5HTP, isolato dai batteri programmati, possono essere ulteriormente etichettati con farmaci o altre molecole, " disse Xiao. "Ecco, mostriamo che il ceppo stesso può fungere da indicatore vivente per le specie reattive dell'ossigeno, e il limite di rilevamento è davvero basso."
Mentre i ricercatori hanno segnalato la creazione di oltre 200 amminoacidi non canonici fino ad oggi, la maggior parte di essi non può essere sintetizzata dai loro organismi ospiti. "Questo è un campo in corso da decenni, ma in precedenza le persone si concentravano sulla parte chimica, " Xiao ha detto. "La nostra visione è quella di progettare cellule intere con il 21° amminoacido che ci permetterà di indagare su problemi biologici o medici negli organismi viventi, piuttosto che trattare solo con le cellule in laboratorio.
"Spostare questa tecnologia sulla specie ospite elimina la necessità di iniettare blocchi artificiali in un organismo, perché possono sintetizzarlo e usarlo da soli, " ha detto. "Questo ci permette di studiare gli amminoacidi non canonici a un livello superiore, livello dell'intero organismo."
In definitiva, i ricercatori sperano che i blocchi di costruzione personalizzati consentiranno alle cellule mirate, come quelli nei tumori, per produrre i propri farmaci terapeutici. "Questa è un'importante direzione futura per il mio laboratorio, " Xiao ha detto. "Vogliamo che le cellule rilevino la malattia, produrre farmaci migliori e rilasciarli in tempo reale. Non pensiamo che sia troppo lontano".
I coautori del documento sono i borsisti post-dottorato di Rice Juan Tang, Lushun Wang e Zeru Tian, lo studente universitario Adam Cardenas e lo studioso in visita Xinlei Fang, e Abhishek Chatterjee, un assistente professore di chimica al Boston College. Xiao è il giovane investigatore Norman Hackerman-Welch e assistente professore di chimica.