Anche se sembra che viviamo in un mondo di abbondanza, dietro le quinte reperire quantità sufficienti di ingredienti chiave può essere una sfida. Ad esempio, la sintesi di alcuni antibiotici, gli antibiotici beta-lattamici, richiede determinate molecole in grandi quantità e, storicamente, ottenerne una quantità sufficiente è stato difficile.
In uno studio, intitolato "Sintesi catalitica di derivati β-lattamici mediante cicloaddizione carbonilativa di acilsilani con immine tramite un intermedio di Fischer-carbene di palladio" e pubblicato su Nature Catalysis , i ricercatori dell'Università di Osaka svelano un nuovo modo semplificato per sintetizzare l'intricata impalcatura beta-lattamica caratteristica degli antibiotici beta-lattamici.
La penicillina, il primo antibiotico prodotto in serie, è un esempio di antibiotico beta-lattamico. Questi antibiotici rappresentano la prima scelta per alcune infezioni batteriche perché sono più selettivi e meno tossici della maggior parte dei farmaci. Non sorprende che esistano dozzine di antibiotici beta-lattamici approvati per uso clinico e in fase di sviluppo.
Sfortunatamente, sintetizzare questi antibiotici in laboratorio è stato impegnativo a causa della loro struttura piccola ma complessa. Pertanto, i catalizzatori sono generalmente necessari per facilitare i passaggi critici durante la sintesi. Un catalizzatore, noto come complesso Fischer-carbene, funziona bene ma deve essere utilizzato in grandi quantità. La sintesi di un catalizzatore Fischer-carbene che funziona in piccole quantità era l'obiettivo dello studio del gruppo di ricerca.
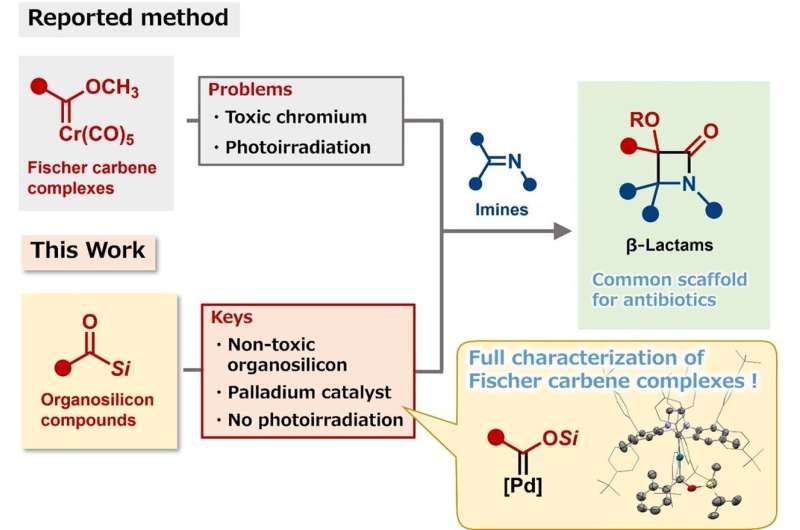
"Il nostro nuovo sistema catalitico può generare complessi Fischer-carbene da composti di organosilicio, che non sono tossici", spiega Tetsuya Inagaki, autore principale dello studio. "Inoltre, siamo stati in grado di isolare e caratterizzare un intermedio chiave:un complesso silossicarbene-palladio."
A differenza dei precedenti protocolli sintetici Fischer-carbene, il processo non produce rifiuti tossici di cromo e non richiede fotoirradiazione. La reazione procede in un solo passaggio, è operativamente semplice e richiede solo una piccola quantità di catalizzatore. I ricercatori lo hanno utilizzato per preparare l'impalcatura dell'antibiotico tienamicina con una resa del 94%.
"Siamo entusiasti perché la nostra ricerca aiuterà a sintetizzare catalizzatori Fischer-carbene che altrimenti sarebbero difficili da isolare e fornirà l'accesso a elementi costitutivi beta-lattamici strutturalmente complicati in un recipiente di reazione", afferma Mamoru Tobisu, autore senior. "Non vediamo l'ora di applicare il nostro protocollo di reazione ad altre classi di bersagli sintetici."
Questo lavoro rappresenta un importante passo avanti nella semplificazione della sintesi dei beta-lattamici, l’impalcatura molecolare più comune degli antibiotici. Poiché il protocollo sintetico è semplice e minimamente tossico, le applicazioni per ulteriori trasformazioni chimiche dovrebbero essere semplici.
Ulteriori informazioni: Tetsuya Inagaki et al, Sintesi catalitica di derivati β-lattamici mediante cicloaddizione carbonilativa di acilsilani con immine tramite un intermedio Fischer-carbene di palladio, Nature Catalysis (2024). DOI:10.1038/s41929-023-01081-5
Informazioni sul giornale: Catalisi della natura
Fornito dall'Università di Osaka