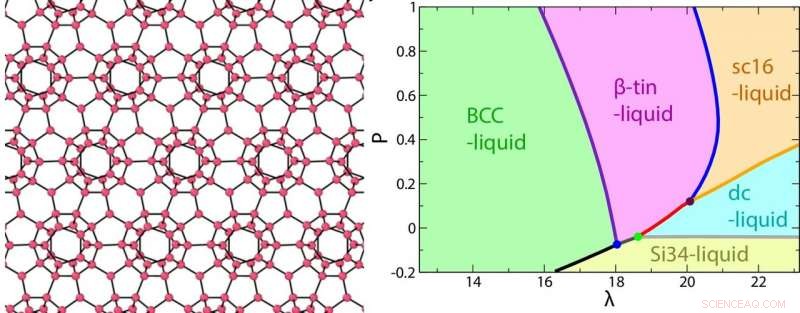
Un'immagine della struttura clatratica (Si34) di un liquido di tipo acquoso formato a pressione negativa (a sinistra) e il diagramma di fase in funzione della forza della tetraedralità λ e della pressione P. Credito:2018 Hajime Tanaka, Istituto di Scienze Industriali, L'Università di Tokyo
Un team di ricerca con sede in Giappone ha studiato il comportamento anomalo dei liquidi tetraedrici come l'acqua. Tramite simulazione al computer, hanno calcolato i diagrammi di fase di una gamma di liquidi modello. Variando un parametro chiamato lambda (λ), che controlla la quantità di struttura tetraedrica nel liquido, hanno scoperto che i liquidi con maggiore λ mostravano più anomalie, come l'espansione a bassa temperatura. Il valore dell'acqua di massimizza l'effetto della tetraedralità, da qui le sue proprietà particolarmente insolite.
L'acqua occupa un posto speciale tra i liquidi per le sue proprietà insolite, e rimane poco compreso. Per esempio, si espande solo al gelo in ghiaccio, e diventa meno viscoso sotto compressione, intorno alla pressione atmosferica. Razionalizzare queste stranezze è una grande sfida per la fisica e la chimica. Una recente ricerca condotta dall'Istituto di scienze industriali (IIS) dell'Università di Tokyo suggerisce che derivino dal grado di ordinamento strutturale nel fluido.
L'acqua appartiene a una classe di liquidi le cui particelle formano strutture tetraedriche locali. La tetraedralità dell'acqua è una conseguenza dei legami idrogeno tra le molecole, che sono vincolati a direzioni fisse. In uno studio in Atti dell'Accademia Nazionale delle Scienze ( PNAS ), i ricercatori hanno studiato il motivo per cui le proprietà fisiche dell'acqua espresse dal suo diagramma di fase sono così notevoli, anche rispetto ad altri liquidi tetraedrici, come silicio e carbonio.
I liquidi tetraedrici sono spesso simulati da un potenziale energetico chiamato modello SW. Si presume che il liquido contenga due fasi in equilibrio termodinamico:uno stato disordinato con un'elevata simmetria rotazionale, e uno stato ordinato tetraedricamente che non lo fa. Nonostante la sua semplicità, il modello prevede con precisione comportamenti liquidi anomali. La proprietà a due stati è controllata dal parametro lambda (λ), che descrive la forza relativa delle interazioni intermolecolari a coppie ea tre corpi. Più alto è λ, il grado di ordine tetraedrico aumenta.
"Ci siamo resi conto che λ, che è piuttosto grande per l'acqua, è stata la chiave dell'unicità di questi liquidi, ", afferma il co-autore dello studio John Russo. "Effettivamente, λ controlla il grado di tetraedralità:all'aumentare di λ, i gusci tetraedrici che si formano attorno a ciascuna molecola diventano energeticamente più stabili. Quindi, questi gusci superano la sfavorevole perdita di entropia che accompagna la creazione dell'ordine." I tetraedri locali assomigliano a strutture allo stato solido, ecco perché i liquidi ad alto cristallizzano più facilmente.
Regolando continuamente λ, hanno simulato una serie di diagrammi di fase per modellare cosa succede quando un liquido "semplice" diventa progressivamente più simile all'acqua. Con l'aumento di , le varie anomalie termodinamiche e dinamiche dei liquidi tetraedrici - come l'espansione a bassa temperatura e la rottura della legge standard di Arrhenius per la diffusione - divennero più pronunciate.
Però, non era così semplice come "più tetraedri equivale a un comportamento più strano". L'influenza della tetraedralità è stata massimizzata per l'acqua, che ha λ =23,15. qui sopra, il comportamento della densità in funzione della temperatura è tornato alla normalità, perché la differenza di volume tra stati ordinati e disordinati cominciava a diminuire. Così, l'acqua ha un valore squisitamente messo a punto o "Riccioli d'oro" di che le consente di spostarsi facilmente tra l'ordine e la casualità. Ciò gli conferisce un'elevata flessibilità strutturale in risposta a variazioni di temperatura o pressione, che è l'origine del suo comportamento unico.
"Collegamento di proprietà osservabili, come la viscosità alle strutture microscopiche, è ciò che riguarda la chimica fisica, ", afferma il co-autore Hajime Tanaka. "Acqua, la sostanza più abbondante e tuttavia più insolita sulla terra, è stata a lungo l'ultima frontiera in questo senso. Siamo stati lieti che un semplice, modello ben noto può spiegare pienamente la stranezza dell'acqua, che nasce dal delicato equilibrio tra ordine e disordine nel liquido."