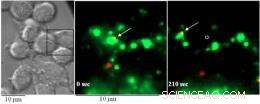
Nanoparticelle (mostrate in rosso) co-localizzate e spostate con Scavenger Receptor A (verde), suggerendo che questo recettore può svolgere un ruolo nel mediare l'interazione e il destino di queste particelle in determinate cellule.
Le nanoparticelle promettono di risolvere una serie di problemi, dall'individuazione di diagnosi mediche allo sviluppo di forme alternative di energia e alla creazione di materiali più durevoli. Ma gli scienziati devono ancora determinare esattamente come interagiscono queste minuscole particelle nel loro ambiente, sia all'interno degli esseri umani che nel mondo in generale, e se tali interazioni possono essere tossiche.
In un recente studio, gli scienziati del Pacific Northwest National Laboratory hanno scoperto interazioni cellulari di nanoparticelle a livello molecolare che possono portare a risposte su come queste particelle influiscono sui sistemi viventi. I loro risultati appariranno sulla rivista nanotossicologia .
Man mano che gli scienziati iniziano a comprendere i meccanismi e le molecole che influenzano le interazioni cellulari delle nanoparticelle dotate di proprietà fisiche e chimiche specifiche, possono prevedere meglio l'impatto delle nanoparticelle sui sistemi biologici.
Con una maggiore comprensione delle interazioni cellulari e della risposta alle nanoparticelle, le agenzie governative e le associazioni scientifiche possono stabilire standard realistici su come utilizzare queste particelle, salvaguardare la salute umana e l'ambiente accelerando le innovazioni nel campo dell'energia, medicinale, e scienze dei materiali.
I ricercatori si sono concentrati sull'identificazione dei meccanismi sottostanti che regolano il modo in cui le nanoparticelle con proprietà specifiche interagiscono con le cellule. Utilizzando la microscopia a fluorescenza ad alta sensibilità time-lapse presso EMSL, una struttura per utenti scientifici del Dipartimento dell'Energia al PNNL, il team ha studiato le nanoparticelle di silice amorfa nei macrofagi, parte del sistema immunitario umano.
Il microscopio ad alta sensibilità ha permesso loro di tracciare le singole nanoparticelle in tempo reale mentre la particella entrava in una cellula, come ha interagito all'interno della cellula viva, e il suo destino. Hanno scoperto che le nanoparticelle tendevano a muoversi insieme a una particolare proteina dei macrofagi, Recettore spazzino A, nella cella.
Quando il recettore era espresso in cellule che normalmente non esprimono questa proteina, le cellule si sono associate a più nanoparticelle. Quando l'espressione del recettore è stata inibita nei macrofagi, le cellule si sono associate a un numero inferiore di nanoparticelle. Però, la mediazione del recettore era principalmente associata a singole nanoparticelle. Quando le nanoparticelle si sono agglomerate e sono diventate una massa più grande, come tendono a fare, solo una frazione più piccola è stata trovata associata al recettore.