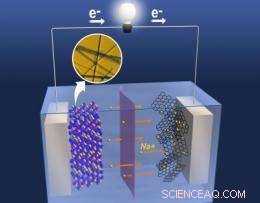
La nanostruttura uniforme dell'ossido di manganese trattato termicamente fornisce tunnel per il flusso di ioni sodio, migliorare le prestazioni degli elettrodi. Attestazione:PNNL
(PhysOrg.com) -- Aggiungendo la giusta quantità di calore, i ricercatori hanno sviluppato un metodo che migliora la capacità elettrica e la durata di ricarica delle batterie ricaricabili agli ioni di sodio, che potrebbe essere un'alternativa più economica per usi su larga scala come lo stoccaggio di energia sulla rete elettrica.
Per collegare le fonti di energia solare ed eolica alla rete elettrica, i gestori di rete richiedono batterie in grado di immagazzinare grandi quantità di energia creata alla fonte. Le batterie ricaricabili agli ioni di litio, comuni nell'elettronica di consumo e nei veicoli elettrici, si comportano bene, ma sono troppo costosi per un uso diffuso sulla rete perché saranno necessarie molte batterie, e probabilmente dovranno essere grandi. Il sodio è la scelta migliore, ma le batterie sodio-zolfo attualmente in uso funzionano a temperature superiori a 300 gradi Celsius, o tre volte la temperatura dell'acqua bollente, rendendoli meno efficienti dal punto di vista energetico e sicuri rispetto alle batterie che funzionano a temperatura ambiente.
Gli sviluppatori di batterie vogliono il meglio di entrambi i mondi:utilizzare sia il sodio economico che il tipo di elettrodi che si trovano nelle ricaricabili al litio. Un team di scienziati del Pacific Northwest National Laboratory del Department of Energy e ricercatori in visita dall'Università di Wuhan a Wuhan, La Cina ha utilizzato nanomateriali per realizzare elettrodi in grado di funzionare con il sodio, hanno riportato online il 3 giugno sulla rivista Materiale avanzato .
"La batteria agli ioni di sodio funziona a temperatura ambiente e utilizza ioni di sodio, un ingrediente nel sale da cucina. Quindi sarà molto più economico e sicuro, " ha detto il chimico del PNNL Jun Liu, che ha co-diretto lo studio con il chimico dell'Università di Wuhan Yuliang Cao.
Gli elettrodi nelle ricaricabili al litio che interessano i ricercatori sono fatti di ossido di manganese. Gli atomi in questo ossido metallico formano molti fori e tunnel attraverso i quali gli ioni di litio viaggiano quando le batterie vengono caricate o sono in uso. Il libero movimento degli ioni di litio consente alla batteria di trattenere l'elettricità o rilasciarla in una corrente. Ma sostituire semplicemente gli ioni di litio con ioni di sodio è problematico:gli ioni di sodio sono il 70% più grandi degli ioni di litio e non si adattano anche alle fessure.
Per trovare un modo per fare buchi più grandi nell'ossido di manganese, I ricercatori del PNNL sono andati molto molto più piccoli. Si sono rivolti ai nanomateriali:materiali realizzati su scala nanometrica, o circa un milione di volte più sottili di un centesimo, che hanno proprietà sorprendenti a causa della loro piccolezza. Per esempio, le brevi distanze che gli ioni di sodio devono percorrere nei nanofili potrebbero rendere l'ossido di manganese un elettrodo migliore in modi non correlati alle dimensioni dei tunnel..
Esplorare, il team ha mescolato due diversi tipi di blocchi atomici di ossido di manganese:uno i cui atomi si dispongono in piramidi, e un altro i cui atomi formano un ottaedro, una struttura a forma di diamante da due piramidi attaccate insieme alle loro basi. Si aspettavano che il materiale finale avesse grandi tunnel a forma di S e tunnel a cinque lati più piccoli attraverso i quali gli ioni potessero fluire.
Dopo aver mescolato, il team ha trattato i materiali con temperature comprese tra 450 e 900 gradi Celsius, quindi ha esaminato i materiali e testato quale trattamento ha funzionato meglio. Utilizzando un microscopio elettronico a scansione, il team ha scoperto che temperature diverse creano materiale di qualità diversa. Trattare l'ossido di manganese a 750 gradi Celsius ha creato i migliori cristalli:troppo bassi e i cristalli apparivano sfaldati, troppo in alto e i cristalli si trasformavano in piatti piatti più grandi.
Zoomando ancora di più usando un microscopio elettronico a trasmissione all'EMSL, Laboratorio di scienze molecolari ambientali del DOE nel campus del PNNL, il team ha visto che l'ossido di manganese riscaldato a 600 gradi aveva dei butteri nei nanofili che potevano impedire agli ioni di sodio, ma i fili trattati a 750 gradi sembravano uniformi e molto cristallini.
Ma anche il materiale più bello è solo una vetrina se non funziona bene. Per scoprire se è all'altezza del suo bell'aspetto, il team PNNL-Wuhan ha immerso il materiale dell'elettrodo nell'elettrolita, il liquido contenente ioni sodio che aiuterà gli elettrodi di ossido di manganese a formare una corrente. Quindi hanno caricato e scaricato ripetutamente le celle della batteria sperimentale.
Il team ha misurato la capacità di picco a 128 milliAmp ore per grammo di materiale per elettrodi quando la cella della batteria sperimentale si è scaricata. Questo risultato ha superato quelli precedenti ottenuti da altri ricercatori, uno dei quali ha raggiunto una capacità di picco di 80 milliAmp ore per grammo per elettrodi realizzati con ossido di manganese ma con un metodo di produzione diverso. I ricercatori pensano che la capacità inferiore sia dovuta agli ioni sodio che causano cambiamenti strutturali in quell'ossido di manganese che non si verificano o si verificano meno frequentemente nel materiale di dimensioni nanometriche trattato termicamente.
Oltre all'elevata capacità, il materiale ha retto bene ai cicli di carica e scarica, come accadrebbe nell'uso da parte dei consumatori. Ancora, il materiale trattato a 750 gradi centigradi si è comportato al meglio:dopo 100 cicli di carica-scarica, ha perso solo il 7% della sua capacità. Il materiale trattato a 600 Celsius o 900 Celsius ha perso circa il 37 percento e il 25 percento, rispettivamente.
Anche dopo 1, 000 cicli, la capacità degli elettrodi trattati con 750 gradi Celsius è diminuita solo del 23 percento circa. I ricercatori pensavano che il materiale avesse funzionato molto bene, mantenendo il 77% della sua capacità iniziale.
Scorso, il team ha caricato la cella sperimentale a velocità diverse per determinare quanto velocemente potrebbe assorbire elettricità. Il team ha scoperto che più velocemente lo caricavano, meno elettricità potrebbe contenere. Ciò ha suggerito al team che la velocità con cui gli ioni sodio potevano diffondersi nell'ossido di manganese limitava la capacità della cella della batteria:quando caricata velocemente, gli ioni sodio non potevano entrare nei tunnel abbastanza velocemente da riempirli.
Per compensare gli ioni sodio lenti, i ricercatori suggeriscono in futuro di realizzare nanofili ancora più piccoli per accelerare la carica e la scarica. Le batterie della rete necessitano di una ricarica rapida in modo da poter raccogliere quanta più energia prodotta da fonti rinnovabili possibile. E devono scaricarsi velocemente quando le richieste aumentano mentre i consumatori accendono i condizionatori e i televisori, e collegare i loro veicoli elettrici a casa.
Tali batterie ad alte prestazioni potrebbero togliere il calore da una rete elettrica già tassata.