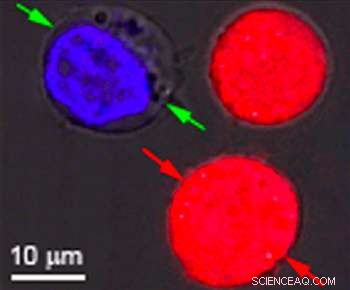
Cellule identiche colorate di rosso e blu sono state l'obiettivo della ricerca presso la Rice University per mostrare l'effetto delle nanobolle plasmoniche. Le bolle si formano attorno a nanoparticelle d'oro riscaldate che prendono di mira particolari cellule, come le cellule cancerose. Quando le particelle sono vuote, si formano bolle abbastanza grandi da uccidere la cellula quando scoppiano. Quando le particelle sono solide, le bolle sono più piccole e possono perforare un foro temporaneo in una parete cellulare, consentendo l'ingresso di farmaci o altro materiale. Entrambi gli effetti possono essere ottenuti contemporaneamente con un singolo impulso laser. Credito:Plasmonic Nanobubble Lab/Rice University
(Phys.org)—I ricercatori della Rice University hanno trovato un modo per uccidere alcune cellule malate e curarne altre nello stesso campione allo stesso tempo. Il processo attivato da un impulso di luce laser lascia intatte le cellule sane vicine.
L'uso esclusivo delle nanobolle plasmoniche sintonizzabili sviluppate nel laboratorio Rice di Dmitri Lapotko promette di sostituire diversi processi difficili ora utilizzati per curare i malati di cancro, tra gli altri, con un veloce, semplice, procedura multifunzionale.
La ricerca è al centro di un articolo pubblicato online questa settimana dalla rivista dell'American Chemical Society ACS Nano ed è stata eseguita a Rice da Lapotko, ricercatrice e autrice principale Ekaterina Lukianova-Hleb e lo studente universitario Martin Matonga, con l'assistenza del Centro per la terapia cellulare e genica del Baylor College of Medicine (BCM), Texas Children's Hospital e l'Università del Texas MD Anderson Cancer Center.
Nanobolle plasmoniche che sono 10, 000 volte più piccolo di un capello umano causa minuscole esplosioni. Le bolle si formano attorno alle nanoparticelle d'oro plasmoniche che si riscaldano quando eccitate da una fonte di energia esterna - in questo caso, un breve impulso laser e vaporizza un sottile strato di liquido vicino alla superficie della particella. La bolla di vapore si espande e collassa rapidamente. Lapotko e i suoi colleghi avevano già scoperto che le nanobolle plasmoniche uccidono le cellule tumorali facendole letteralmente esplodere senza danneggiare i vicini sani, un processo che ha mostrato precisione e selettività molto più elevate rispetto a quelli mediati dalle sole nanoparticelle d'oro, Egli ha detto.
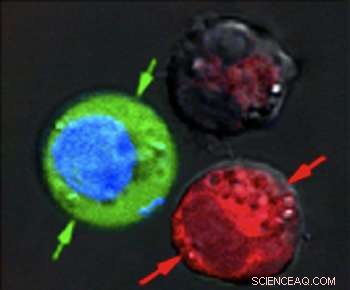
Dopo l'impulso laser, le cellule rosse mostrano segni di danni massicci dovuti all'esplosione di nanobolle, mentre le cellule colorate di blu sono rimaste intatte, ma con colorante fluorescente verde tirato dentro dall'esterno. Credito:Plasmonic Nanobubble Lab/Rice University
Il nuovo progetto porta questa straordinaria capacità a qualche passo in più. Una serie di esperimenti ha dimostrato che un singolo impulso laser crea grandi nanobolle plasmoniche attorno a nanogusci d'oro cavi, e queste grandi nanobolle distruggono selettivamente le cellule indesiderate. Lo stesso impulso laser crea nanobolle più piccole attorno a nanosfere d'oro massiccio che colpiscono un minuscolo, poro temporaneo nella parete di una cellula e creano un nanogetto in entrata che "inietta" rapidamente farmaci o geni nelle altre cellule.
Nei loro esperimenti, Lapotko e il suo team hanno posizionato nanogusci cavi larghi 60 nanometri in cellule tumorali modello e le hanno colorate di rosso. In un lotto separato, hanno messo nanosfere larghe 60 nanometri nello stesso tipo di cellule e le hanno colorate di blu.
Dopo aver sospeso le cellule insieme in un colorante fluorescente verde, hanno sparato un singolo ampio impulso laser sul campione combinato, lavato via la macchia verde e controllato le cellule al microscopio. I globuli rossi con i nanogusci cavi sono stati fatti saltare in aria da grandi nanobolle plasmoniche. Le cellule blu erano intatte, ma il liquido macchiato di verde dall'esterno era stato trascinato nelle cellule dove nanobolle plasmoniche più piccole attorno alle nanoparticelle d'oro solido hanno temporaneamente aperto le pareti.
Perché tutto questo avviene in una frazione di secondo, fino a 10 miliardi di celle al minuto potrebbero essere processate selettivamente in un sistema a flusso continuo come quello in fase di sviluppo alla Rice, disse Lapotko, un collega di facoltà in biochimica e biologia cellulare e in fisica e astronomia. Questo ha il potenziale per far progredire la terapia cellulare e genica e il trapianto di midollo osseo, Egli ha detto.
La maggior parte delle terapie cellulari e geniche che combattono le malattie richiedono "ex vivo" - al di fuori del corpo - l'elaborazione di innesti di cellule umane per eliminare le cellule indesiderate (come quelle cancerose) e per modificare geneticamente altre cellule per aumentare la loro efficienza terapeutica, disse Lapotko. "L'attuale elaborazione delle celle è spesso lenta, costoso e ad alta intensità di lavoro e soffre di elevate perdite di celle e scarsa selettività. Idealmente sia l'eliminazione che la trasfezione (l'introduzione di materiali nelle cellule) dovrebbero essere altamente efficienti, selettivo, veloce e sicuro."
La tecnologia delle nanobolle plasmoniche promette "un metodo per fare più cose contemporaneamente su una popolazione cellulare, " disse Malcolm Brenner, professore di medicina e pediatria alla BCM e direttore del Centro di terapia cellulare e genica della BCM, che collabora con il team Rice. "Per esempio, se voglio mettere qualcosa in una cellula staminale per farla trasformare in un altro tipo di cellula, e allo stesso tempo uccidono le cellule circostanti che hanno il potenziale per fare del male quando tornano in un paziente, o in un altro paziente, queste nanobolle plasmoniche molto sintonizzabili hanno il potenziale per farlo".
L'obiettivo a lungo termine di uno sforzo collaborativo tra Rice, BCM, Texas Children's Hospital e MD Anderson è quello di migliorare l'esito per i pazienti con malattie il cui trattamento richiede l'elaborazione cellulare ex vivo, disse Lapotko.
Lapotko prevede di costruire un prototipo della tecnologia con l'obiettivo di testare le cellule umane nel prossimo futuro. "Vorremmo che questa fosse una piattaforma universale per la terapia cellulare e genica e per il trapianto di cellule staminali, " Egli ha detto.