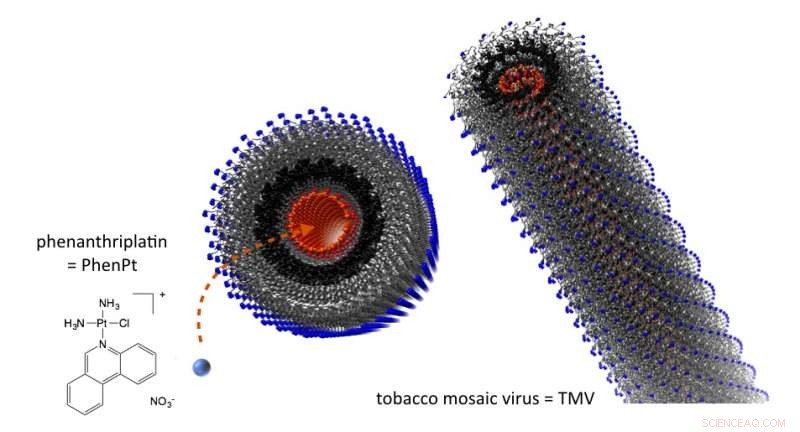
Quando confezionato all'interno di nanoparticelle di virus del mosaico del tabacco, il fenantriplatino viene somministrato ai tumori, dove si è dimostrato più efficace in vivo di un platino approvato. Credito:Case Western Reserve University
In un paio di primati, i ricercatori della Case Western Reserve University e del Massachusetts Institute of Technology hanno dimostrato che il fenantriplatino candidato al farmaco può essere più efficace di un farmaco approvato in vivo, e che un vettore a base di virus vegetali fornisce con successo un farmaco in vivo.
I tumori del cancro al seno triplo negativo dei topi trattati con le nanoparticelle che trasportano fenantriplatino erano quattro volte più piccoli di quelli trattati con cisplatino, un farmaco chemioterapico comune e correlato, o fenantriplatino libero iniettato per via endovenosa in circolo.
Gli scienziati credono che il lavoro, riportato sul giornale ACS Nano , è un passo promettente verso gli studi clinici.
"Potremmo aver trovato il vettore perfetto per questo particolare farmaco candidato, " ha detto Nicole Steinmetz, un assistente professore di ingegneria biomedica alla Case Western Reserve, che ha trascorso 10 anni a studiare l'uso dei virus delle piante per scopi medici.
Ha collaborato con Stephen J. Lippard, Arthur Amos Noyes Professore di chimica al MIT, e un esperto in interazioni biologiche che coinvolgono chemioterapie a base di platino.
I farmaci a base di platino sono usati per trattare più della metà dei malati di cancro sottoposti a chemioterapia. Due dei farmaci più comunemente usati sono il cisplatino e il carboplatino. Formano legami incrociati bifunzionali con il DNA nelle cellule tumorali, che impediscono al DNA di trascrivere i geni e provocano la morte cellulare, Spiegò Lippard.
Nonostante l'uso diffuso, è stato dimostrato che il cisplatino cura solo il cancro ai testicoli, e molti tumori hanno o sviluppano immunità al farmaco.
Il laboratorio di Lippard ha alterato il cisplatino sostituendo uno ione cloruro con la fenantridina e ha scoperto che la nuova molecola si lega anche al DNA. Invece di formare legami incrociati, però, il fenantriplatino si lega a un singolo sito ma blocca ancora la trascrizione.
Infatti, il suo laboratorio ha scoperto che il fenantriplatino è fino a 40 volte più potente dei platini tradizionali quando testato direttamente contro le cellule tumorali del polmone, Seno, ossa e altri tessuti. La molecola sembra anche evitare meccanismi di difesa che trasmettono resistenza.
Ma quando iniettato in modelli murini di cancro, il candidato al farmaco non ha avuto risultati migliori dei platini standard.
Lippard si rese conto che il fenantriplatino non stava raggiungendo il suo obiettivo. Aveva un problema con la consegna della droga.
Ha trovato una potenziale soluzione mentre visitava il campus della Case Western Reserve e ha sentito Steinmetz spiegare il suo lavoro sulle indagini sul virus del mosaico del tabacco (TMV) per la somministrazione di farmaci più di un anno fa.
"Ho immaginato che TMV sarebbe stato il veicolo perfetto, " Ha detto Lippard. "Così abbiamo bevuto una birra e abbiamo formato una collaborazione".
Il lungo, le nanoparticelle sottili del virus del mosaico del tabacco sono naturali per la somministrazione del candidato farmaco nei tumori, detto Steinmetz, nominato dalla Case Western Reserve School of Medicine.
Le particelle virali, che non infetterà gli umani, sono vuote. Un tubo centrale di circa 4 nanometri di diametro percorre la lunghezza del guscio e il rivestimento porta una carica negativa.
Il fenantriplatino ha un diametro di circa 1 nanometro e, se trattato con nitrato d'argento, ha una forte carica positiva. Entra facilmente e si lega al rivestimento centrale.
La forma allungata della nanoparticella la fa rotolare lungo i margini dei vasi sanguigni, rimangono inosservati dalle cellule immunitarie e passano attraverso il sistema vascolare che perde dei tumori e si accumulano all'interno. Poco tessuto sano è esposto al farmaco tossico.
Dentro i tumori, le nanoparticelle si raccolgono all'interno dei compartimenti lisosomiali delle cellule cancerose, dove sono, in sostanza, digerito. Il pH è molto più basso che nel sangue circolante, ha spiegato Steinmetz. Il guscio si deteriora e rilascia fenantriplatino.
Il guscio viene scomposto in proteine e eliminato attraverso processi metabolici o cellulari naturali entro un giorno mentre il candidato farmaco inizia a bloccare la trascrizione, portando a maggiori quantità di morte cellulare attraverso l'apoptosi rispetto ai platini reticolanti.
I ricercatori affermano che la somministrazione del fenantriplatino nel tumore ha portato a un miglioramento delle sue prestazioni rispetto al cisplatino o al fenantriplatino libero.
Lippard e Steinmetz continuano a collaborare, indagare sull'uso di questo sistema per fornire altri farmaci o farmaci candidati, utilizzare in altri tipi di cancro, l'aggiunta di agenti sulla parte esterna del guscio per aumentare l'accumulo all'interno dei tumori e altro ancora.