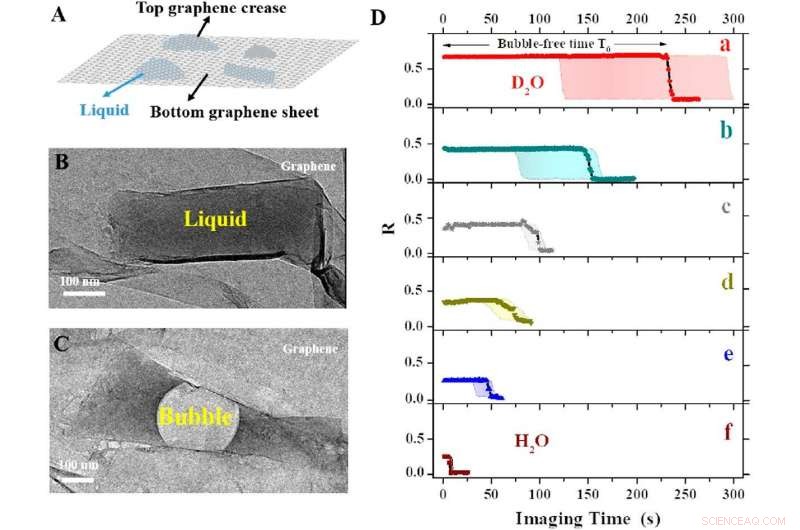
(A) La tasca in grafene protegge il campione contenuto nel liquido. (B) Foto della tasca del grafene. (C) Come risultato del fascio di elettroni incidente, una bolla d'aria riempie la maggior parte della tasca dopo un breve periodo di tempo. (D) Tempo di formazione delle bolle, a seconda del tipo di soluzione che riempie la tasca. Il tempo più lungo senza bolle si ottiene quando la tasca viene riempita con a) acqua pesante (D2O), seguito da acqua (H2O) con b) 50% glicerolo, c) NaCl 100 mM, d) gallato di n-propile 10 mM, e) 3% di glicerolo, e f) solo acqua. Credito:Istituto per le scienze di base
Poiché la vita si basa principalmente sull'acqua, le nostre molecole si muovono, vibrare e fare capriole in un ambiente liquido. Ma la microscopia elettronica, una tecnica per studiare una versione statica di questo nanomondo, è stata quasi impossibile da usare per vedere le molecole in movimento, perché il fascio di elettroni incidente danneggia i campioni. Scienziati del Center for Soft and Living Matter, all'interno dell'Istituto per le scienze di base (IBS), segnalare un notevole miglioramento in questo settore.
Questo studio, pubblicato in ACS Nano , è il primo ad utilizzare acqua pesante (D 2 O) - una forma di acqua che contiene deuterio (D) invece di idrogeno - nel campo della microscopia elettronica a trasmissione (TEM). Questo approccio ritarda notevolmente il danneggiamento del campione, che è uno dei principali impedimenti per una più ampia applicazione della TEM in fase liquida a campioni biologici fragili.
Nella microscopia elettronica, gli elettroni emessi contro il campione hanno una lunghezza d'onda molto più corta della luce, quindi sono più adatti a fornire informazioni sulle singole molecole. D'altra parte, il fascio di elettroni è estremamente potente e rischia di danneggiare il provino a causa della sua elevata energia, che genera una carica elettrica e rompe i legami chimici.
I ricercatori dell'IBS hanno utilizzato una minuscola tasca piena di liquido racchiusa tra fogli di grafene atomicamente sottili, all'interno del quale le molecole del campione sono libere di muoversi e sono protette da cariche elettriche, e testato diversi tipi di liquidi per trovare quello che conserva il campione più a lungo. "In contrasto con l'approccio comune di ridurre l'energia del fascio di elettroni per ritardare il danneggiamento del campione, ci siamo concentrati sulla messa a punto dell'ambiente:l'acqua in cui sono disciolte le molecole di interesse, "dice Huan Wang, coautore dello studio.
Gli scienziati dell'IBS hanno dimostrato che l'uso dell'acqua pesante presenta numerosi vantaggi rispetto ai metodi concorrenti. D 2 O ritarda nel modo più efficace non solo la formazione di bolle di gas, ma anche danni strutturali delle singole molecole polimeriche. Rispetto a H 2 Oh, D 2 O ha un neutrone in più, il che significa che è più pesante, quindi più difficile da dissociare in radicali, e meno reattivo nel successivo processo dannoso.

Quando esposto al fascio di elettroni, le molecole di polimero (polistirene solfonato) vengono degradate più rapidamente nella soluzione di glicerolo rispetto al D2O. Credito:Istituto per le scienze di base
"L'acqua pesante supera i metodi concorrenti di un fattore da due a cinque almeno, " disse Kandula Hima Nagamanasa, coautore dello studio. "Dal momento che la formazione delle bolle è ritardata e le molecole sono rimaste visibili per il doppio del tempo".
Un vantaggio altrettanto importante è che D 2 O è una crema solare innocua. Il campione, un polimero di polistirene solfonato in questo caso, ha mostrato lo stesso modello di dinamica e contrasto simile in D 2 O e in acqua.
"Nel futuro, intendiamo estendere questo studio a macromolecole più complesse, come DNA e proteine, " ha spiegato Steve Granick, direttore del centro IBS e corrispondente autore dello studio. "Inoltre, lo studio apre strade per osservare fenomeni a lungo termine in altre tecniche di microscopia correlate, come cryoEM (microscopia elettronica criogenica), e per ottenere maggiori informazioni statistiche su fenomeni complessi, come l'autoassemblaggio di singole molecole in strutture biologiche più complesse."