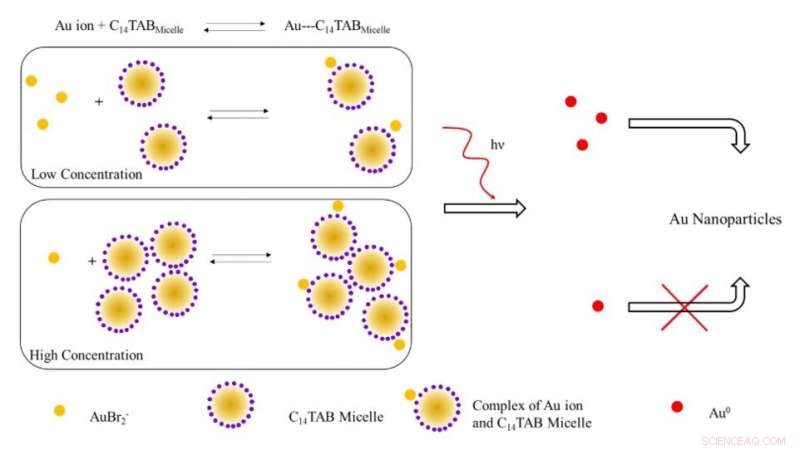
Illustrazione schematica del meccanismo proposto per la formazione di nanoparticelle d'oro per irradiazione con radiazioni ionizzanti. A basse concentrazioni di tensioattivo, la maggior parte degli ioni d'oro (AuBr2- /Au1+) sono probabilmente liberi in soluzione (non legati alle micelle). Con l'aumento della concentrazione di tensioattivo, l'equilibrio si sposta verso destra con una diminuzione degli ioni oro liberi. All'irradiazione, il numero di atomi di Au^0 formati per riduzione a bassa concentrazione di tensioattivo è maggiore a causa della presenza di un maggior numero di ioni d'oro liberi rispetto al sistema ad alta concentrazione di tensioattivo. Il maggior numero di atomi d'oro liberi porta ad una maggiore resa di nanoparticelle d'oro a causa della riduzione assistita dalla superficie con ioni d'oro non reagiti. Credito:progressi scientifici, doi:10.1126/sciadv.aaw8704.
La misurazione di routine delle dosi di radiazioni può essere clinicamente difficile a causa delle limitazioni con i dosimetri convenzionali utilizzati per misurare l'assorbimento della dose di radiazioni ionizzanti esterne. In un nuovo studio, Karthik Pushpavanam e un team interdisciplinare di ricercatori nei dipartimenti di Ingegneria Chimica, Scienze Molecolari, Banner MD Anderson Cancer Center e Arizona Veterinary Oncology negli Stati Uniti hanno descritto un nuovo nanosensore a base di gel. La tecnologia consente il rilevamento colorimetrico e la quantificazione dei profili topografici della dose di radiazioni durante la radioterapia.
In caso di esposizione a radiazioni ionizzanti, gli scienziati hanno convertito gli ioni d'oro nel gel in nanoparticelle d'oro (AuNPs) accompagnate da un cambiamento visivo nel colore del gel dovuto alle proprietà plasmoniche. Hanno usato l'intensità del colore formato nel gel come reporter quantitativo per le radiazioni ionizzanti e hanno utilizzato per la prima volta il nanosensore in gel per rilevare schemi di dose topografici complessi dopo la somministrazione a modelli fantasma antropomorfi, seguiti da applicazioni con pazienti canini vivi sottoposti a radioterapia clinica. La facilità di fabbricazione, operazione, lettura rapida, il rilevamento colorimetrico e il costo relativamente basso della tecnologia implicavano il potenziale traslazionale per la mappatura topografica della dose durante le applicazioni di radioterapia clinica. Il lavoro di ricerca è ora pubblicato su Progressi scientifici .
I progressi nella radioterapia hanno portato a notevoli sofisticazioni e software di pianificazione all'avanguardia per fornire alte dosi di radiazioni conformi ai pazienti per una migliore qualità della vita dopo il trattamento. Durante la radioterapia, una dose elevata viene in genere erogata a un tumore bersaglio riducendo al minimo la dose di radiazioni erogata al tessuto circostante. Durante le cure palliative ai pazienti vengono somministrate dosi frazionarie maggiori per concludere il trattamento in un breve lasso di tempo. Però, errori software durante tali procedure possono portare a sovradosaggio e conseguente morbilità.
Per ridurre al minimo la sovraesposizione accidentale, i ricercatori cercano di verificare in modo indipendente la dose di radiazioni erogata in corrispondenza o in prossimità del tessuto bersaglio per una sicurezza avanzata del paziente. tecnicamente, sia i sensori molecolari che i nanosensori possono superare i limiti presenti nei sistemi convenzionali per formare alternative pratiche come sensori facili. Però, i loro limiti esistenti dovrebbero essere affrontati e alleviati per sviluppare sensori robusti ed efficaci che determinino quantitativamente e qualitativamente i profili di dose topografici durante la radioterapia clinica.

Immagini digitali e spettri UV-visibili di diverse formulazioni di nanosensori in gel esposti a dosi terapeutiche di raggi X (A) Immagini di nanosensori in gel fabbricati in piastre di coltura cellulare da 24 pozzetti e contenenti diverse concentrazioni di C14TAB (da 24,5 a 73,5 mM) dopo l'esposizione a varie dosi di radiazioni ionizzanti (raggi X da 0 a 10 Gy); Il tempo di attesa di Na2S era di 5 minuti dopo l'irradiazione, e il tempo di incubazione è stato di 10 min. Le immagini sono state acquisite 1 ora dopo l'irradiazione. Si osserva un aumento visibile dell'intensità del colore marrone con dosi crescenti di radiazioni ionizzanti per la maggior parte delle concentrazioni di C14TAB utilizzate durante lo sviluppo del sensore gel. (B a F) Spettri di assorbanza (300 a 990 nm) degli stessi nanosensori gel contenenti (B) 24,5 mM, (C) 31 mm, (D) 37 mm, (E) 49 mm, e (F) 73,5 mM irradiati utilizzando diverse dosi di radiazioni. I picchi di assorbimento caratteristici tra le lunghezze d'onda di 500 e 600 nm sono indicativi di nanoparticelle d'oro formate nei gel. Le corrispondenti dosi di radiazioni sono menzionate nella legenda con l'aumento della dose di radiazioni (dall'alto verso il basso). A.U., unità arbitrarie. Credito fotografico:Sahil Inamdar, Università statale dell'Arizona. Credito:progressi scientifici, doi:10.1126/sciadv.aaw8704
Poiché le nanoparticelle d'oro (AuNP) hanno caratteristiche fisiche e chimiche uniche che forniscono un'eccellente piattaforma per sviluppare sensori. Pushpavanam et al. ha progettato un sensore colorimetrico in cui le radiazioni ionizzanti causavano la formazione di AuNP da precursori di sale incolori. La formazione di un nanosensore a base di gel può consentire una facile manipolazione e applicazioni durante la radioterapia clinica.
Nel presente lavoro, il team ha dimostrato il rilevamento colorimetrico e la quantificazione dei profili di distribuzione della dose utilizzando un nanosensore in gel per mappare topograficamente le dosi di radiazioni lungo le superfici dei tessuti. Durante le valutazioni precliniche, il team ha somministrato la tecnologia del nanosensore in gel a pazienti canini vivi sottoposti a radioterapia. In totale, i risultati hanno indicato la portata della tecnologia per la traduzione clinica nei pazienti umani e la capacità di determinare le dosi topografiche per pianificare i trattamenti e verificare i dosaggi durante la radioterapia del cancro.
Durante gli esperimenti, la conversione degli ioni d'oro in nanoparticelle è stata accompagnata da uno sviluppo di colore marrone nella regione irradiata del nanosensore in gel. Mentre l'oro esiste in uno stato trivalente in generale (AuCl 4 - ) può essere ridotto a uno stato di valenza +1 metastabile (AuBr 2 - ) a temperatura ambiente utilizzando acido ascorbico (vitamina C). L'irradiazione di gel contenenti livelli terapeutici di radiazioni ha stimolato la radiolisi o la scissione delle molecole d'acqua in radicali liberi altamente reattivi. Gli elettroni idrati generati dalla radiolisi a loro volta riducevano l'oro monovalente per formare atomi d'oro nel suo stato zerovalente (Au 0 ) che ha nucleato e maturato in AuNP di colore marrone. L'intensità variava con la dose di radiazioni e il team ha utilizzato la gamma di risposte lineari per calibrare il nanosensore in gel. Sulla base di questo principio, Pushpavanam et al. determinato la risposta dei gel completamente irradiati per calibrare l'assorbanza con la dose di radiazione.
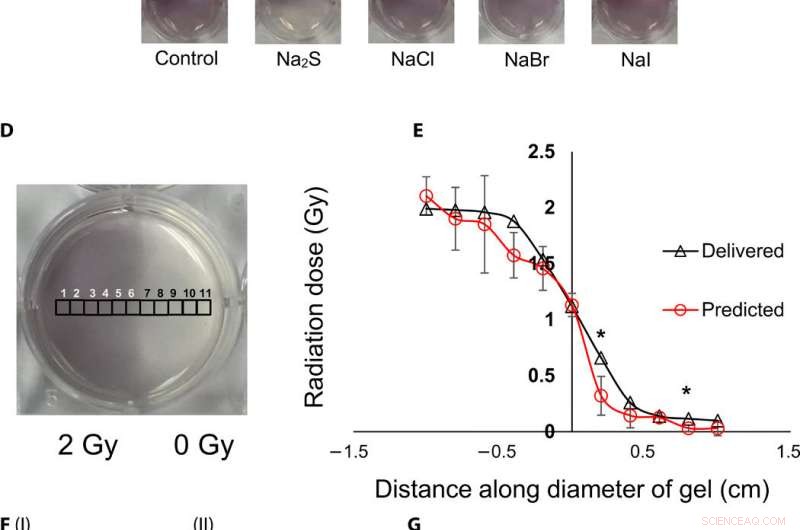
Visualizzazione topografica e quantificazione delle dosi di radiazioni mediante nanosensori a gel. (A) Nanosensore in gel (a sinistra) prima dell'irradiazione, (al centro) metà superiore irradiata con 4 Gy e immagine acquisita 2 min dopo l'irradiazione, e (a destra) immagine acquisita 1 ora dopo l'irradiazione. Un aumento visibile dell'intensità del colore nella metà inferiore non irradiata indica trasudazione del colore e perdita di informazioni topografiche. (B) I:gel di agarosio 1,5% (p/v) (a sinistra) 2 min dopo l'irradiazione e (a destra) 1 ora dopo l'irradiazione; II:2% (w/v) agarose gel (left) 2 min after irradiation and (right) 1 hour after irradiation indicates that the increase in agarose weight percentage does not preserve topographical dose information. (C) Gel nanosensor incubated with 5 mM sodium sulfide (Na2S) and various sodium halides with a wait time of 10 min and incubation time of 10 min; images were acquired after 1 hour. No loss of topographical information is observed upon incubation with sodium sulfide. All gels were fabricated in 24-well plates. (D) Colorimetric response of the gel nanosenor irradiated on one-half with a 2-Gy x-ray dose. A visible appearance of maroon color in the irradiated region illustrates the ability of the gel nanosensor to visualize topographical dose profiles. Each black square box (labeled 1 to 11) on the gel nanosensor corresponds to a grid of size ≈2 × 2 mm, whose absorbance at 540 nm is determined. Grids starting from 1 to 5 are regions exposed to ionizing radiation, 6 is the grid at the edge of the irradiation field, and grids from 7 to 11 are regions outside the field of irradiation. (E) Dose fall-off profile for the gel nanosensor irradiated by 2 Gy on one-half. The delivered and predicted radiation doses are comparable, which indicates the efficacy of the gel nanosensor in visualizing and retaining topographical information. In tutti i casi, Na2S was added for 10-min incubation time after a wait time of 30 min. Radiation doses predicted by the gel nanosensor as compared with the delivered radiation dose as obtained from the treatment planning system. Asterisks indicate statistically significant differences (P <0.05) between the delivered dose and the dose predicted by the gel nanosensor (n =3 independent experiments). (F) Representative image of a petri dish containing the gel nanosensor formulation (≈3 mm thick and ≈10 cm diameter) irradiated with a 1 cm × 1 cm square field of x-ray radiation. From the left, each square indicates increasing radiation dose from (I) 0.5 Gy (red box), 1 Gy, and 1.5 Gy; (II) 2, 2.5, 3, and 3.5 Gy; and (III) 4, 4.5, and 5 Gy; the black box in image (II) shows 0 Gy. (G) Visualization of a complex topographical dose pattern (ASU letters) generated using a 2-Gy x-ray dose. The petri dish has a diameter of ≈10 cm. In (F) and (G), the gel nanosensors contain 24.5 mM C14TAB, and Na2S was added after a wait time of 30 min and incubation time of 10 min; a representative image from three independent experiments is shown. Photo credit:Sahil Inamdar, Università statale dell'Arizona. Credito:progressi scientifici, doi:10.1126/sciadv.aaw8704.
To determine intensity of the color and dose delivered within gels after irradiation, the researchers used absorbance spectroscopy and observed a decrease in the spectral profile width, with increasing radiation dose for decreased polydispersity (ratio of the percentage of the standard deviation to the average value) of the nanoparticles. The peak absorbance intensity increased with increasing radiation dose to corroborate the observed increase in color intensity.
To understand the gel nanosensor's ability to detect topographical distribution of the radiation dose, the scientists irradiated half of the gel nanosensor with a 4 gray (Gy) dose. The maroon-color only appeared in the irradiated area confirming AuNP formation, but after one hour of exposure, the color bled into the irradiated region showing loss of topographic information in the gel with time. The team observed the phenomenon to arise from reaction-controlled conditions and not based on the gel composition. By incubating the gel with sodium sulfide (Na 2 S) for 10 minutes, they suppressed the color bleed-over and reasoned that to the ability to quench unreacted gold ions in the nonirradiated region and preserve dose information accurately for dose visualization and dosimetry. The scientists adopted the sensor for wide dose ranges by modulating the time of Na 2 S addition; to achieve a level of flexibility hitherto unavailable in clinical dose detection systems.
The research team then used the gel nanosensor to visualize diverse topographical radiation patterns, where the intensity of the color increased with increasing dose while preserving topographical integrity. Come prova del concetto, they showed the gel nanosensor's ability to detect complex radiation patterns with a model dose patterned to form "ASU" (after Arizona State University). Then using transmission electron microscopy (TEM), the scientists characterized the generated gold nanoparticles as a function of dose to observe reduced average nanoparticle diameter and polydispersity at higher doses of radiation. They followed this with energy dispersive X-ray spectroscopy (EDS) to detect higher yields of AuNPs in the irradiated regions of the gel nanosensor as expected.

Gel nanosensor enabled topographical detection and quantification of clinical radiation doses in anthropomorphic head and neck phantoms. (A) Anthropomorphic head and neck phantom treated with an irregularly shaped x-ray radiation field below the left eye. (B) Image of the gel nanosensor positioned on the anthropomorphic phantom in the radiation field mimicking a conventional radiotherapy session. (C) Axial view of the treatment planning image along the central axis of the radiation beam representing an irregularly shaped radiation field used to deliver a complex radiation pattern under the eye of the phantom. The core of the crescent-shaped treatment region receives a radiation dose of 2.3 Gy (highlighted in red), and regions receiving lower doses are highlighted with different colors going outward (from green to light pink). (D) Visual image of the dose pattern on the gel nanosensor formed after delivery of 2.3 Gy. Only the irradiated region develops a maroon color, while the nonirradiated region remains colorless. (E) Expected topographical dose “heat map” profile of the radiation dose delivered to the gel placed in the phantom. The expected profile is generated from the treatment plan in the dose delivery system. In these figures, red and blue colors indicate higher and lower radiation doses, rispettivamente. (F) Topographical doses predicted by the irradiated gel nanosensor. Absorbance values of ≈2 mm × 2 mm grids were quantified using a calibration curve to generate the topographical dose profile. The anticipated dose received by the core of the crescent-shaped profile (2.3 Gy) is comparable to the dose profile predicted by the gel nanosensor (2.3 Gy), which demonstrates the capability of the gel nanosensor to qualitatively and quantitatively detect complex topographical dose profiles. Photo credit:Sahil Inamdar, Università statale dell'Arizona. Credito:progressi scientifici, doi:10.1126/sciadv.aaw8704.
To investigate translational potential of the gel nanosensor and predict topographical profiles of radiation, Pushpavanam et al. first used a head and neck phantom model. They delivered an irregular crescent-shaped radiation dose near the eye to mimic clinically challenging administration modes of radiotherapy close to critical structures such as the eye during skin cancer treatment. The dose profile delivered using the treatment planning system was in excellent agreement with the predictions of the gel nanosensor. Indicating its capability to detect and predict complex radiation patterns similar to those used in clinical human radiotherapy.
During preclinical studies, the research team used two canine models undergoing radiotherapy to investigate the efficiency of gel nanosensors as independent, nanoscale radiation dosimeters for the first time and compared the efficiency with conventional clinical radiochromic films. On completion of the treatment, Pushpavanam et al. observed maroon color formation in one-half of the gel, whereas the non-irradiated region remained colorless. They showed predictions of the gel nanosensor in the irradiated region to agree excellently with the treatment planning system and the radiochromic film. The gel nanosensor also predicted for the region external to the irradiation to receive minimal radiation and their topographical dose profiles as well. The performance was comparable to clinical radiochromic films but with faster than conventional wait times (typically> 24 hours) to obtain the results. The scientists demonstrated the simplicity of fabrication, operation, readout time and cost effectiveness ($ 0.50 per gel material only) of the frugal invention. They maintained the response of the gel nanosensor for at least seven days to indicate long-term retrieval of dosing data unlike with fluorescence-based dosimeters with readouts that lasts mere minutes.
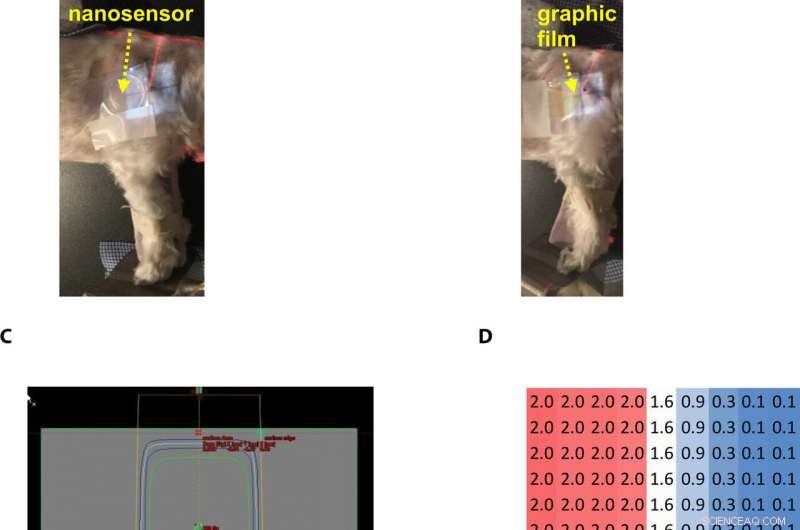
Gel nanosensor enabled topographical detection and quantification of radiation delivered to canine patient A undergoing clinical radiotherapy. Representative image of (A) half of the gel nanosensor and (B) half of the radiographic film positioned in the radiation field delivered to canine patient A. (C) Treatment planning software depicting the delivery of a 2-Gy dose delivered to the surface of patient A (neon green edge along the rectangular gray box indicates the region receiving the 2-Gy dose). (D) The irradiated region received a dose of 2 Gy (highlighted in red squares), with irradiation dose dropping to a minimal radiation 0.1 Gy (highlighted in blue squares) outside the field of irradiation. A color change is visible in both the (E) gel nanosensor whose color changes to maroon and (F) radiographic film whose color changes to dark green after irradiation. The predicted dose map in the gel nanosensor (Na2S addition wait time of 30 min and incubation time of 10 min) and radiographic film are shown below each corresponding sensor. Similarity in the dose profiles indicates the efficacy of the gel nanosensor for clinical dosimetry. The time for readout of the gel nanosensor was 1 hour after irradiation, while the radiochromic film required>24 hours of developing time before readout. All experiments were carried out three independent times. Photo credit:Sahil Inamdar, Università statale dell'Arizona. Credito:progressi scientifici, doi:10.1126/sciadv.aaw8704.
In questo modo, Karthik Pushpavanam and colleagues developed the first colorimetric gel nanosensor as a nanoscale dosimeter to detect and distinguish regions exposed to irradiation. They optimized the platform with a chemical quenching agent (Na 2 S) to accurately reveal topographical dose distribution during clinical radiotherapy. The scientists can control the pore size distribution of the gel substrate to enhance efficacy of the nanosensor. They tested the efficiency of the gel nanosensor to predict complex topographical dose profiles in anthromorphic head and neck phantoms and in live canine patients undergoing radiotherapy. The highly disruptive and translational potential of the gel nanosensor technology will lead to improved patient safety and outcomes in clinical radiotherapy.
© 2019 Scienza X Rete