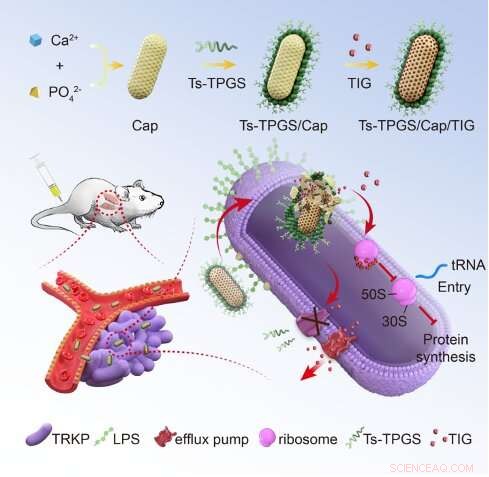
Rappresentazione schematica della fabbricazione dei nanorods e del meccanismo per superare la resistenza alla tigeciclina di TRKP. TIG:tigeciclina; Ts-TPGS/Cap/TIG:TPGS caricati con tigeciclina e nanobarre di fosfato di calcio funzionalizzate con S-tanatina; TRKP:polmonite da Klebsiella resistente alla tigeciclina. LPS:lipopolisaccaride. Credito:Scuola di Medicina dell'Università di Zhejiang
L'uso a lungo termine ed eccessivo di antibiotici ha causato la diffusione della resistenza agli antibiotici. Il processo di sviluppo di nuovi antibiotici, che richiede tempo e denaro, si traduce in un'emergenza molto più lenta di nuovi farmaci antibatterici rispetto a quella della resistenza batterica. L'emergere di superbatteri è cresciuto fino a diventare una sfida dominante nella salute umana. La tigeciclina è considerata l'ultima linea di difesa per combattere la Klebsiella pneumoniae multiresistente. Tuttavia, il crescente utilizzo ha portato a un aumento della resistenza ai farmaci e al fallimento del trattamento. La resistenza alla tigeciclina di Klebsiella pneumoniae rimane un problema globale che deve essere urgentemente risolto.
Il 29 giugno 2022, il Prof. Du Yongzhong del College of Pharmaceutical Sciences, Zhejiang University, il Prof. Lu Xiaoyang e Jiang Saiping del First Affiliated Hospital, Zhejiang University School of Medicine hanno co-pubblicato un articolo intitolato "TPGS-based and S- nanorod funzionalizzati thanatin per superare la resistenza ai farmaci nella polmonite da Klebsiella" sulla rivista Nature Communications . La loro ricerca dimostra che nanobarre modificate con D-alfa tocoferil polietilenglicole succinato (TPGS) e funzionalizzate con peptide S-tanatina (Ts) a base di nanoparticelle di fosfato di calcio possono superare la resistenza alla tigeciclina della polmonite da Klebsiella.
In primo luogo, i ricercatori hanno preparato le nanobarre modificate con TPGS caricate con tigeciclina e funzionalizzate con peptide S-tanatina, Ts-TPGS/Cap/TIG (TTCT) e hanno caratterizzato le proprietà del TTCT. Hanno scoperto che i nanorod Ts-TPGS/Cap preparati potrebbero incapsulare efficacemente il TIG e ottenere un rilascio prolungato del farmaco. Il TTCT con una dimensione delle particelle di ~ 25 nm non si disassemblava in circolazione e mostrava un'eccellente stabilità a temperatura ambiente.
Successivamente, i ricercatori hanno valutato l'attività antibatterica del TTCT ed esplorato i meccanismi alla base del superamento della resistenza. Hanno scoperto che Ts-TPGS/Cap mostrava il targeting e un maggiore accumulo sia nella polmonite da Klebsiella (KPN) che nella TRKP attraverso il legame tra Ts e LPS. TPGS potrebbe esercitare la sua capacità inibitoria sull'attività delle pompe di efflusso e sull'espressione di acrA, acrB e ramA in TRKP. In questo modo, la concentrazione di TIG all'interno dei batteri era significativamente più alta nel gruppo TTCT rispetto ad altri gruppi. La capacità antibatterica sinergica tra Ts e TIG ha ulteriormente potenziato l'attività antibatterica TTCT, superando così la farmacoresistenza del TRKP.
Nei topi con polmonite, Ts-TPGS/Cap si accumulava specificamente nei polmoni. La somministrazione di TTCT potrebbe ridurre significativamente la conta dei globuli bianchi e dei neutrofili nei campioni di sangue e diminuire i livelli di cellule totali e di proteina C reattiva (CRP) nel liquido di lavaggio broncoalveolare (BALF). Inoltre, il TTCT è stato in grado di migliorare l'infiltrazione dei neutrofili nei polmoni e ridurre le colonie batteriche da BALF, aumentando così apparentemente i tassi di sopravvivenza dei topi con polmonite causata da TRKP.
Nel complesso, è stato progettato un sistema di somministrazione di nanofarmaci basato su TPGS e modificato con Ts. I nanorod preparati possono aumentare l'accumulo di tigeciclina nei batteri attraverso l'effetto inibitorio sulle pompe di efflusso esercitato da TPGS e la capacità di indirizzare la S-tanatina ai batteri. La capacità antibatterica sinergica tra S-tanatina e tigeciclina potenzia ulteriormente l'attività antibatterica, superando così la resistenza alla tigeciclina del TRKP. I risultati forniscono una strategia terapeutica per le malattie delle infezioni causate da batteri gram-negativi MDR. + Esplora ulteriormente