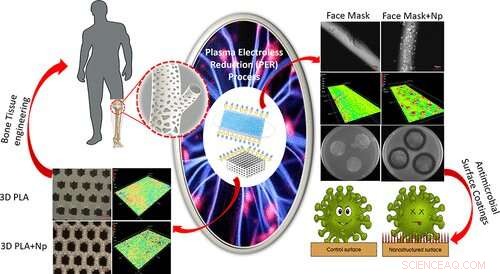
Astratto grafico. Credito:Materiali applicati e interfacce ACS (2022). DOI:10.1021/acsami.2c01195
Un team interdisciplinare di ricercatori dell'Università dell'Alabama a Birmingham ha sviluppato un nuovo processo abilitato al plasma che potrebbe limitare la proliferazione delle tossine dagli impianti nel flusso sanguigno di un paziente. Il team, guidato da Vinoy Thomas, Ph.D., professore associato presso il Dipartimento di ingegneria meccanica e dei materiali della UAB School of Engineering, ha recentemente pubblicato i risultati in ACS Applied Materials &Interfaces rivista.
Nell'articolo, gli autori spiegano che una delle principali sfide nello sviluppo di materiale da impianto biomedico modificato con nanoparticelle consiste nell'attaccare stabilmente nanoparticelle metalliche su superfici diverse, in particolare superfici polimeriche.
"Per anni, gli scienziati hanno ottenuto la sintesi di nanoparticelle metalliche in soluzioni acquose utilizzando agenti riducenti sia chimici che biologici (estratti vegetali)," ha affermato Thomas. "La sfida di attaccare nanoparticelle metalliche è particolarmente difficile nei casi che coinvolgono biomateriali polimerici idrofobici, in cui ricade la maggior parte dei biomateriali polimerici."
Per affrontare questa sfida, Thomas e il suo team hanno sviluppato un processo abilitato al plasma chiamato riduzione senza elettrolisi del plasma. Il processo PER consente ai ricercatori di depositare nanostrutture di oro e argento su diverse superfici di materiali polimerici 2D e 3D, come carta di cellulosa, maschere facciali a base di polipropilene e scaffold polimerici stampati in 3D.
"È noto che esistono problemi di tossicità offerti dal rilascio rapido e prematuro delle nanostrutture metalliche dal materiale dell'impianto nel flusso sanguigno", ha affermato Thomas. "Questo problema potrebbe essere affrontato solo garantendo l'ancoraggio stabile delle nanostrutture metalliche sulle superfici dell'impianto. Questo ci ha ispirato a ottimizzare il nostro processo PER conducendo un'indagine sistematica e approfondita della concentrazione del precursore metallico seguito dal lavaggio con sonicazione prima della coltura cellulare in vitro."
Nello studio di Thomas, il suo team è stato in grado di ancorare con successo le nanoparticelle d'argento sulla superficie dei polimeri stampati in 3D senza alcun rilascio rapido nell'ambiente circostante. L'esperienza del team nella produzione additiva ha anche consentito loro di progettare wafer per scaffold 3D più piccoli che si adattano al pozzetto di una piastra da 96 pozzetti.
"Prevediamo che la progettazione di un'impalcatura 3D così piccola e coerente garantirebbe test in vitro su larga scala e più affidabili di scaffold 3D", ha affermato Thomas. "Questa ottimizzazione sistematica della realizzazione di nanostrutture metalliche uniformi su scaffold 3D con citocompatibilità e potenziali proprietà antibatteriche sarà altamente rilevante e può potenzialmente avere un impatto sul futuro sviluppo di scaffold biocompatibili, in particolare per la malattia dell'osteomielite".
Ci sono voluti due anni prima che il team sviluppasse il processo PER, ma il processo è solo uno dei numerosi aspetti che Thomas sta studiando riguardo al plasma.
"Il plasma, il quarto stato della materia, è un gas parzialmente ionizzato che rappresenta uno dei metodi più ecologici per sintetizzare nanoparticelle metalliche in una fase liquida", ha affermato. "Ha un'enorme capacità nella lavorazione dei materiali e nel decontaminare le superfici per prevenire la diffusione di COVID-19 e altre malattie trasmissibili". + Esplora ulteriormente