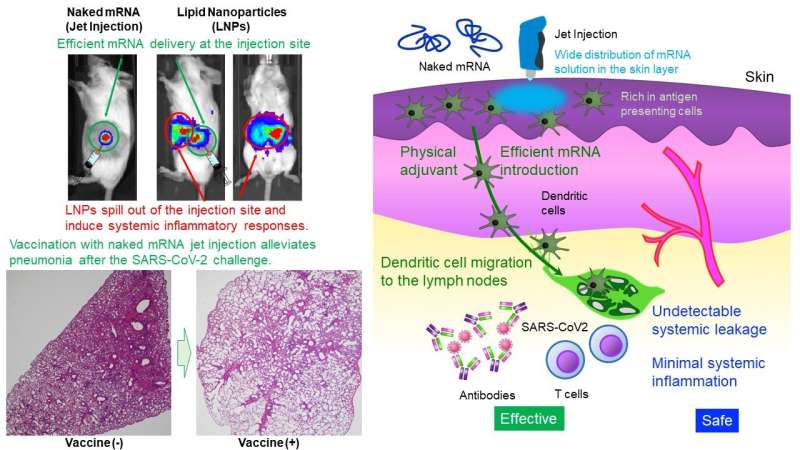
Il Laboratorio Uchida del Centro Innovazione di NanoMedicina ha dimostrato che la somministrazione intradermica del solo mRNA (mRNA nudo) senza protezione da nanoparticelle ha indotto una forte vaccinazione contro la SARS CoV-2, un virus che causa COVID-19, nei topi e nei primati. L'mRNA è altamente instabile, generalmente si ritiene che richieda una minuscola capsula, come le nanoparticelle lipidiche (LNP), per la somministrazione.
Il metodo qui riportato è il primo vaccino a mRNA nudo che dimostra la prevenzione contro la SARS-CoV-2. Senza l’utilizzo di LNP, che hanno un’elevata probabilità di causare eventi avversi sistemici, questo vaccino può consentire somministrazioni ripetute. Ora è in fase di sviluppo per studi clinici. I risultati dettagliati della ricerca saranno pubblicati in Molecular Therapy .
Durante la pandemia di COVID-19, i vaccini mRNA hanno dimostrato un’efficacia eccezionale, con miliardi di dosi somministrate in tutto il mondo. Tuttavia, nel corso del loro rapido sviluppo, sono emerse sfide, in particolare riguardanti reazioni avverse relativamente forti, comprese quelle gravi, che rimangono problemi significativi.
Sebbene queste reazioni avverse possano essere ritenute accettabili per un numero limitato di dosi durante una pandemia, una piattaforma più sicura che consenta dosi multiple nel corso della vita è auspicabile per i richiami in corso del COVID-19 e per l’estensione dell’applicazione del vaccino mRNA ad altre malattie infettive. Gli attuali vaccini a mRNA sono stati associati a reazioni avverse, attribuite principalmente alle nanoparticelle lipidiche (LNP) che trasportano l'mRNA (mRNA avvolto in un rivestimento lipidico).
Gli LNP possiedono proprietà immunostimolanti e possono fuoriuscire dal sito di iniezione, provocando risposte infiammatorie sistemiche. Tuttavia, gli LNP svolgono un ruolo cruciale nell’efficacia del vaccino, come la [Funzione I] che previene la degradazione dell’mRNA e lo trasporta in modo efficiente nelle cellule, la [Funzione II] che migra ai linfonodi per fornire l’mRNA alle cellule immunitarie e la [Funzione III] che stimola il sistema immunitario. attraverso lipidi immunostimolanti. Il presente studio mira a ottenere queste funzioni senza fare affidamento sugli LNP.
Questo studio fornisce una progettazione semplice e sicura, la somministrazione di mRNA nudo. Per quanto riguarda la [Funzione II], poche cellule immunitarie risiedono nel tessuto muscolare, un attuale sito di somministrazione dei vaccini a mRNA. Pertanto, è stato preso di mira il tessuto cutaneo, che è più ricco di cellule immunitarie.
Inoltre, per la [Funzione I], il gruppo di ricerca ha utilizzato un Jet Injector che facilita il rilascio di mRNA alle cellule della pelle utilizzando lo stress fisico indotto dal flusso a getto. In uno studio condotto da un reporter, Jet Injector ha migliorato l’efficienza di erogazione dell’mRNA di oltre 100 volte rispetto all’iniezione convenzionale con ago e siringa. Inoltre, l'mRNA è rimasto nel sito di iniezione senza perdite sistemiche rilevabili.

D’altra parte, gli LNP caricati con mRNA (mRNA ricoperto da un rivestimento lipidico) sono migrati nel fegato, nella milza e in altri organi sistemici dopo la somministrazione intradermica, provocando infiammazioni lì. Inoltre, l'infiammazione nel sito di iniezione era molto minore nel nostro metodo, mentre l'mRNA avvolto in un rivestimento lipidico induceva l'infiltrazione di cellule infiammatorie e la necrosi dei tessuti.
Successivamente, il gruppo di ricerca ha dimostrato per la prima volta la capacità di vaccinazione dell’mRNA nudo utilizzando un antigene modello. L'iniettore a getto ha migliorato drasticamente l'efficacia della produzione di anticorpi a un livello paragonabile a quello dell'mRNA avvolto in un rivestimento lipidico alle dosi massime tollerabili.
Questi anticorpi combattono i virus presenti nel corpo, prevenendo l’infezione, ma non possono rimuovere le cellule infette. D’altra parte, l’immunità cellulare rimuove tali cellule malate, svolgendo un ruolo fondamentale nella prevenzione di malattie gravi. Curiosamente, il vaccino a mRNA nudo aumenta efficacemente il numero di immunociti, come le cellule T CD4-positive e le cellule T CD8-positive.
Quindi, il gruppo di ricerca ha condotto esperimenti di sfida al virus dopo la vaccinazione con mRNA nudo che prendeva di mira la proteina spike del virus SARS-CoV-2. La vaccinazione ha ridotto significativamente la quantità di virus nei polmoni e ha alleviato l’infiammazione polmonare rispetto a un controllo non vaccinato. Questo vaccino ha fornito alle scimmie cynomolgus un'efficacia paragonabile a quella dei topi senza reazioni avverse significative.
Il presente studio include anche analisi meccanicistiche. Per quanto riguarda la [Funzione II], il vaccino a mRNA nudo è rimasto nel sito di iniezione e non è migrato verso i linfonodi. D'altra parte, le cellule presentanti l'antigene che hanno assorbito l'mRNA nel sito di iniezione sono migrate verso i linfonodi, il che può contribuire all'efficacia della vaccinazione.
Infatti, il vaccino ha indotto la maturazione del linfonodo vicino al sito di iniezione. Per la [Funzione III], il Jet Injector ha causato un'infiammazione transitoria localizzata nel sito di iniezione, reclutando linfociti. L'iniezione di ago e siringa di mRNA nudo non ha indotto una tale risposta infiammatoria. Questi risultati suggeriscono che la stimolazione immunitaria mediante Jet Injector può funzionare come adiuvante fisico per migliorare l’efficacia della vaccinazione. Le reazioni infiammatorie locali osservate sono scomparse in pochi giorni.
In conclusione, il vaccino a mRNA nudo riduce le reazioni avverse sistemiche, un problema con l’mRNA avvolto in un rivestimento lipidico, e induce un’immunità sufficiente per la protezione dalle malattie infettive. Si tratta di un risultato leader a livello mondiale nella prevenzione delle malattie infettive con il solo mRNA. In pratica, questo vaccino potrebbe diventare una piattaforma che consente somministrazioni ripetute con reazioni avverse minori. Attualmente sono in corso ulteriori studi, con l'obiettivo di una sperimentazione clinica prevista per il 2026.
Ulteriori informazioni: Saed Abbasi et al, Il vaccino mRNA privo di portatori induce una robusta immunità contro la SARS CoV-2 nei topi e nei primati non umani senza reattogenicità sistemica, Terapia molecolare (2024). DOI:10.1016/j.ymthe.2024.03.022
Informazioni sul giornale: Terapia molecolare
Fornito dal Centro Innovazione di NanoMedicina