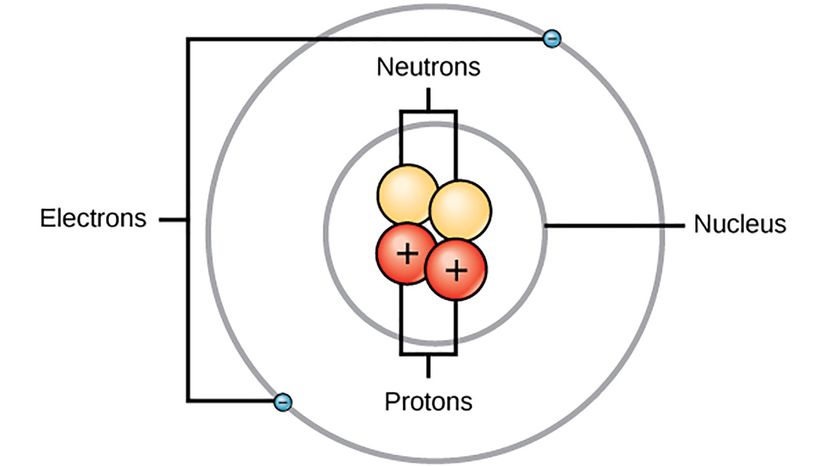
Puoi cercare l'immagine di un atomo su Internet e ne troverai uno, anche se nessuno ha mai visto un atomo prima. Ma abbiamo una stima dell'aspetto di un singolo atomo grazie al lavoro di un gruppo di scienziati diversi come il fisico danese Niels Bohr.
Gli atomi sono gli elementi costitutivi della materia:un singolo atomo di ogni singolo elemento è l'entità più elementare in natura che si attiene ancora alle regole della fisica che possiamo osservare nella vita di tutti i giorni (le particelle subatomiche che compongono gli atomi hanno le loro regole speciali) . Gli scienziati sospettavano che gli atomi esistessero da molto tempo prima di poter concettualizzare la loro struttura - anche gli antichi greci pensavano che la materia dell'universo fosse composta da componenti così piccoli che non potevano essere scomposti in qualcosa di più piccolo, e chiamarono queste unità fondamentali atomico , che significa "indiviso". Alla fine del XIX secolo, si era capito che le sostanze chimiche potevano essere scomposte in atomi, che erano molto piccoli e gli atomi di elementi diversi avevano un peso prevedibile.
Ma allora, nel 1897, Il fisico britannico J.J. Thomson scoprì che gli elettroni - particelle caricate negativamente all'interno degli atomi che tutti avevano passato la maggior parte del secolo a credere fossero completamente indivisibili - come le più piccole cose che esistessero. Thomson ha appena ipotizzato che esistessero gli elettroni, ma non riusciva a capire esattamente come gli elettroni si inserissero in un atomo. La sua migliore ipotesi era il "modello di budino di prugne, " che raffigurava l'atomo come una torta carica positivamente costellata di aree caricate negativamente sparse ovunque come la frutta in un dolce vecchio stile.
"Gli elettroni sono risultati elettrici negativi, e tutti con la stessa massa e molto piccoli rispetto agli atomi, "dice Dudley Herschbach, un chimico di Harvard che ha condiviso il Premio Nobel per la Chimica nel 1986 per i suoi "contributi riguardanti la dinamica dei processi chimici elementari, " in una e-mail. "Ernest Rutherford scoprì il nucleo nel 1911. I nuclei erano elettrici positivi, con varie masse ma molto più grandi degli elettroni, ma di dimensioni molto ridotte".
Niels Bohr era uno studente di Rutherford che assunse coraggiosamente il progetto del suo mentore di decifrare la struttura dell'atomo nel 1912. Gli ci volle solo un anno per elaborare un modello funzionante di un atomo di idrogeno.
"Il modello di Bohr del 1913 per l'atomo di idrogeno aveva orbite circolari di elettroni attorno al protone - come le orbite della Terra intorno al sole, " dice Herschbach. "Bohr aveva fatto uso di un modello semplice e regolare per lo spettro dell'atomo di idrogeno, che era stato trovato da Johann Balmer nel 1885. Ha anche fatto uso dell'idea dell'idea quantistica, trovata da Max Planck nel 1900."
Nel 1913, il modello di Bohr fu un enorme balzo in avanti perché incorporava le caratteristiche della neonata meccanica quantistica nella descrizione di atomi e molecole. Quell'anno, pubblicò tre articoli sulla costituzione di atomi e molecole:il primo e più famoso era dedicato all'atomo di idrogeno e gli altri due descrivevano alcuni elementi con più elettroni, usando il suo modello come cornice. Il modello da lui proposto per l'atomo di idrogeno aveva gli elettroni che si muovevano attorno al nucleo, ma solo su piste speciali con diversi livelli di energia. Bohr ipotizzò che la luce fosse emessa quando un elettrone saltava da una traccia a energia più alta a una traccia a energia più bassa:questo è ciò che fa brillare l'idrogeno in un tubo di vetro. Ha ottenuto l'idrogeno giusto, ma il suo modello era un po' difettoso.
"Il modello non è riuscito a prevedere il valore corretto delle energie dello stato fondamentale degli atomi a molti elettroni e delle energie di legame delle molecole, anche per i più semplici sistemi a 2 elettroni, come l'atomo di elio o una molecola di idrogeno, "dice Anatoly Svidzinsky, un professore dell'Institute for Quantum Science and Engineering presso Texas A&M, in un'intervista via e-mail. "Così, già nel 1913, era chiaro che il modello di Bohr non è del tutto corretto. Anche per l'atomo di idrogeno, il modello di Bohr predice erroneamente che lo stato fondamentale dell'atomo possiede un momento angolare orbitale diverso da zero."
Quale, Certo, potrebbe non avere molto senso per te se non sei un fisico quantistico. Però, Il modello di Bohr fu accelerato per ricevere un Premio Nobel per la fisica nel 1922. Ma anche se Bohr stava cementando la sua reputazione nel mondo della fisica, gli scienziati stavano migliorando il suo modello:
"Il modello di Bohr per l'atomo di idrogeno fu migliorato da Arnold Sommerfeld nel 1916, " dice Herschbach. "Ha trovato orbite ellittiche che rappresentavano linee spettrali vicine a quelle che provenivano da orbite circolari. Il modello di Bohr-Sommerfeld per l'atomo di idrogeno è fondamentale, ma quantistica e relatività sono diventati aspetti principali."
Tra il 1925 e il 1928, Werner Heisenberg, Massimo Nato, Wolfgang Pauli, Erwin Schrodinger e Paul Dirac hanno sviluppato questi aspetti ben oltre il modello atomico di Bohr, ma il suo è di gran lunga il modello di atomo più riconosciuto. I modelli atomici che la fisica quantistica ci ha fornito sembrano meno un sole circondato da pianeti elettronici e più simili all'arte moderna. È probabile che usiamo ancora il modello di Bohr perché è una buona introduzione al concetto di atomo.
"Nel 1913, Il modello di Bohr ha dimostrato che la quantizzazione è una strada giusta da percorrere nella descrizione del micromondo, " dice Svidzinsky. "Così, Il modello di Bohr ha mostrato agli scienziati una direzione per la ricerca e ha stimolato l'ulteriore sviluppo della meccanica quantistica. Se conosci il percorso, poi prima o poi troverai la giusta soluzione al problema. Si può pensare al modello di Bohr come a uno dei segnali di direzione lungo un sentiero escursionistico nel mondo quantistico".
Ora è interessanteIl padre di Niels Bohr, Christian Bohr, è stato nominato per tre diversi premi Nobel per la fisiologia della medicina, anche se non ha mai vinto.