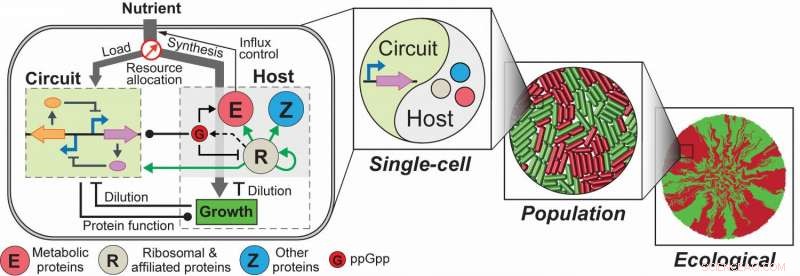
Interazioni circuito-host e loro conseguenze su diverse scale. I circuiti sintetici e l'host formano una dinamica, relazione multistrato che coinvolge interazioni generiche e specifiche del sistema, quindi regolando reciprocamente i comportamenti gli uni degli altri. Poiché l'accoppiamento circuito-ospite altera la crescita cellulare, le influenze dell'accoppiamento possono propagarsi attraverso le scale, che influenzano la dinamica delle singole cellule, comportamenti della popolazione e l'emergere dell'ecologia spaziale. Qui, le cellule rosse e verdi rappresentano due fenotipi distinti causati dalle interazioni circuito-ospite; le macchie verdi e rosse sono ammassi cellulari formati dai due fenotipi. Credito: Microbiologia della natura , DOI:10.1038/s41564-017-0022-5
Negli ultimi 17 anni, scienziati e ingegneri hanno sviluppato circuiti genetici sintetici in grado di programmare la funzionalità, prestazione, e comportamento delle cellule viventi. Analogamente ai circuiti integrati che sono alla base di una miriade di prodotti elettronici, circuiti genici ingegnerizzati possono essere utilizzati per generare dinamiche definite, ricablare reti endogene, percepire gli stimoli ambientali, e produrre preziose biomolecole.
Questi circuiti genici sono molto promettenti nelle applicazioni mediche e biotecnologiche, come combattere i super insetti, produzione di biocarburanti avanzati, e produzione di materiali funzionali.
Ad oggi, la maggior parte dei circuiti sono costruiti attraverso un metodo per tentativi ed errori, che si basa molto sull'intuizione di un designer ed è spesso inefficiente, ha detto Ting Lu, professore associato di bioingegneria dell'Università dell'Illinois. "Con l'aumento della complessità del circuito, la mancanza di linee guida di progettazione predittiva è diventata una sfida importante nella realizzazione del potenziale della biologia sintetica, " disse Lu, che è anche affiliato al Carl R. Woese Institute for Genomic Biology and Physics Department dell'Illinois.
I ricercatori si sono rivolti alla modellizzazione quantitativa per affrontare questa sfida di progettazione di circuiti genici. I modelli tipici considerano i circuiti genici come entità isolate che non interagiscono con i loro ospiti e si concentrano solo sui processi biochimici all'interno dei circuiti, ha notato Lu.
"Anche se di grande valore, l'attuale paradigma di modellazione è spesso incapace di quantificare, o anche qualitativamente a volte, descrivendo i comportamenti del circuito, " ha detto. "Crescenti prove sperimentali hanno suggerito che i circuiti e il loro ospite biologico sono intimamente connessi e il loro accoppiamento può avere un impatto significativo sui comportamenti dei circuiti".
Lu e i suoi studenti laureati, Chen Liao e Andrew Blanchard, ha recentemente affrontato la sfida costruendo un quadro di modellizzazione integrato per descrivere e prevedere quantitativamente i comportamenti dei circuiti genici. Usando Escherichia coli ( E. coli ) come ospite modello, la struttura consiste in una descrizione grossolana ma meccanicistica della fisiologia dell'ospite che implica il partizionamento dinamico delle risorse, accoppiamento circuito-host multistrato, e un modulo cinetico dettagliato dei circuiti esogeni.
La squadra ha dimostrato che, dopo la formazione, il framework è stato in grado di catturare e prevedere un ampio set di dati sperimentali riguardanti l'ospite e la semplice sovraespressione del gene. Ad esempio, hanno scoperto che gli effetti mediati da ppGpp sono la chiave per comprendere l'espressione genica costitutiva sotto i cambiamenti ambientali, compresi i cambiamenti sia dei nutrienti che degli antibiotici. Il team ha anche dimostrato l'utilità della piattaforma applicandola per esaminare un circuito di feedback che modula la crescita la cui dinamica è qualitativamente alterata da accoppiamenti circuito-host e rivelando i comportamenti di un interruttore a levetta su scale dalla dinamica della singola cellula alla struttura della popolazione e al ecologia spaziale.
Sebbene la struttura di Lu sia stata stabilita utilizzando E. coli come host modello, ha il potenziale per essere generalizzato per descrivere più organismi ospiti. "Per esempio, l'abbiamo trovato, variando un solo parametro, il framework ha previsto con successo diverse metriche host chiave, compreso il rapporto RNA-proteina, contenuto di RNA per cellula, e il tasso medio di allungamento del peptide, per Salmonella typhimurium e Streptomyces coelicolor , " disse Lu.
Secondo Lu, questo lavoro fa avanzare la comprensione quantitativa dei comportamenti dei circuiti genici, e facilita la trasformazione della progettazione della rete genica dalla costruzione per tentativi ed errori all'ingegneria razionale in avanti. Illustrando sistematicamente i processi cellulari chiave e le interazioni circuito-ospite multistrato, getta ulteriore luce sulla biologia quantitativa verso una migliore comprensione della complessa fisiologia batterica.
Il lavoro è descritto nell'articolo di Lu, "Un framework di modellizzazione circuito-host integrativo per prevedere i comportamenti della rete di geni sintetici, " pubblicato il 25 settembre, numero 2017 di Microbiologia della natura .