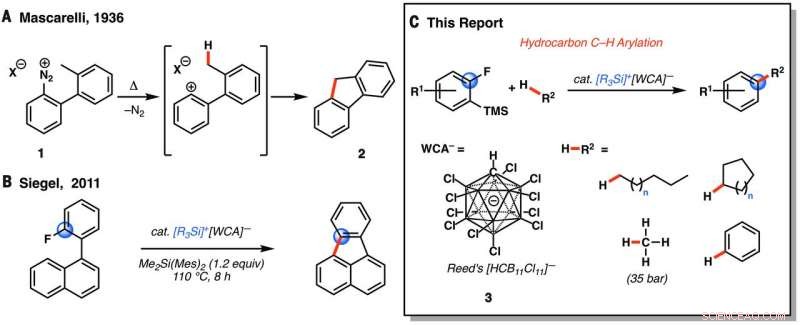
Reazioni che coinvolgono presunti cationi fenile. (A) La reazione di Mascarelli (12). (B) Reazione intramolecolare di Friedel-Crafts di Siegel dei fluoruri arilici (15). (C) La nostra doppia strategia di funzionalizzazione C–F/C–H. R =etile o triisopropile; R1 =arile, alchile, alogenuro, o silil etere; WCA, anione debolmente coordinante; TMS, trimetilsilile; me, mesitile; Me, metile; gatto., catalitico. Credito:(c) Scienza (2017). DOI:10.1126/science.aam7975
(Phys.org)—Un team di chimici dell'Università della California ha sviluppato un modo più economico per funzionalizzare gli alcani non attivati (idrocarburi come l'etano, metano e propano) utilizzando catalizzatori molto più abbondanti. Nel loro articolo pubblicato sulla rivista Scienza , il team descrive il progetto di reazione che hanno creato che supera le sfide precedenti relative ai profili di reattività ad alta energia.
Attualmente, gli alcani non attivati sono considerati difficili da funzionalizzare:la maggior parte utilizza un approccio che prevede l'apertura di legami idrocarburici C-H utilizzando un processo che coinvolge metalli preziosi e costosi. In questo nuovo sforzo, il team ha invece trovato un modo per utilizzare silicio e boro come catalizzatori. Questo è importante perché l'industria ha bisogno di convertire gli alcani come il gas naturale e il petrolio in prodotti più preziosi.
Gli alcani reagiscono relativamente facilmente alle alte temperature, come si vede nei motori a combustione interna, ma tali reazioni sono considerate estremamente difficili da controllare. Funzionalizzare gli alcani consente di ottenere di più da essi oltre al loro potenziale energetico, permette di estrarre componenti che possono essere utilizzati come precursori per la creazione di sostanze chimiche rare che, in alcuni casi, sono notevolmente più preziosi. Poiché sono relativamente inerti, e i legami tra il carbonio e l'idrogeno sono forti, sono difficili da funzionalizzare. Per spezzare quei forti legami, la squadra ne ha fatte di ancora più forti.
Il gruppo è iniziato con anelli di benzene, preparandoli con sostituti del silicio e del fluoro. Successivamente hanno innescato un ciclo utilizzando silicio attivato aggiuntivo, che hanno accoppiato con il carborano, questo ha costretto il fluoro a creare un intermedio arilico che era in grado di rompere i legami alcani C-H (che includevano in particolare il metano). L'anello risultante ha quindi rilasciato silicio, che ha mantenuto la reazione in corso. Il team nota che la reazione può essere condotta in intervalli di temperatura da 30° a 100°C. Non è ancora chiaro se il processo possa essere ridimensionato per essere efficace in termini di costi, ma se è così, potrebbe portare a un calo dei prezzi per alcuni prodotti, in particolare quelli basati su gas naturale sempre più abbondante.
Il gruppo dovrebbe fare una presentazione del proprio lavoro alla prossima riunione dell'ACS.
© 2017 Phys.org