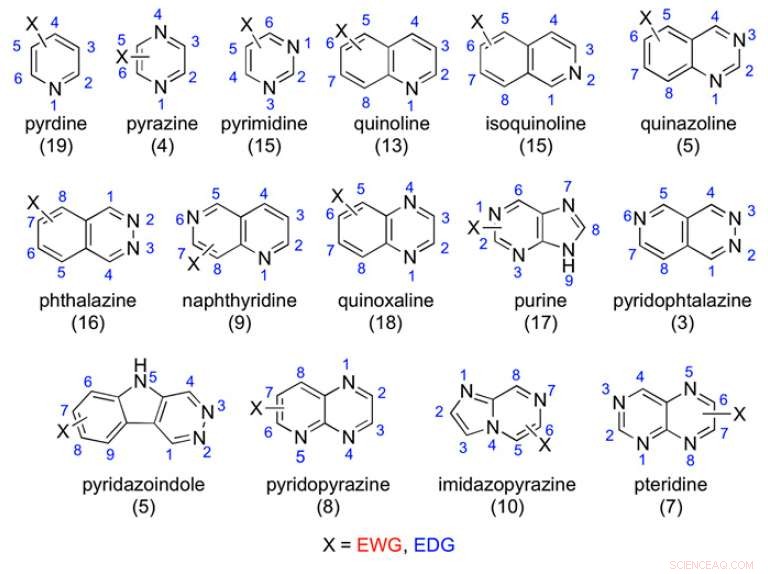
Esempi degli scaffold aza-aromatici studiati:tra parentesi è riportato il numero di composti testati. Credito:(c) Atti dell'Accademia Nazionale delle Scienze (2017). DOI:10.1073/pnas.1618881114
(Phys.org)—La progettazione di farmaci prevede prove ed errori guidati. Il modo in cui il corpo metabolizza un particolare farmaco è importante per determinare l'efficacia del farmaco. Ci sono stati molti studi per capire come gli xenobiotici interagiscono con il citocromo P450, un'importante classe di enzimi nel metabolismo dei farmaci, ma sono state fatte poche ricerche per comprendere il metabolismo dell'aldeide ossidasi (AOX). AOX, localizzato nel fegato, svolge un ruolo importante nel metabolismo dei farmaci; però, molti potenziali farmaci finiscono per fallire durante gli studi in fase avanzata a causa della loro interazione con l'AOX.
Per comprendere meglio la relazione struttura-metabolismo tra gruppi funzionali e AOX, nonché per stabilire linee guida generali per il metabolismo dei farmaci non citocromo P450, ricercatori dell'Università di Perguia in Italia hanno condotto test su 198 composti con scaffold aza-aromatici per vedere quali sono stati ossidati dall'AOX. Per di più, hanno testato 75 scaffold ammidici per determinare quali erano idrolizzati. Hanno scoperto che i fattori elettronici e l'ingombro sterico hanno influenzato l'orientamento della molecola nel sito attivo di MoCo, che ha determinato se il composto è stato metabolizzato da AOX. Il loro lavoro appare nel Atti dell'Accademia Nazionale delle Scienze .
L'AOX è un enzima localizzato nel fegato che tende ad ossidare i composti aza-aromatici come metabolita di fase I. Gli studi hanno dimostrato che AOX attiva il carbonio non sostituito orto all'azoto sull'eterociclo aza. Poiché questo è il carbonio più elettropositivo dell'anello aromatico, la densità elettronica probabilmente gioca un ruolo nell'attivazione di AOX. Ma questi studi, così come altri che guardano al metabolismo AOX, si basavano su un numero limitato di molecole che non consente di dedurre un modello generale di relazione struttura-metabolismo.
Nello studio attuale, Lepri et al. testato 198 composti aza-aromatici per vedere se fossero ossidati da AOX. Ciascuno di questi aveva tipiche impalcature aza-aromatiche con variazioni sui sostituenti elettrontrattori e donatori di elettroni. Hanno acquisito o realizzato questo catalogo di composti e poi hanno condotto studi sul metabolismo in vitro utilizzando il citosol epatico umano.
I calcoli DFT sono stati utilizzati per chiarire gli effetti della densità elettronica sull'attività AOX. Il sito del metabolismo sul composto aromatico tendeva a corrispondere al carbonio non sostituito più elettropositivo, come previsto. Inoltre, sono stati utilizzati studi di calcolo per condurre l'analisi di aggancio dei composti nel sito attivo di AOX.
Gli autori hanno trovato alcune tendenze per il sito del metabolismo; però, queste tendenze sono complicate da diversi fattori. L'impalcatura piridinica era l'unica che, come classe di impalcature, non era suscettibile al metabolismo degli AOX. Gli altri gruppi dipendevano fortemente dalla densità elettronica su particolari carboni o, come gli autori hanno trovato con composti come le chinossaline e alcuni composti biciclici, l'impedimento sterico nel sito attivo ha impedito il metabolismo degli AOX.
Lepri et al. anche testato 73 composti ammidici per vedere se AOX ha idrolizzato il legame ammidico. Generalmente, se c'era un gruppo elettron attrattore in posizione orto sull'analina, quindi AOX non l'ha ossidato. Se esistesse un gruppo donatore di elettroni, poi lo ha fatto. Le versioni meta e para dei gruppi donatori di elettroni e prelevatori di elettroni non erano suscettibili al metabolismo dell'AOX.
Gli effetti dell'esposizione erano una componente importante per stabilire se un composto fosse metabolizzato da AOX. Ciò ha a che fare con l'orientamento della molecola verso il centro MoCo nel sito attivo dell'AOX. Alcuni gruppi ingombranti non hanno portato a nessuna attività dove ci si aspettava uno basato su studi computazionali. Inoltre, l'idrofobicità ha anche influenzato il modo in cui il composto ha interagito con il sito attivo. Quando il carbone reattivo è esposto al centro MoCo, quindi il composto viene facilmente metabolizzato. Ma, quando la porzione non reattiva del composto è orientata verso il centro MoCo, quindi è meno probabile che il composto venga ossidato o idrolizzato.
Gli autori sottolineano che da questi esperimenti "emerge che non è affatto semplice prevedere se un composto sia o meno un substrato di AOX". La difficoltà sta nel comprendere la reattività del carbonio elettrofilo sul composto e come quel particolare composto si orienterà nel sito attivo dell'enzima. Però, questo studio fornisce un punto di partenza per ulteriori studi e tecniche di modellazione più sofisticate.
© 2017 Phys.org