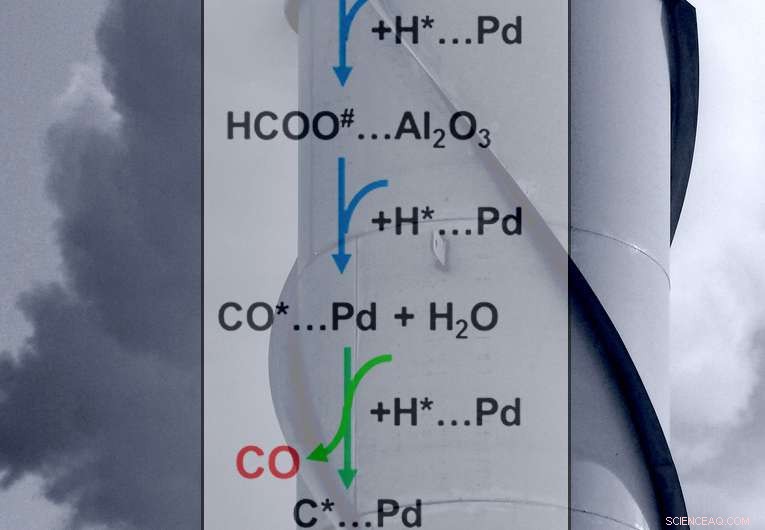
Le frecce verdi mostrano il passaggio fondamentale nel controllo dei prodotti finali delle reazioni:metano o monossido di carbonio. Credito:Scott Butner
E se potessimo trasformare l'anidride carbonica, CO2, in una risorsa preziosa? L'utilizzo della CO2 come materia prima per creare combustibili o altre sostanze chimiche offrirebbe vantaggi economici e ambientali. La sfida è progettare processi efficaci che producano solo la sostanza chimica desiderata:metano o monossido di carbonio. Come mai? Gli scienziati non avevano una chiara comprensione dei passaggi fondamentali nel meccanismo di reazione. Scienziati del Pacific Northwest National Laboratory, guidato dal dottor Janos Szanyi, determinato quel formiato (HCOO-), uno ione spesso trascurato, era un intermedio critico nel processo di conversione della CO2. L'equilibrio nei tassi di conversione del formiato e degli intermedi di monossido di carbonio determina quali sostanze chimiche vengono prodotte.
"Questo studio ci fornisce informazioni cruciali per utilizzare una materia prima facilmente disponibile, CO2, e trasformarlo in qualcosa di utile, un intermedio chimico, monossido di carbonio, o un vettore energetico, metano. Questo intermedio può essere utilizzato per la produzione di idrocarburi superiori, o combustibili, ", ha detto Szanyi.
Per anni, alcuni consideravano il formato nient'altro che un passante, una molecola che non ha contribuito alla reazione. Ora, la squadra ha dimostrato che il formato è davvero vitale. Comprendere i passaggi, e il ruolo dei formati, consente agli scienziati di progettare un catalizzatore selettivo che pompa le sostanze chimiche desiderate. Comprendere le fasi della reazione fornisce agli scienziati informazioni cruciali per controllare la reazione. Ulteriore, il lavoro pone fine a una lunga controversia sul ruolo dei formiati sulla superficie del catalizzatore.
In questo studio, un team del Pacific Northwest National Laboratory ha determinato i fattori che controllano la selettività di un catalizzatore per l'idrogenazione della CO2 a monossido di carbonio o metano. Hanno usato una nuova combinazione di esperimenti FTIR di trasmissione operando e SSITKA (Fourier Transform Infrared Spectroscopy/Steady State Isotopic Transient Kinetic Analysis).
Hanno determinato il comportamento dei principali intermedi (formati e monossido di carbonio) sulla superficie del catalizzatore. Per la formazione di monossido di carbonio, il passaggio determinante per il tasso è la conversione, o riduzione, di formiato adsorbito all'interfaccia del catalizzatore metallico di palladio e del supporto di ossido di alluminio. Per la formazione di metano, la fase determinante per la velocità (vedere le frecce verdi nella figura) consiste nell'aggiungere idrogeno al monossido di carbonio adsorbito. L'equilibrio tra le velocità di riduzione del formiato assorbito e la metanazione del monossido di carbonio determina la selettività del catalizzatore. Questo è, la selettività ruota attorno alla velocità con cui gli intermedi sulla superficie raccolgono idrogeno, creando monossido di carbonio o metano.
Avendo determinato gli aspetti chiave della reazione, il team ha progettato tre catalizzatori con diverse distribuzioni di palladio. La quantità di palladio sulla superficie, hanno trovato, è un altro aspetto fondamentale nella scelta dei prodotti. Il catalizzatore con meno palladio produceva sia monossido di carbonio che metano, con maggiore selettività per il monossido di carbonio. In contrasto, è stata osservata una selettività superiore all'80% verso la formazione di metano sul catalizzatore con il carico di metallo più elevato.
Il team sta ora modificando l'ambiente intorno al sito attivo del catalizzatore per regolarne la selettività. Questo lavoro ha lo scopo di ridurre la quantità di prodotti indesiderati rilasciati. Inoltre, il team sta sviluppando metodi per preparare catalizzatori a singolo atomo per aumentare l'efficienza dei metalli preziosi coinvolti.