Questa molecola è stata generata in situ per estrazione di idruro da n fluorobenzene. Credito:Pacific Northwest National Laboratory
L'idrogeno è l'elemento più abbondante nell'universo. La molecola di diidrogeno, con un legame H-H, è uno dei più semplici e flessibili in chimica. La scissione di un legame diidrogeno per produrre o immagazzinare energia richiede la progettazione del catalizzatore con il perfetto equilibrio di proprietà per ottenere la reattività desiderata. Inoltre, la capacità di far sì che quella molecola si ricomponga e di controllare la velocità di assemblaggio e smontaggio è importante nella produzione di combustibili puliti. Morris Bullock e i suoi colleghi del Pacific Northwest National Laboratory hanno ottenuto il controllo sulla velocità di scissione e riassemblaggio di una molecola di diidrogeno.
Nella continua ricerca di una produzione di combustibile pulito, gli scienziati hanno studiato modi semplici per scindere eteroliticamente la molecola di idrogeno in due prodotti irregolari. Comprendere le proprietà della scissione del legame diidrogeno eterolitico e controllare la posizione e l'energia del protone risultante e dell'idruro caricato negativamente è importante per la progettazione di nuovi catalizzatori per celle a combustibile e altre fonti di energia pulita.
Il legame diidrogeno è il più semplice in chimica ma offre una flessibilità nel modo in cui il legame viene rotto. Può essere rotto in due modi diversi, omoliticamente o eteroliticamente, in due frammenti identici o in due frammenti con carica diversa, un protone e un idruro. La scissione eterolitica è la rottura della coppia di elettroni di legame in due prodotti irregolari. Questo è un processo comune nell'uso dell'idrogeno nelle celle a combustibile e nei processi biologici che si verificano in natura in cui gli enzimi ossidano l'idrogeno. La scissione eterolitica inversa è il processo di prendere questi frammenti irregolari e ricostruirli nella loro struttura originale; questo è, combinando il protone e l'idruro e creando diidrogeno.
Prima di questo studio, Bullock e i suoi colleghi hanno studiato come i legami diidrogeno si rompono e si riformano in una molecola di diidrogeno. "Quello che stiamo cercando di fare è trovare le giuste caratteristiche elettroniche in modo che l'energia necessaria per la scissione sia bassa, "dice Bullock, uno scienziato della catalisi.
Progettare questa molecola è un atto di bilanciamento. Le precedenti iterazioni di queste molecole o erano legate troppo fortemente al catalizzatore dopo la scissione o erano troppo deboli per legarsi al catalizzatore. In risposta, Gli scienziati del PNNL hanno creato una serie di catalizzatori a base di molibdeno, per cui la velocità di sfaldamento e riassemblaggio H-H potrebbe essere sistematicamente variata.
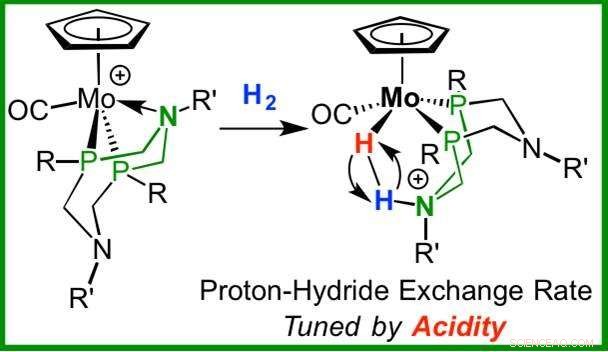
Inoltre, Bullock ei suoi colleghi hanno dimostrato che esiste un meccanismo per controllare il tasso di scissione eterolitica reversibile. Utilizzando la spettroscopia di risonanza magnetica nucleare al PNNL, hanno osservato la reazione mentre si verificava. Ulteriore, controllavano il tasso di scissione modificando sistematicamente le caratteristiche elettroniche dei complessi metallici. Alcuni di questi legami si scindono e si ricompongono a circa 10 milioni di volte al secondo a temperatura ambiente. Modificando l'acidità di questi complessi, il tasso di scissione eterolitico reversibile può essere modificato di un fattore 10, 000.
La comprensione delle proprietà termodinamiche e cinetiche della scissione del legame diidrogeno eterolitico e il controllo del trasferimento del protone e dell'idruro sono di fondamentale importanza per la progettazione di nuovi catalizzatori. Il prossimo passo è determinare come ottenere la scissione dei legami H-H e controllare la consegna di protoni e idruri dopo la rottura del legame H-H.