Credito:Wiley
Per una terapia del cancro efficiente con pochi effetti collaterali, il farmaco attivo dovrebbe raggiungere selettivamente un'alta concentrazione nel tumore. Nel diario Angewandte Chemie , gli scienziati hanno introdotto un nuovo approccio, in cui due componenti sinergici del farmaco sono combinati in un dimero. Questo dimero può essere incorporato in nanotrasportatori polimerici a concentrazione eccezionalmente elevata. I componenti vengono attivati quando il dimero viene suddiviso all'interno del tumore. Inoltre, consentono l'uso di due diverse tecniche di imaging.
Le micelle polimeriche sono i più importanti nanotrasportatori utilizzati nel trattamento dei tumori. Nonostante il miglioramento dei sistemi di trasporto, molte sfide devono ancora essere superate:carico insufficiente, rilascio prematuro del farmaco, nessuna capacità di monitorare la distribuzione del farmaco, e limitato accumulo del farmaco all'interno del tessuto tumorale. Longjiang Zhang, Guizi Zhu, Xiaoyuan Chen, e il loro team hanno affrontato questi problemi dall'altra direzione. Invece di migliorare il trasportatore, hanno migliorato il carico.
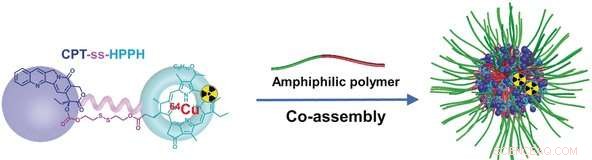
Gli scienziati del National Institutes of Health di Bethesda, STATI UNITI D'AMERICA, e l'Università di Nanchino, Cina, hanno usato un trucco semplice ma efficace:hanno collegato due farmaci, camptotecina e uno speciale fotosensibilizzatore, per fare un dimero. Le micelle possono essere caricate in modo molto efficiente con una quantità insolitamente grande del carico dimerico (59%). I dimeri sono meno idrofili dei loro singoli componenti, permettendo loro di essere introdotti più facilmente nell'interno idrofobo delle micelle. Per la stessa ragione, i dimeri non escono dalle micelle mentre viaggiano attraverso i vasi sanguigni. Questo riduce gli effetti collaterali indesiderati.
Entrambi i componenti del dimero inizialmente inattivo sono collegati da un ponte disolfuro che può essere rotto solo da una cascata di reazione dipendente dal glutatione. Il glutatione è una piccola proteina presente in alta concentrazione in molti tumori. Entrambi i farmaci vengono attivati solo dopo che il dimero si è diviso all'interno delle cellule tumorali.
Quando l'area del tumore viene irradiata con luce laser, il fotosensibilizzatore converte l'ossigeno normale in ossigeno singoletto altamente reattivo, che danneggia la cellula e provoca una carenza di ossigeno. La camptotecina inibisce il fattore 1α, che aiuta le cellule a resistere alla carenza di ossigeno. Questo aumenta l'effetto citotossico del fotosensibilizzante. Un altro effetto della camptotecina è che danneggia il DNA delle cellule tumorali.
Inoltre, il fotosensibilizzante è un colorante fluorescente e può legare il radioisotopo rame-64, che consente la visualizzazione sia con l'imaging a fluorescenza che con la tomografia a emissione di positroni (PET). Il PET quantitativo consente un monitoraggio preciso del dimero, così come la conferma della sua farmacocinetica e biodistribuzione in vivo.
Esperimenti con colture cellulari e topi tumorali hanno dimostrato che questo nuovo metodo ha migliorato significativamente il trasporto e l'accumulo del farmaco nei tumori con effetti collaterali significativamente inferiori, mentre riduce il tumore in misura significativamente maggiore rispetto alla somministrazione dei singoli componenti non legati.