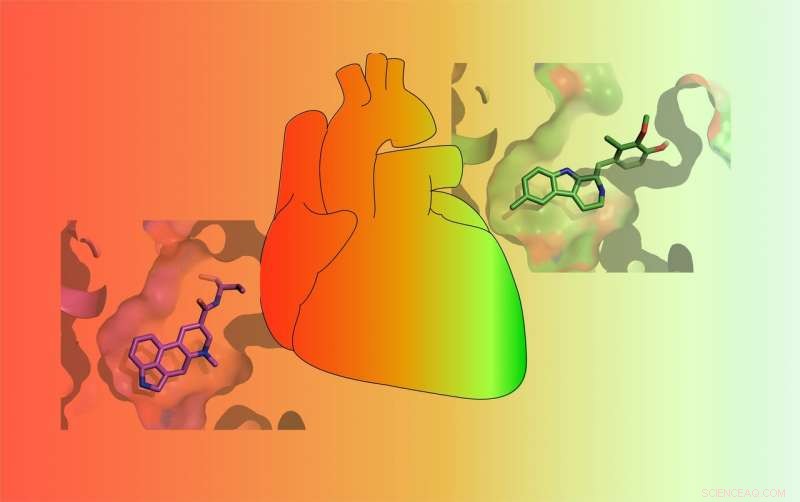
I farmaci variano nella loro capacità di attivare il recettore della serotonina 5-HT2B. Alcuni farmaci (ROSSO) attivano fortemente il recettore e causano una cardiopatia valvolare potenzialmente pericolosa per la vita, mentre altri lo attivano solo debolmente (VERDE) e hanno meno probabilità di causare gravi effetti collaterali. Credito:Roth Lab
serotonina, noto come neurotrasmettitore della "felicità", è una sostanza chimica presente nel corpo responsabile delle sensazioni di benessere. Ma la serotonina non è l'unica sostanza chimica che si lega ai 13 recettori della serotonina presenti sulla superficie delle cellule. Lontano da esso. Molti farmaci approvati si legano anche ai recettori della serotonina. E uno di questi recettori, chiamato 5-HT2BR, ha reso gli sviluppatori di farmaci molto infelici. Questo perché alcuni farmaci che curano il morbo di Parkinson, emicranie, tumori ipofisari, e l'obesità sono stati progettati per colpire altri recettori cellulari ma anche attivare 5-HT2BR, portando a una malattia cardiaca valvolare pericolosa per la vita. Di conseguenza, molti di questi farmaci sono stati ritirati dal mercato.
Ora, per la prima volta, Gli scienziati della UNC School of Medicine hanno capito esattamente perché un farmaco si lega al 5-HT2BR e attiva il recettore per causare problemi cardiaci, mentre farmaci molto simili non lo fanno. Hanno anche scoperto perché un terzo farmaco agisce come un antagonista 5-HT2BR—blocca l'attività del recettore—mentre il noto farmaco allucinogeno LSD non lo fa.
Pubblicato in Biologia strutturale e molecolare della natura , questa ricerca fornisce agli sviluppatori di farmaci le informazioni necessarie su questo recettore della serotonina e altri simili.
"Per molto tempo, abbiamo bisogno di sapere esattamente come questo recettore e altri si legano a vari composti se vogliamo progettare farmaci più sicuri ed efficaci, " ha detto l'autore senior Bryan L. Roth, dottore, dottorato di ricerca, il Michael Hooker Distinguished Professor di Protein Therapeutics e Translational Proteomics nel Dipartimento di Farmacologia. "Risolvere le strutture cristalline di questi recettori della serotonina legati a diversi composti è il primo passo essenziale necessario per creare farmaci migliori, non solo per le suddette condizioni ma per molte altre tra cui la schizofrenia, ansia, e depressione".
Negli esperimenti condotti da John McCorvy, dottorato di ricerca, che era un borsista post-dottorato nel laboratorio Roth durante questa ricerca, gli scienziati hanno faticosamente indotto i recettori a condensare in un reticolo cristallino strettamente compresso mentre i recettori erano attaccati a un farmaco. Quindi hanno sparato raggi X al cristallo per calcolare la struttura del recettore dai modelli di diffrazione risultanti. McCorvy e colleghi lo hanno fatto più volte per cristallizzare i recettori della serotonina legati a diversi composti, che era stato impossibile per decenni perché i recettori sono notoriamente proteine volubili:piccole, fragile, e tipicamente in movimento mentre si legano ai composti.
Gli scienziati hanno quindi utilizzato altre tecniche sperimentali delineate nel documento per mostrare con precisione come ciascun farmaco ha attivato o meno il recettore.
In una serie di esperimenti, McCorvy e colleghi hanno dimostrato che la metilergonovina, il principio attivo di un farmaco per l'emicrania, si lega a una particolare regione di 5-HT2BR e la attiva. La metilergonovina è un agonista. Ma il suo composto genitore, metisergide, non attiva il recettore, rendendolo un antagonista. Il laboratorio di Roth ha scoperto che la differenza tra i due farmaci è solo un atomo di carbonio e alcuni atomi di idrogeno. Insieme sono chiamati metile. Questo minuscolo metile risulta essere il colpevole dei problemi alle valvole cardiache legati al 5-HT2BR.
In una seconda serie di esperimenti, hanno mostrato perché la lisuride, il farmaco per il Parkinson, non attiva il 5-HT2BR ma l'LSD lo fa. La differenza nel sito di legame è solo un singolo atomo di azoto e stereochimica, essenzialmente lo spazio tra il farmaco e il recettore che gioca un ruolo nel modo in cui qualsiasi farmaco potrebbe adattarsi al recettore per attivare o interrompere l'attività cellulare.
interessante, la lisuride e l'LSD si legano al recettore della serotonina nella regione tipica che gli scienziati si aspetterebbero. Ma la chimica di come questi due farmaci si legano in quel sito non spiega i loro effetti molto diversi sulle cellule e sulle persone. McCorvy e colleghi hanno scoperto che la lisuride è anche incuneata in un'altra parte del recettore chiamata tasca estesa di legame, ma il contatto di lisuride non è forte. L'LSD d'altra parte si lega fortemente alla tasca di rilegatura estesa, rendendo l'LSD un agonista molto forte:attiva il 5-HT2BR (così come altri recettori). LSD lo fa reclutando una proteina chiamata beta-arrestin2. Gli scienziati chiamano questo processo "attivazione della via -arrestina, " ed è stato implicato in vari effetti collaterali legati alle terapie.
Questi risultati aiuteranno i progettisti di farmaci a evitare l'attivazione di 5-HT2BR durante la progettazione di farmaci per colpire altre proteine recettrici, comunemente indicate come recettori accoppiati a proteine G, o GPCR. Al contrario, questa ricerca aiuterà gli sviluppatori di farmaci che vogliono inibire l'attivazione di 5-HT2BR per trattare la cardiopatia valvolare e altri disturbi.
"Fondamentalmente, cristallizzando le strutture del 5-HT2BR legato a diversi farmaci comuni, abbiamo scoperto che non esiste un meccanismo attraverso il quale il recettore viene attivato, "Ha detto McCorvy. "Ce ne sono diversi." Per creare un preciso, sicuro, e farmaci efficaci, gli scienziati vogliono sfruttare solo i percorsi cellulari importanti per il trattamento della condizione a cui sono interessati. McCorvy ha aggiunto, "Questo è l'avanguardia dello sviluppo di farmaci".