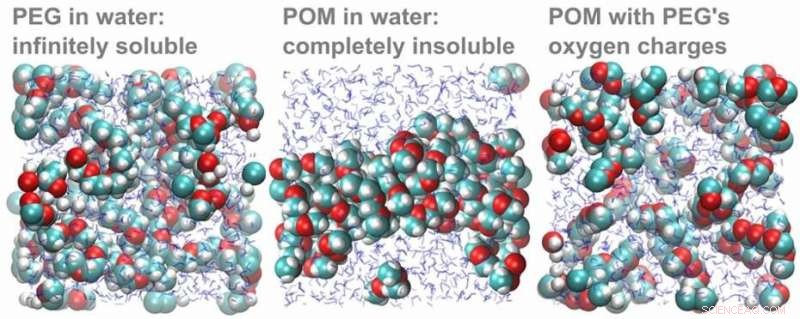
Simulazioni al computer di molecole PEG e POM in acqua. A sinistra:le molecole di PEG si dissolvono in acqua. Centro:le molecole di POM non si dissolvono in acqua, ma si uniscono in un grumo. A destra:quando la carica degli atomi di ossigeno viene modificata al valore in PEG, le molecole di POM si dissolvono rapidamente. Credito:HIMS
Le molecole di polietere tendono a dissolversi meglio in acqua poiché contengono più ossigeno e meno atomi di carbonio. Ma ci sono eccezioni molto controintuitive a questa tendenza, il più noto è il POM di plastica ampiamente utilizzato. Ha il più alto rapporto ossigeno/carbonio possibile ma è completamente insolubile. Nel numero attuale di Comunicazioni sulla natura , ricercatori dell'Università di Amsterdam e dell'Istituto Max Planck per la ricerca sui polimeri di Magonza hanno ora fornito una spiegazione definitiva.
I ricercatori in particolare hanno fatto luce sulle differenze di solubilità tra i polieteri PEG (polietilenglicole) e POM (poliossimetilene) che sono ovunque nella nostra vita quotidiana. PEG ha molte applicazioni in soluzioni acquose per scopi farmaceutici e cosmetici, ad esempio nelle creme da barba e nella cura della pelle. Il POM è un materiale plastico onnipresente:molti oggetti della vita quotidiana sono fatti di POM, così come le coloratissime clip Keck per il collegamento della vetreria, ben noto a ogni chimico.
Sebbene questi due polieteri siano molto simili a livello molecolare, hanno solubilità molto controintuitive in acqua. PEG (unità ripetitiva -CH 2 -CH 2 -O-) è perfettamente solubile, e ogni studente di chimica può dirti perché:gli atomi di ossigeno nel PEG sono leggermente caricati negativamente, che li rende idrofili. Questa spiegazione sembra essere confermata dal polimero comparabile PPG (polipropilenglicole, unità ripetitiva-CH 2 -CH 2 -CH 2 -O-):contiene relativamente meno atomi di ossigeno del PEG, ed è meno solubile, il che è perfettamente logico.
Ma aspetta:POM (unità ripetuta -CH 2 -O-) contiene relativamente più atomi di ossigeno del PEG, quindi la spiegazione suggerirebbe una maggiore solubilità. Però, Il POM è completamente insolubile!
L'induzione come principio esplicativo
Per svelare il mistero, i ricercatori di Amsterdam e Mainz hanno utilizzato una combinazione di spettroscopia infrarossa a femtosecondi, esperimenti di rilassamento dielettrico, calcoli quantistici e simulazioni al computer.
Gli esperimenti hanno mostrato che l'interazione acqua-polimero, che determina la solubilità, dipende fortemente dal rapporto carbonio/ossigeno del polimero. interessante, calcoli quantistici hanno mostrato che questa dipendenza non è dovuta alla distanza tra gli atomi di ossigeno nella catena polimerica. Questo è stato spesso proposto:l'idea è che la distanza ossigeno-ossigeno nel PEG si adatti meglio alla rete di legami idrogeno dell'acqua.
In Nature Communications i ricercatori ora mostrano che la relazione tra il rapporto carbonio/ossigeno e la solubilità implica l'induzione:gli atomi di ossigeno sono caricati negativamente perché ritirano la densità elettronica dagli atomi di carbonio vicini nella catena polimerica. In PEG, ogni atomo di ossigeno ha due atomi di carbonio vicini a sua completa disposizione per prelevare la densità elettronica. In POM, però, gli atomi di ossigeno devono "condividere" tra loro gli atomi di carbonio, e quindi può ritirare meno densità di elettroni. Di conseguenza, la carica negativa parziale sugli atomi di ossigeno in POM è circa il doppio rispetto a PEG. Il concetto di induzione spiegherebbe quindi perfettamente perché il POM è molto meno idrofilo, e quindi insolubile.
Elegante conferma
Per confermare che la differenza di carica parziale di ossigeno spiega effettivamente la differenza di solubilità, i ricercatori teorici del team hanno condotto un elegante esperimento al computer. Primo, hanno simulato una soluzione di molecole POM, che è precipitato come previsto. Quando poi hanno cambiato le cariche di ossigeno del POM con quelle calcolate per il PEG, le cariche POM-con-PEG si sono prontamente dissolte.
Oltre a risolvere un antico mistero legato ai materiali di uso quotidiano, i risultati mostrano che gli effetti di induzione possono avere un impatto maggiore sulle solubilità. Tenendo conto di questo effetto dovrebbe essere più facile prevedere le solubilità in futuro.