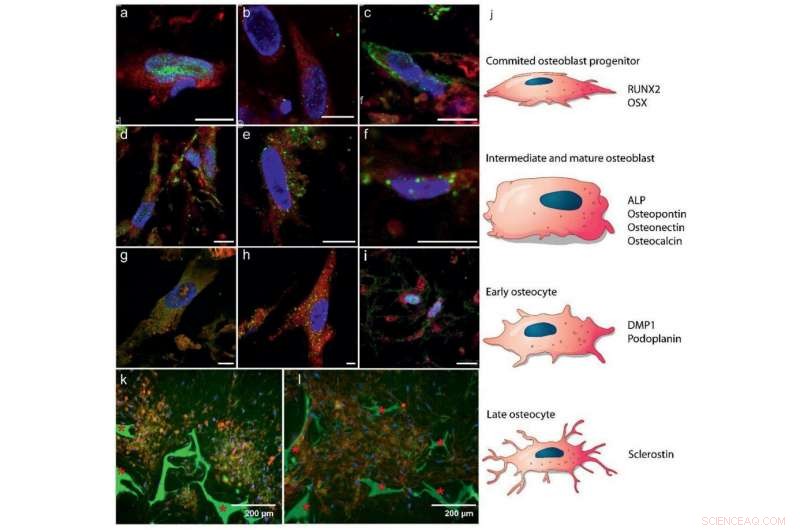
Differenziazione delle hBMSC in osteoblasti e osteociti:a–i) imaging immunoistochimico a fluorescenza che mostra marcatori per a–c) fasi iniziali della formazione degli osteoblasti, d–f) osteoblasti maturi, e g–i) sviluppo degli osteociti (glucosio 5,55 mm). Codice colore:citoplasma a cellule rosse, blu - nuclei cellulari, verde:a) RUNX2 (giorno 7), b) OSX (giorno 7), c) ALP (giorno 26), d) osteocalcina (giorno 26), e) osteopontina (giorno 26), f) osteonectina (giorno 21), g) DMP1 (giorno 28), h) podoplanina (giorno 28), e i) sclerostina (giorno 28). Barre della scala:10 µm. Vedi figura S4, Informazioni di supporto, per canali separati. j) Illustrazione schematica della differenziazione delle MSC in osteoblasti e osteociti, indicando in quale stato è prevista l'espressione della proteina in a–i. K, l) Immagini fluorescenti che indicano domini auto-organizzati di osteociti incorporati in una matrice mineralizzata dopo 8 settimane (25 mm di glucosio), k) co-localizzazione degli osteociti (sclerostina, rosso) e minerale (calceina, verde), e l) collagene (CNA35, rosso) e minerale (calceina, verde) * Indica l'impalcatura in fibroina di seta.
Immagina di usare le cellule staminali del tuo midollo osseo per far crescere un pezzo di tessuto osseo in laboratorio, dopo di che i medici esplorano quali farmaci hanno l'effetto desiderato sulle tue ossa. In questo modo, si realizzerebbe un piano di trattamento su misura per tutti, con l'approccio migliore chiaro in anticipo:la medicina personalizzata al suo meglio.
Quella visione del futuro non è più fantascienza ora che i ricercatori della Eindhoven University of Technology e del centro medico universitario di Radboud hanno effettivamente realizzato la prima parte:far crescere un pezzo di tessuto osseo realistico da cellule staminali umane. È il primo organoide dell'osso, una versione semplificata dell'originale, i ricercatori riferiscono oggi sulla rivista Materiali funzionali avanzati .
Immagine coerente
"Con questo, noi presentiamo, per la prima volta, il quadro completo della formazione ossea in fase iniziale, "dice Sandra Hofmann, professore associato in Bioingegneria ossea da TU/e. E questo è di grande importanza:come si formano le nostre ossa è ancora in gran parte un mistero. L'osso è un materiale molto complesso in cui interagiscono innumerevoli cellule e processi, e comprende un'ingegnosa matrice di collagene e minerale per fornire forza. Si sa molto sui singoli componenti, ma finora è mancato un quadro coerente.
Tre tipi di cellule svolgono il ruolo principale nella formazione dell'osso:gli osteoblasti (che costruiscono il tessuto osseo), osteoclasti (che asportano l'osso) e osteociti (che regolano la costruzione e la disgregazione dell'osso). "La maggior parte degli studi finora si è concentrata su uno di questi tipi di cellule, ma questa non è una buona rappresentazione del tessuto reale, ", afferma Hofmann. "Vi presentiamo qui un pezzo di osso intrecciato (osso in fase iniziale) che si è sviluppato da cellule staminali e contiene due tipi di queste cellule:osteoblasti e osteociti. Ora vediamo che possiamo creare ossa realistiche esclusivamente con questi due tipi di cellule".
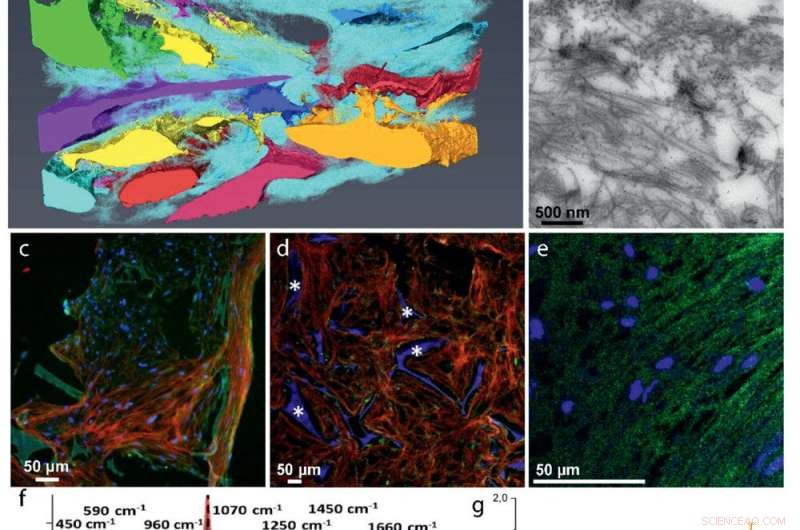
Sviluppo ECM:a) La ricostruzione FIB/SEM 3D mostra l'incorporamento delle cellule nella matrice di collagene (ciano). Le celle discrete sono rappresentate con colori diversi. b) Immagine TEM di una sezione di 70 nm che mostra la distribuzione casuale delle fibrille di collagene. Il collagene di tipo I è stato identificato mediante immunomarcatura. c-e) Immunoistochimica fluorescente che identifica le proteine chiave non collagene nella matrice collagena:c) Co-localizzazione dell'osteocalcina (verde) e del collagene (rosso). d) Distribuzione dell'osteopontina (verde) nella matrice di collagene (rossa). * Indica l'impalcatura in fibroina di seta. e) Co-localizzazione di DMP1 (verde) con la struttura del collagene (vedi Figura S5, Informazioni di supporto, per l'immagine del collagene). f–g) Microspettrometria Raman di matrici mineralizzate. f) Spettri Raman localizzati del collagene mineralizzato dell'osso di zebrafish in via di sviluppo (rosso), la co-coltura osteogenica 3D (blu), e osso umano di una femmina di 10 anni (grigio g) Rapporti minerale/matrice derivati da Raman di 4 tessuti mineralizzati di zebrafish (N =6, rosso), Coltura osteogenica 3D (N =7, verde), Femmina umana di 10 anni (N =1, grigio), e maschio umano di oltre 48 anni (N =7, Nero, tratto da rif. [36]). Le barre indicano le deviazioni standard del campione. h) Presentazione della mappa termica di una sezione trasversale FIB/SEM 3D che mostra fibrille di collagene disorganizzate con diversi gradi di mineralizzazione (Figura S10, Informazioni di supporto). Le frecce indicano le fibrille di collagene non mineralizzate (azzurro), la freccia indica la fibrilla di collagene mineralizzata (arancione). i) Immagine TEM che mostra le singole fibrille di collagene mineralizzate.
Diventare più saggi con il frugare molecolare
"E forse, cosa più importante, il nostro sistema si comporta proprio come l'osso in fase iniziale, "dice Anat Akiva, assistente professore di biologia cellulare presso Radboudumc. "Mostriamo che entrambi i tipi di cellule producono le proteine di cui hanno bisogno per la loro funzionalità, e mostriamo con il massimo dettaglio che la matrice è in realtà la matrice ossea che vediamo nel tessuto reale".
Il fatto che sia ora possibile una rappresentazione semplificata della formazione dell'osso a livello molecolare offre possibilità senza precedenti, secondo i ricercatori. "Un osso è composto per il 99% da collagene e minerali, ma c'è anche un altro 1% di proteine che sono essenziali per una formazione ossea di successo, " spiega il professor Nico Sommerdijk di Radboudumc. "Allora qual è il ruolo di queste proteine? Come supportano la formazione ossea? Mai prima d'ora siamo stati in grado di guardare le pietre miliari di questo processo a livello molecolare".
E con ciò, hanno immediatamente un buon ingresso per indagare sulla causa di malattie ossee genetiche come la "malattia delle ossa fragili" e le loro possibili cure. "Ricordate che l'origine di molte malattie è a livello molecolare, e così anche il trattamento, " dice Akiva. "In effetti, ora abbiamo un sistema semplice in un ambiente affidabile in cui possiamo curiosare e vedere come le cellule ossee reagiscono agli stimoli che forniamo".