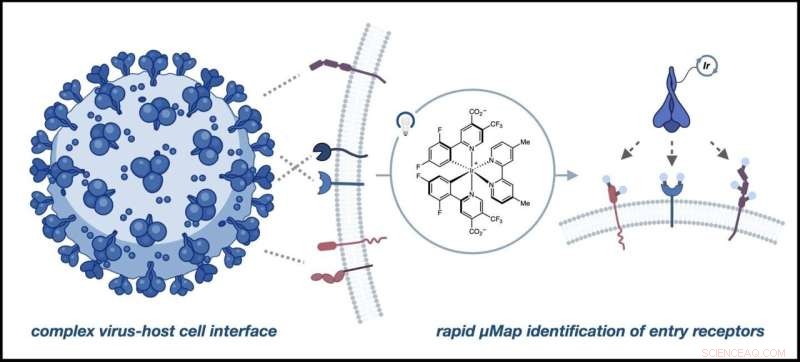
La cellula ospite e l'interfaccia del virus possono essere complesse e coinvolgere molte proteine, ma µMap consente l'interrogazione diretta di interazioni funzionalmente importanti. Credito:Saori Suzuki et al, Rivista della American Chemical Society (2022). DOI:10.1021/jacs.2c06806
Uno dei fattori essenziali di cui il virus COVID-19 ha bisogno per entrare in un ospite è un recettore su una cellula umana, un luogo in cui la proteina spike universalmente riconosciuta può attaccarsi alla superficie cellulare, perforarla, rigettare il suo contenuto infettivo e replicarsi.
Senza un recettore, non c'è replicazione. Senza replica, non c'è infezione.
I ricercatori del Dipartimento di Chimica e del Dipartimento di Biologia Molecolare dell'Università di Princeton hanno utilizzato una tecnologia di mappatura cellulare chiamata µMap, introdotta solo due anni fa dal MacMillan Lab, per scoprire otto punti di interesse precedentemente sconosciuti per la proteina spike.
Quattro di loro, hanno scoperto i ricercatori, sono funzionalmente importanti per l'ingresso virale.
La ricerca è stata pubblicata all'inizio di questo mese nel Journal of the American Chemical Society (JACS) . Potrebbe ampliare la suite di strumenti utilizzati per combattere il virus, in particolare perché muta ed evolve i modi per eludere i vaccini.
Il progetto di collaborazione è stato avviato al culmine dell'incertezza pandemica due anni fa sotto Alexander Ploss, un importante virologo e professore di biologia molecolare, e David MacMillan, il Distinguished University Professor James S. McDonnell e un premio Nobel per la chimica.
Da quando il virus SARS-CoV-1 è apparso nel 2003, gli scienziati sanno che il suo principale recettore virale era un enzima chiamato enzima di conversione dell'angiotensina 2, o ACE2. Questo enzima è stato confermato nel 2020 come lo stesso recettore per SARS-CoV-2, il virus che causa il COVID-19.
Ma il progetto Princeton è partito dal presupposto che ACE2 non fosse l'unica storia.
"Sapevamo che ci sono alcune molecole ospiti da cui questo virus dipende assolutamente per entrare nelle cellule polmonari per causare l'infezione, e una di queste molecole si chiama ACE2", ha detto Ploss. "Quindi in pratica abbiamo detto, ok, vediamo se c'è di più là fuori. Abbiamo cercato raccoglitori immediati.
"Ma come puoi immaginare, il processo di ingresso è complesso. Il virus si attacca a qualcosa e quindi deve ancora passare attraverso la membrana cellulare per entrare in una cellula, e lungo questo percorso potrebbe interagire con altri fattori dell'ospite. Voglio dire che tutto è dettato dall'ingresso del virus. Ovviamente, ci sono un certo numero di processi ugualmente essenziali all'interno della cellula dopo l'ingresso del virus che possono influenzare la gravità della malattia.
"Ma è ovviamente il primo passo fondamentale. Se il virus non riesce a entrare, il gioco è finito."
Steve Knutson, coautore dell'articolo e ricercatore post-dottorato presso il MacMillan Lab, ha aggiunto:"Sebbene la scoperta di ACE2 come principale recettore sia stata un'enorme pietra miliare, di certo non racconta l'intera storia della patologia COVID. La biologia può essere intrinsecamente promiscua e abbiamo indovinato correttamente che la proteina spike SARS-CoV-2 interagisce con più proteine della cellula ospite per l'ingresso."
Ha aggiunto che indagini come questa sono una ricerca "perfetta" adatta alla tecnologia µMap.
Il picco come antenna µMap
Micromap (µMap) è una tecnologia di etichettatura di prossimità che identifica i "vicini" di proteine ed enzimi sulla superficie di una cellula. Utilizza un fotocatalizzatore, una molecola che, quando attivata dalla luce, stimola una reazione chimica, per segnalare queste relazioni spaziali generando un marcatore che contrassegna i vicini molecolari.
In questo lavoro, i ricercatori hanno utilizzato la stessa proteina spike come marcatore o "antenna" per contrassegnare tutti i siti recettoriali nelle vicinanze di ACE2.
"Alex ha avuto questo grande istinto che ci sono altre cose oltre a ACE2 che potrebbero permetterti di pensare all'infettività", ha detto MacMillan. "Quindi quello che abbiamo fatto è stato mettere questo fotocatalizzatore - e li chiamiamo antenne - sulla proteina spike, in modo che ogni volta che si lega a cose sulla cellula vicino a ACE2, questa piccola antenna assorbe l'energia fotonica, la luce.
"Ma non può cedere quell'energia su lunghe distanze. Può darla solo a ciò che è vicino. La molecola che fluttua liberamente deve sostanzialmente incontrarla entro due nanometri", ha aggiunto MacMillan. "Quindi sappiamo cosa c'è accanto. Sappiamo cosa interagisce con esso."
Dopo che la tecnologia ha identificato otto nuovi recettori che hanno interagito con la proteina spike, gli scienziati li hanno caratterizzati utilizzando una pseudoparticella virale. (Una pseudoparticella imita l'ingresso virale ma non trasporta il materiale genetico per diffondere il virus.) Hanno quindi isolato quattro fattori di ingresso degni di ulteriori indagini.
"Il sistema di pseudoparticelle ci consente di disaccoppiare l'assorbimento virale e studiare il processo di ingresso da tutto ciò che è a valle del ciclo infettivo", ha affermato Ploss. "Se stai cercando l'impatto di determinati fattori dell'ospite sull'ingresso, vuoi vedere che puoi studiarlo indipendentemente dalla replicazione. Quindi qui, fondamentalmente stiamo introducendo un gene reporter nella cellula e possiamo quindi quantificare l'efficienza dell'ingresso ha avuto luogo."
MacMillan ha affermato che sono necessari ulteriori lavori per determinare in definitiva la funzione dei recettori, ma i ricercatori si chiedono se potrebbero portare un indizio sulla gravità della malattia.
"Non possiamo dire che tutti e otto i fattori siano correlati all'ingresso di SARS-CoV-2", ha affermato Saori Suzuki, ricercatore associato presso il Ploss Lab. "Quattro fattori su otto sono risultati eccezionali in base alla valutazione virologica. Dobbiamo valutare di più e valutare in modo più preciso.
"Nel passaggio successivo, dobbiamo valutare in che modo questi fattori supportano ACE2 per l'ingresso del virus e se le nuove varianti virali emergenti utilizzano lo stesso insieme di fattori". + Esplora ulteriormente